Nat. Commun. | 低复杂度重复序列介导的RNA–RNA相互作用: 机制解析与深度学习双链预测框架
Nat. Commun. | 低复杂度重复序列介导的RNA–RNA相互作用: 机制解析与深度学习双链预测框架

DrugAI
发布于 2026-01-27 15:14:02
发布于 2026-01-27 15:14:02
DRUGONE
RNA–RNA 相互作用在基因调控和 RNA 代谢中发挥核心作用,但其序列层面的决定因素仍不清楚。研究人员系统分析了多种转录组尺度的 RNA–RNA 相互作用数据,发低复杂度重复序列(low-complexity repeats, LCRs)是驱动 RNA–RNA 相互作用的关键序列特征。LCR 使 RNA 能够与多个互作伙伴形成热力学稳定的双链结构,从而在 RNA 互作网络中充当“枢纽”。这些相互作用广泛参与 RNA 稳定性、翻译调控及发育相关过程。
基于这一发现,研究人员构建了深度学习模型 RIME,利用核酸语言模型的序列嵌入表示来预测 RNA–RNA 相互作用。RIME 在多种数据集上均优于传统基于热力学的预测方法,能够有效捕捉 LCR 的作用,并准确识别高置信度、具有生物学功能的 RNA–RNA 相互作用。

RNA 不仅是遗传信息的载体,还通过 RNA–RNA 相互作用参与转录、剪接、稳定性控制和翻译调控等关键过程。近年来,多种高通量技术实现了 RNA–RNA 相互作用的系统性测绘,揭示了其在细胞中的广泛存在。然而,决定 RNA–RNA 相互作用特异性和稳定性的序列规则仍缺乏系统认识。
已有研究提示,重复序列可能在 RNA–RNA 相互作用中发挥重要作用,但相关证据零散,缺乏大规模、系统性的验证。同时,传统基于热力学的计算方法在预测长 RNA 之间的相互作用方面存在明显局限。随着语言模型在生物序列建模中的成功应用,研究人员希望借助深度学习方法,从序列层面重新理解 RNA–RNA 相互作用的决定机制。
方法
研究人员整合了多种转录组尺度 RNA–RNA 相互作用数据,重点保留来源于成熟转录本的跨分子双链结构,并系统过滤高丰度 RNA 和小 RNA 的干扰。通过重复序列注释、富集分析和网络分析,评估低复杂度重复序列在 RNA–RNA 相互作用中的作用。在模型构建方面,研究人员基于核酸语言模型生成的序列嵌入,训练深度神经网络 RIME,用于区分真实 RNA–RNA 相互作用与非互作区域,并在多个独立数据集上进行系统评估。
结果
RNA–RNA 相互作用显著富集低复杂度重复序列
在多种实验数据中,RNA–RNA 相互作用区域显著富集简单重复和低复杂度序列。这一现象在不同物种和不同实验平台中高度一致,表明 LCR 是普遍存在的序列特征。
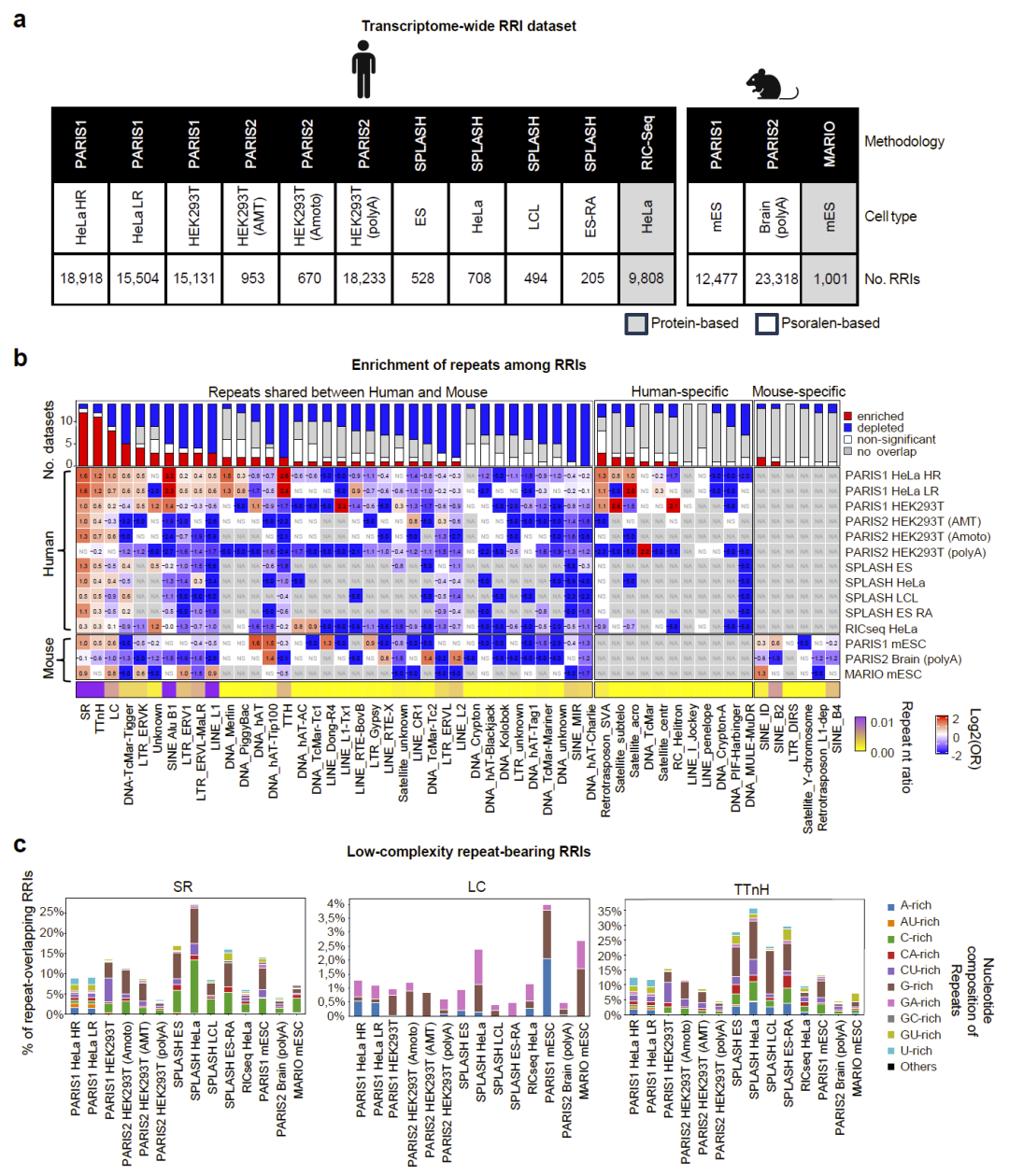
图 1:RNA–RNA 相互作用数据构建与重复序列富集分析。
含 LCR 的相互作用区域更易结合调控蛋白并发生 RNA 编辑
含 LCR 的 RNA–RNA 相互作用区域更频繁地与调控 RNA 稳定性和翻译的 RNA 结合蛋白重叠,同时也是 RNA 编辑酶偏好的作用位点,提示其在转录后调控中的功能重要性。
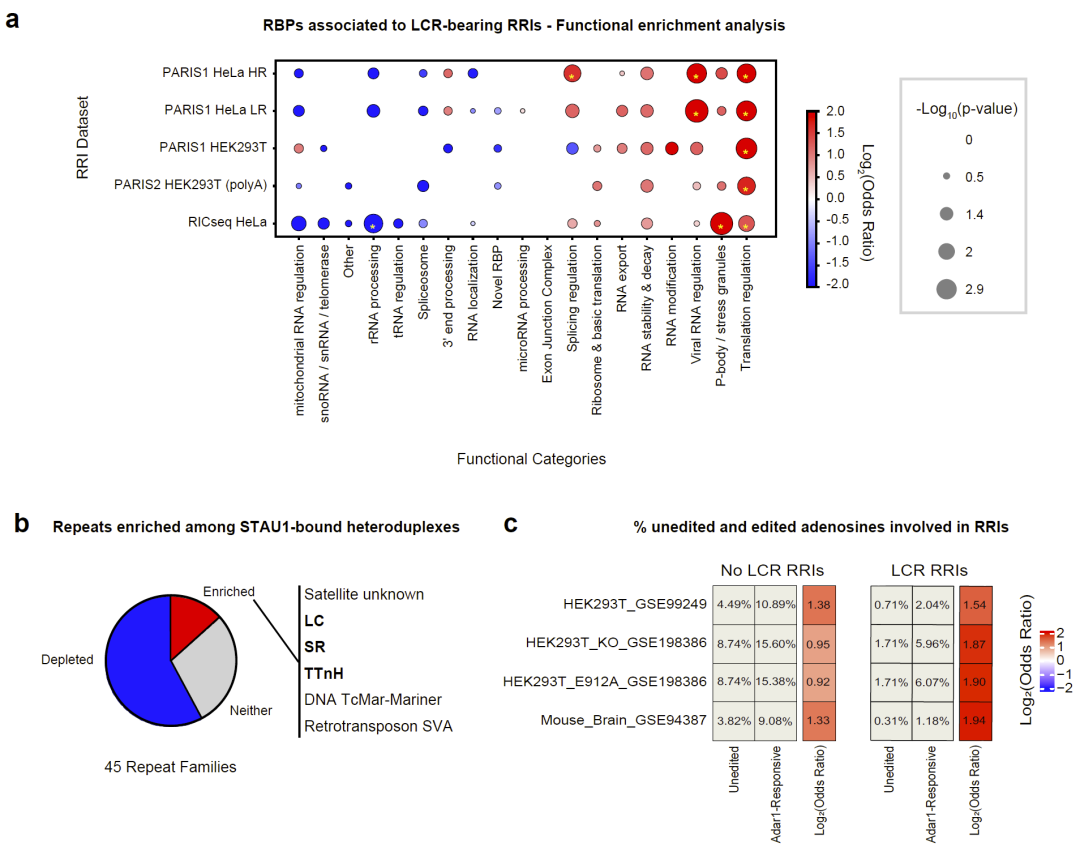
图 2:LCR、RNA 结合蛋白与 RNA 编辑的关联。
LCR 促进多重 RNA–RNA 互作并形成网络枢纽
网络分析显示,含 LCR 的 RNA 区域更可能与多个 RNA 形成相互作用,在互作网络中处于中心位置。这种多价互作能力是其他类型重复序列所不具备的。
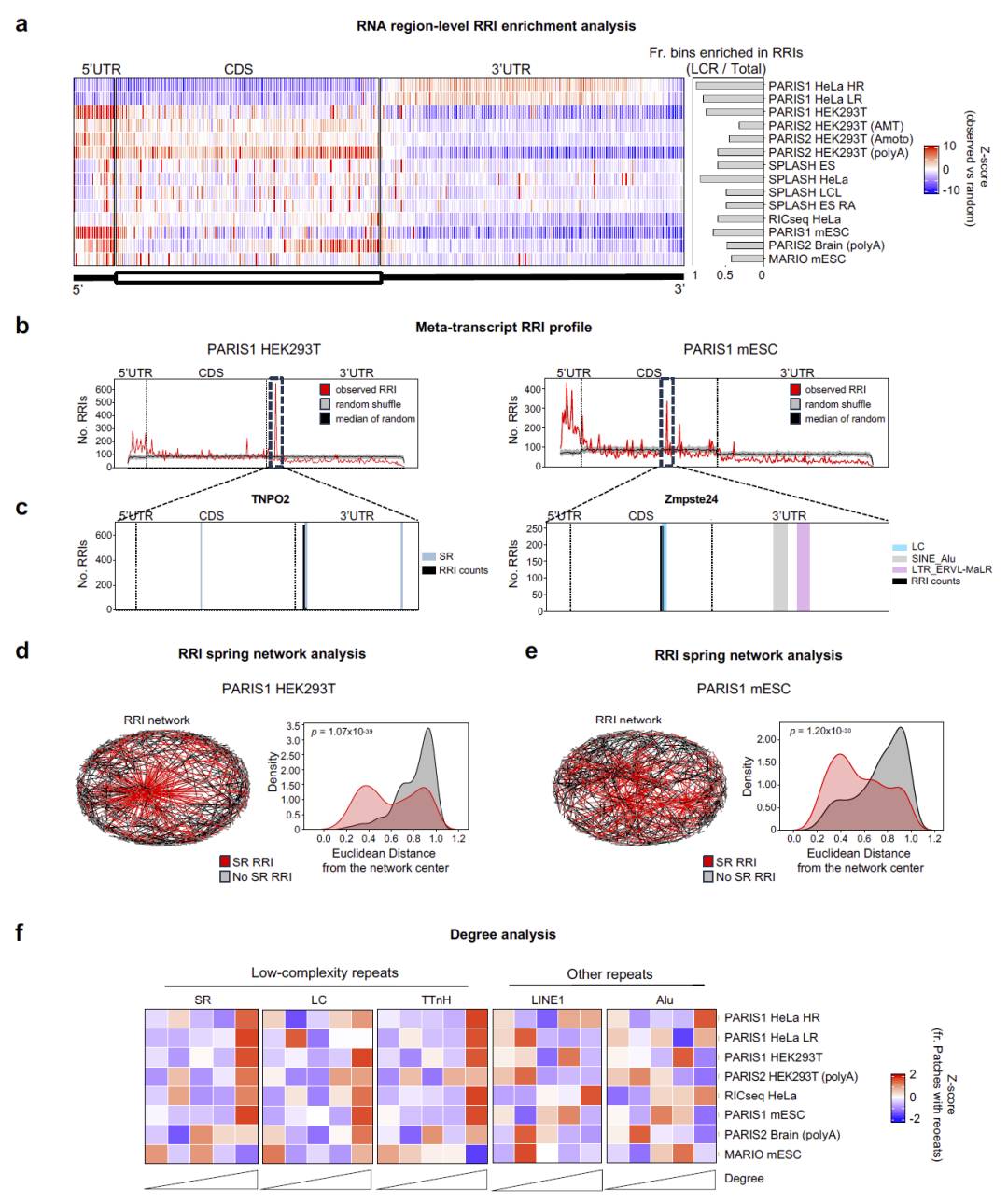
图 3:RNA–RNA 相互作用网络与枢纽特性。
互补的低复杂度重复介导 lncRNA–靶 RNA 相互作用
在特定 lncRNA 的靶向研究中,研究人员发现 lncRNA 与其靶 RNA 之间常通过互补的低复杂度重复序列形成双链结构,验证了 LCR 在靶向调控中的直接作用。
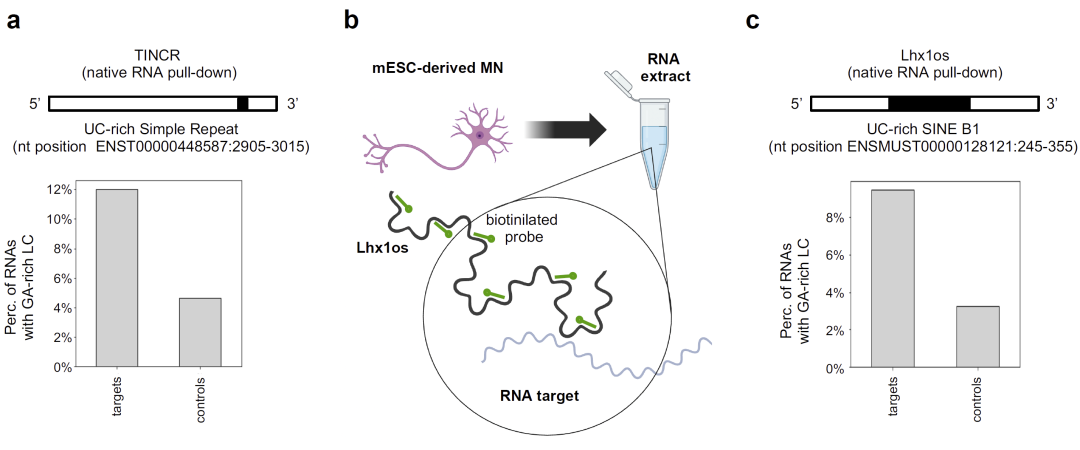
图 4:lncRNA–RNA 相互作用中的低复杂度重复。
LCR 介导的 RNA–RNA 相互作用具有更高热力学稳定性
热力学分析表明,含 LCR 的相互作用在能量上更有利,尽管其局部结构可能较为稳定,但仍能重排形成更稳定的跨分子配对。
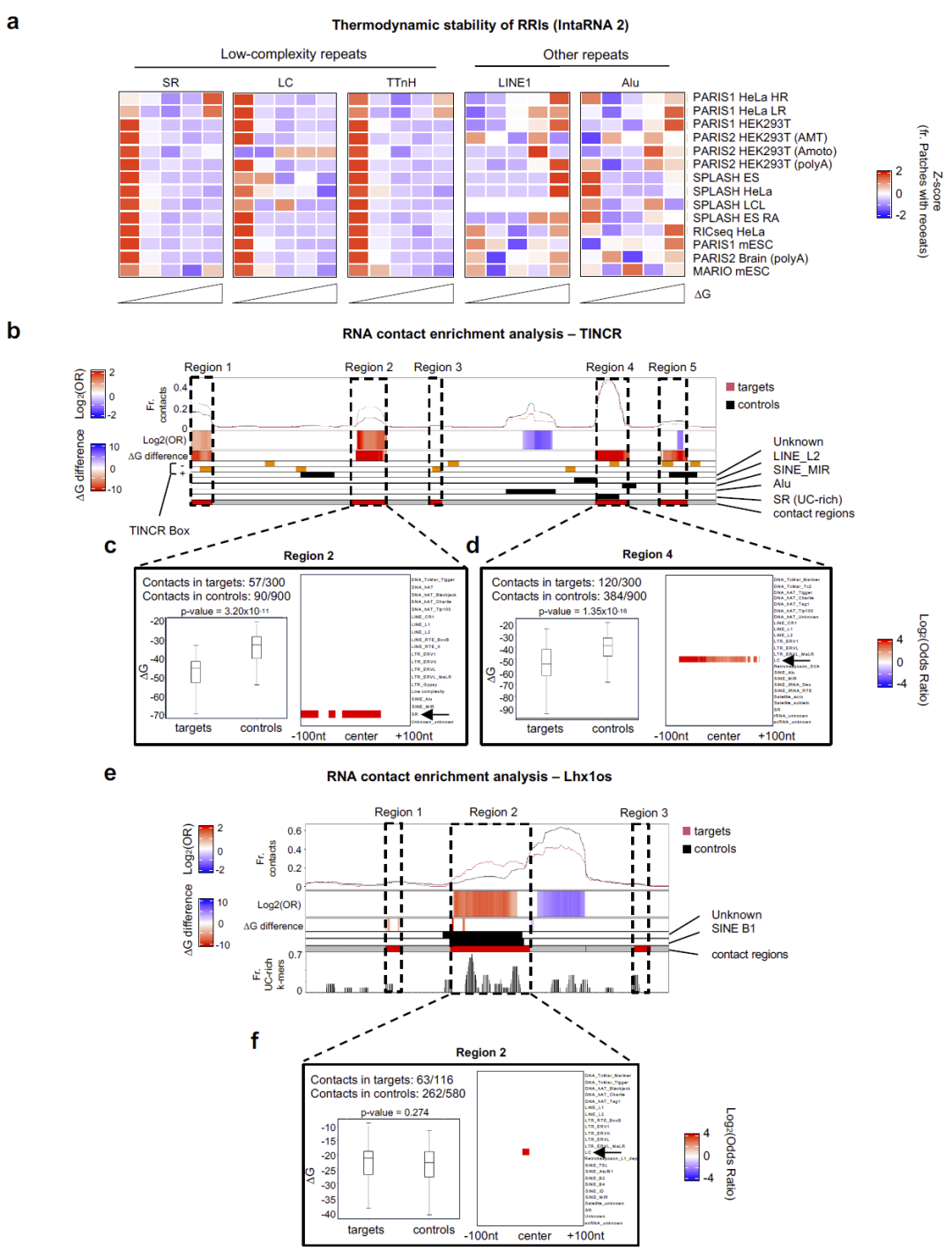
图 5:低复杂度重复与相互作用稳定性。
基于语言模型的深度学习框架 RIME
研究人员构建了 RIME 模型,利用语言模型嵌入表示 RNA 序列特征,从而捕捉传统热力学方法难以描述的相互作用模式。
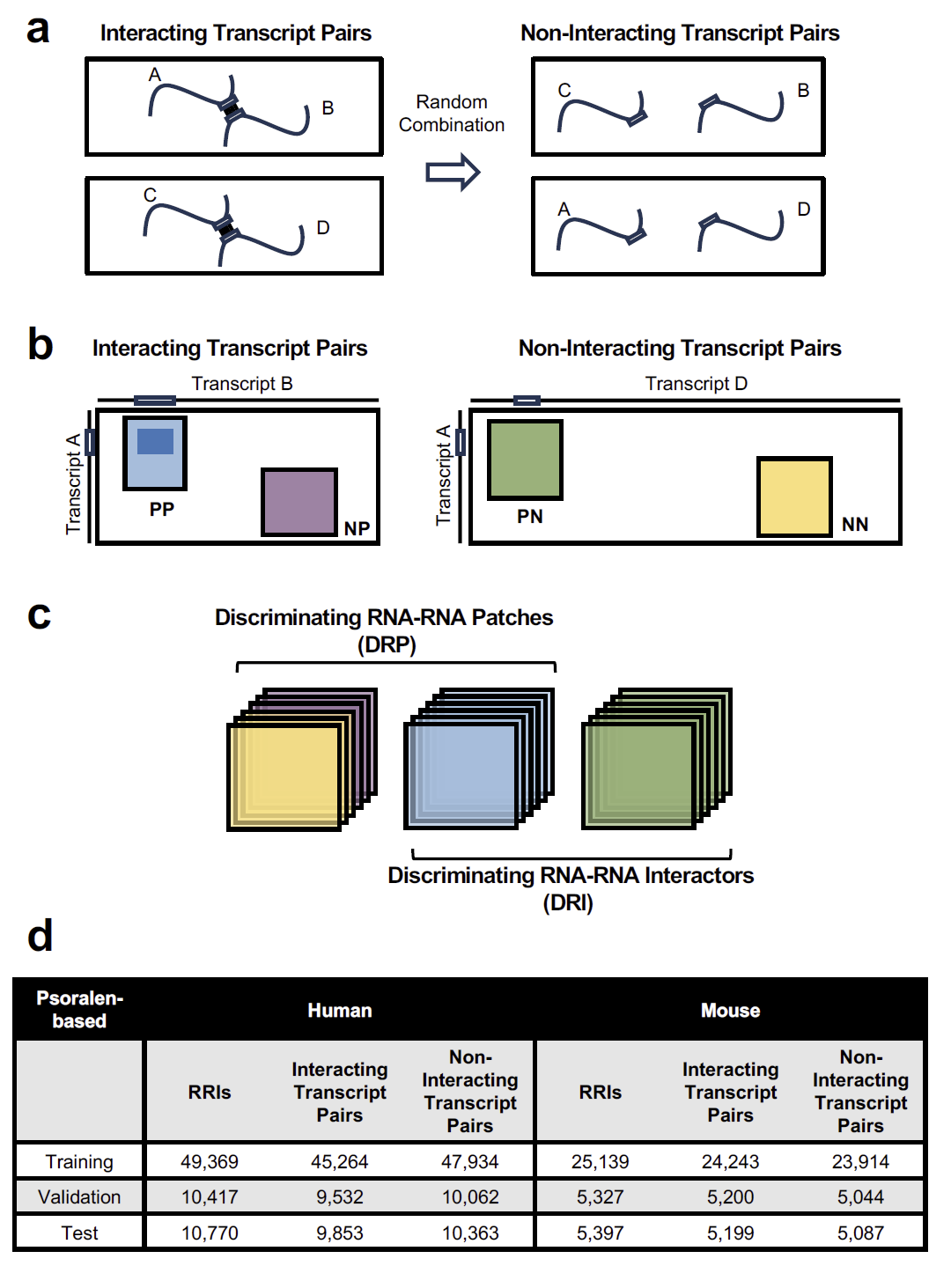
图 6:RIME 模型架构与训练策略。
RIME 显著优于传统预测方法
在多种高质量数据集上,RIME 在预测准确率和鲁棒性方面均显著优于现有热力学模型及其他深度学习方法。
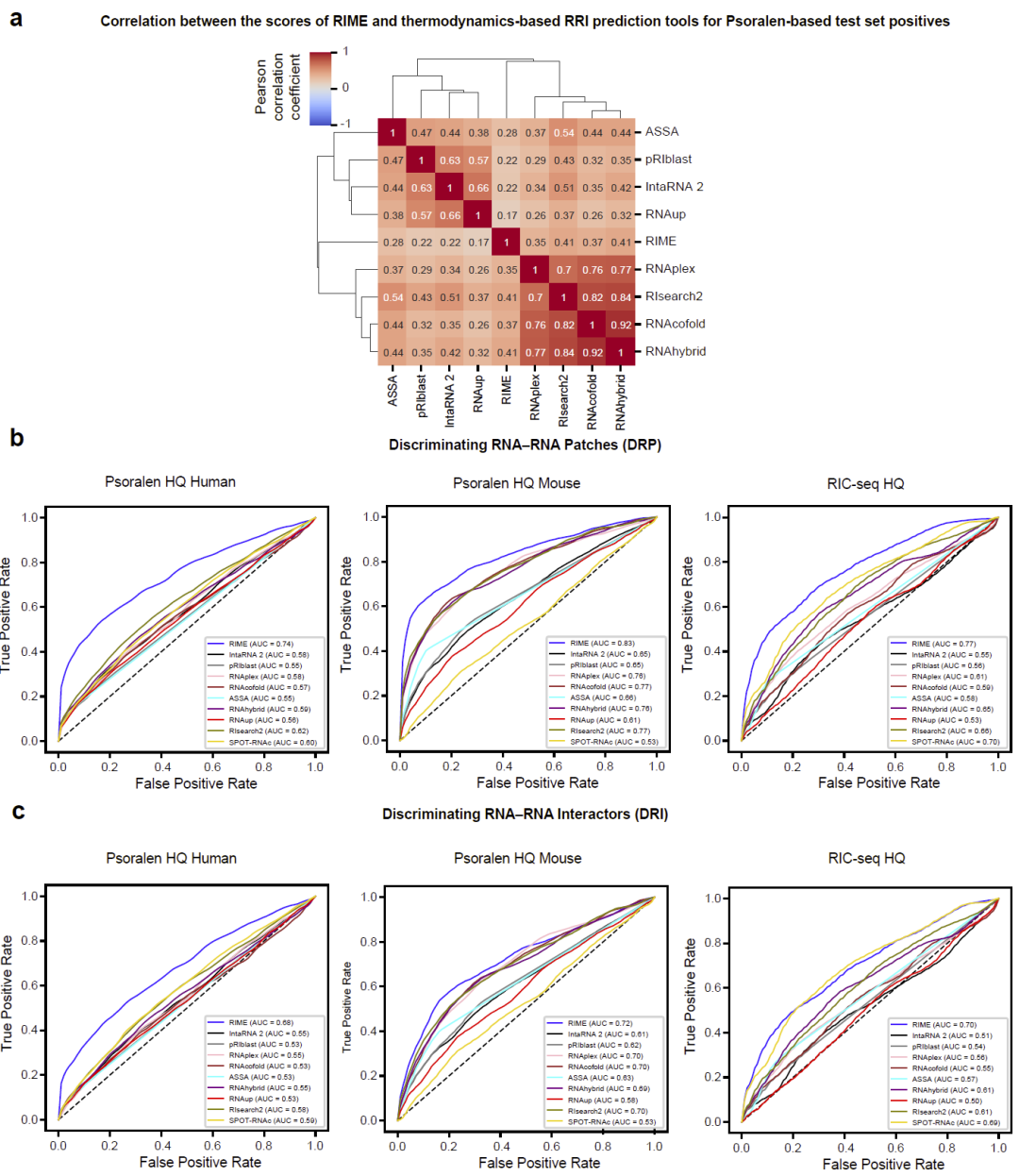
图 7:RIME 与其他方法的性能比较。
RIME 捕捉 RNA 相互作用的关键序列决定因素
模型解释性分析显示,RIME 自动学习到 LCR 在 RNA–RNA 相互作用中的关键作用,并能够定位潜在的互作区域。
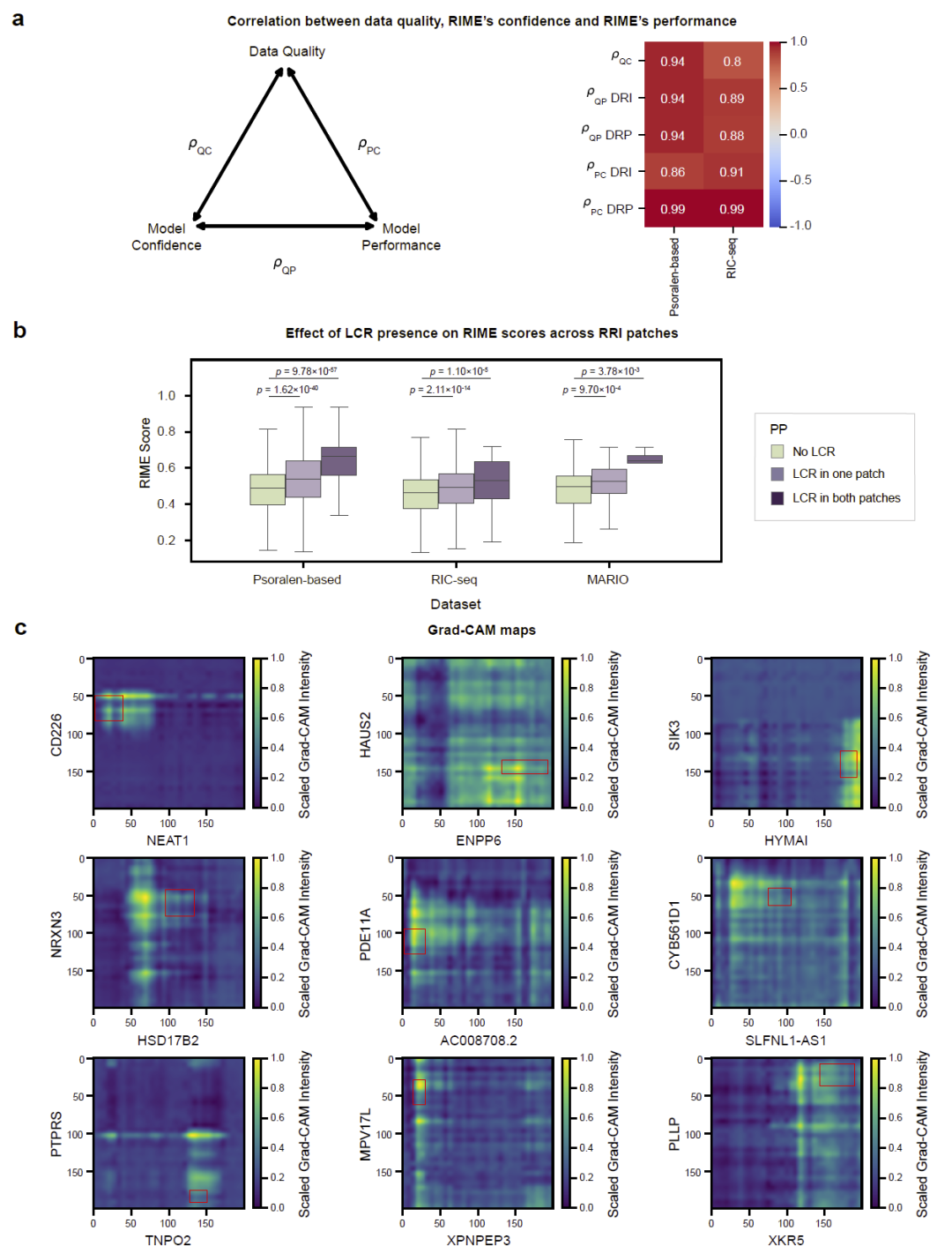
图 8:RIME 的预测置信度与特征解释。
RIME 准确预测功能性 RNA–RNA 相互作用
在多个已验证的 RNA–RNA 相互作用案例中,RIME 成功识别关键互作区域,并在转录内和转录间相互作用预测中均表现出良好泛化能力。
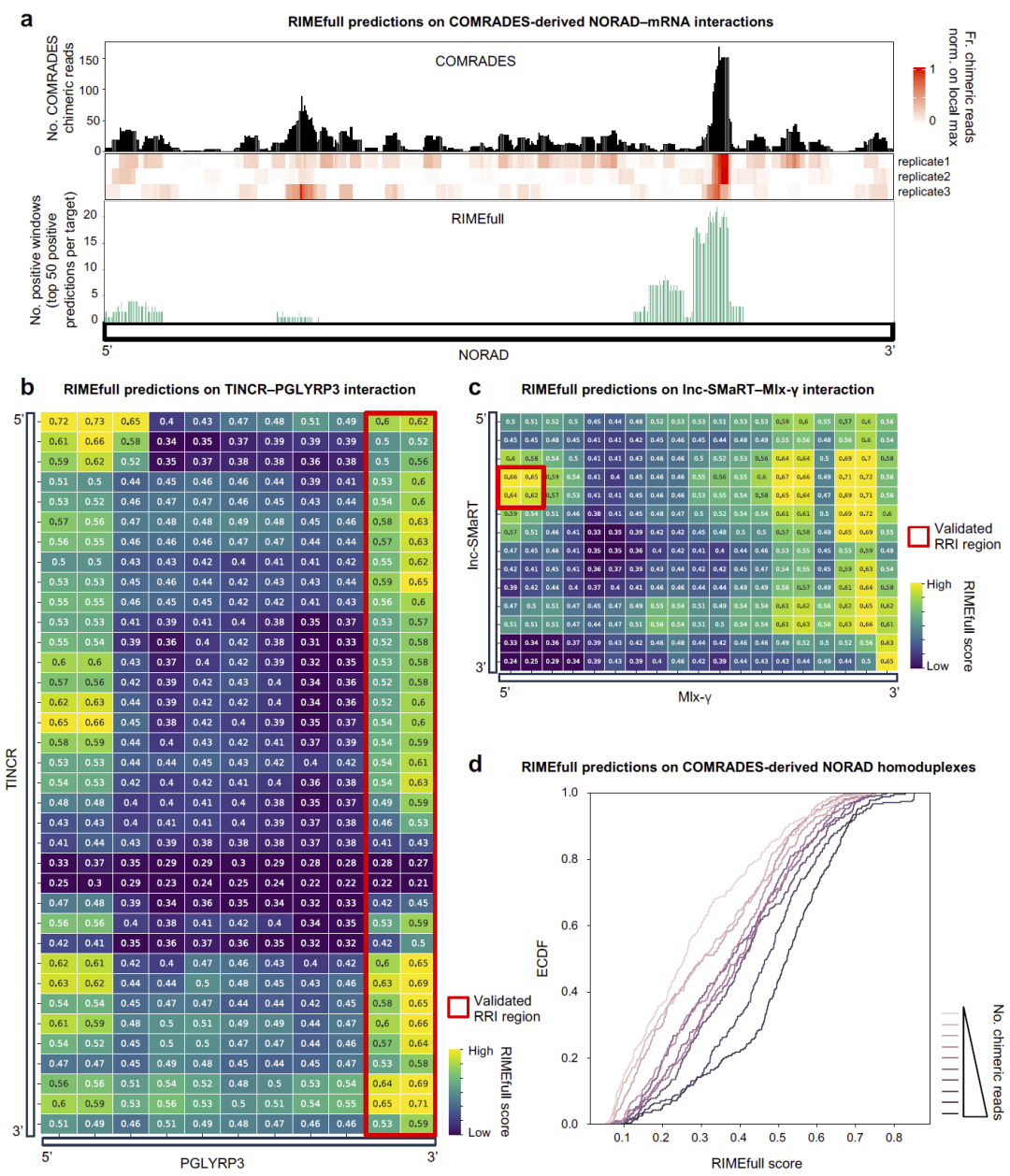
图 9:RIME 在功能性实例中的应用。
讨论
本研究首次在转录组尺度系统性地证明了低复杂度重复序列是 RNA–RNA 相互作用的核心序列决定因素。LCR 通过其简单、可扩展的序列特性,为 RNA 提供多价互作能力,使其在 RNA 调控网络中充当“粘性枢纽”。这些特性不仅与发育调控密切相关,也可能在神经系统疾病等病理状态中发挥作用。
在方法学层面,RIME 证明了基于语言模型的深度学习框架能够有效突破传统热力学模型的限制,为 RNA–RNA 相互作用预测提供了新的范式。研究人员认为,该框架未来可与表达调控和疾病数据整合,用于解析复杂 RNA 调控网络并探索潜在的治疗靶点。
整理 | DrugOne团队
参考资料
Setti, A., Bini, G., Flaminia, P. et al. The role of low-complexity repeats in RNA–RNA interactions and a deep learning framework for duplex prediction. Nat Commun (2026).
https://doi.org/10.1038/s41467-026-68356-w
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-01-23,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

