Nat. Commun. | 基于空间转录组数据的基因标记与细胞类型的稳健可解释预测
Nat. Commun. | 基于空间转录组数据的基因标记与细胞类型的稳健可解释预测

DrugAI
发布于 2026-01-27 14:26:05
发布于 2026-01-27 14:26:05
DRUGONE
空间转录组(Spatial Transcriptomics, ST)技术将组织形态与基因表达联系起来,为数字病理学提供了新的研究范式。然而,空间转录组实验成本高、流程复杂,限制了其在临床中的广泛应用。近年来,深度学习方法被用于直接从常规 H&E 组织切片中预测基因表达和细胞类型,但在稳健性、不确定性评估和可解释性方面仍存在明显不足。
研究人员提出 STimage,一种稳健且可解释的深度学习框架,可直接从 H&E 图像中预测空间基因表达并识别细胞类型。该方法通过概率建模预测基因表达分布,并显式量化数据不确定性与模型不确定性,同时结合单细胞尺度的可解释性分析,将模型预测与病理学特征和功能基因联系起来。研究人员在多种癌症与非肿瘤数据集中验证了 STimage 的泛化能力,并进一步展示了其在患者生存分层和药物响应预测中的潜在临床价值。

H&E 染色是病理诊断中最常用的组织学手段,但传统人工阅片过程耗时且主观性强,且许多在分子层面差异显著的细胞类型难以通过形态直接区分。空间转录组技术能够在保留组织结构的前提下测量上万基因的表达,为理解肿瘤异质性提供了关键工具。然而,其高昂成本和有限可及性限制了临床应用。
为提升可扩展性,研究人员尝试利用深度学习模型从组织图像中推断空间基因表达,但现有方法多给出确定性预测,缺乏对预测不确定性的量化,也难以解释模型究竟依赖了哪些形态学特征。这在临床场景中会降低模型的可信度和可用性。因此,亟需一种同时具备稳健性、不确定性评估能力和可解释性的图像到分子预测框架。
方法
STimage 以空间转录组数据与对应的 H&E 图像作为训练输入,将组织图像切分为与空间测序位点对应的小块,并进行染色归一化和低组织覆盖区域过滤。模型利用预训练卷积神经网络或病理基础模型提取图像特征,并通过概率回归模块预测每个基因在空间位置上的表达分布,而非单一数值。同时,研究人员采用模型集成策略区分数据本身的不确定性与模型不确定性。在可解释性方面,STimage 结合核分割与局部可解释方法,在单细胞尺度上定位对基因预测贡献最大的组织结构。
结果
STimage 框架与整体性能
STimage 能够从 H&E 图像中稳定预测空间基因表达模式,并在多个独立数据集上保持一致表现,显示出良好的跨平台和跨样本稳健性。
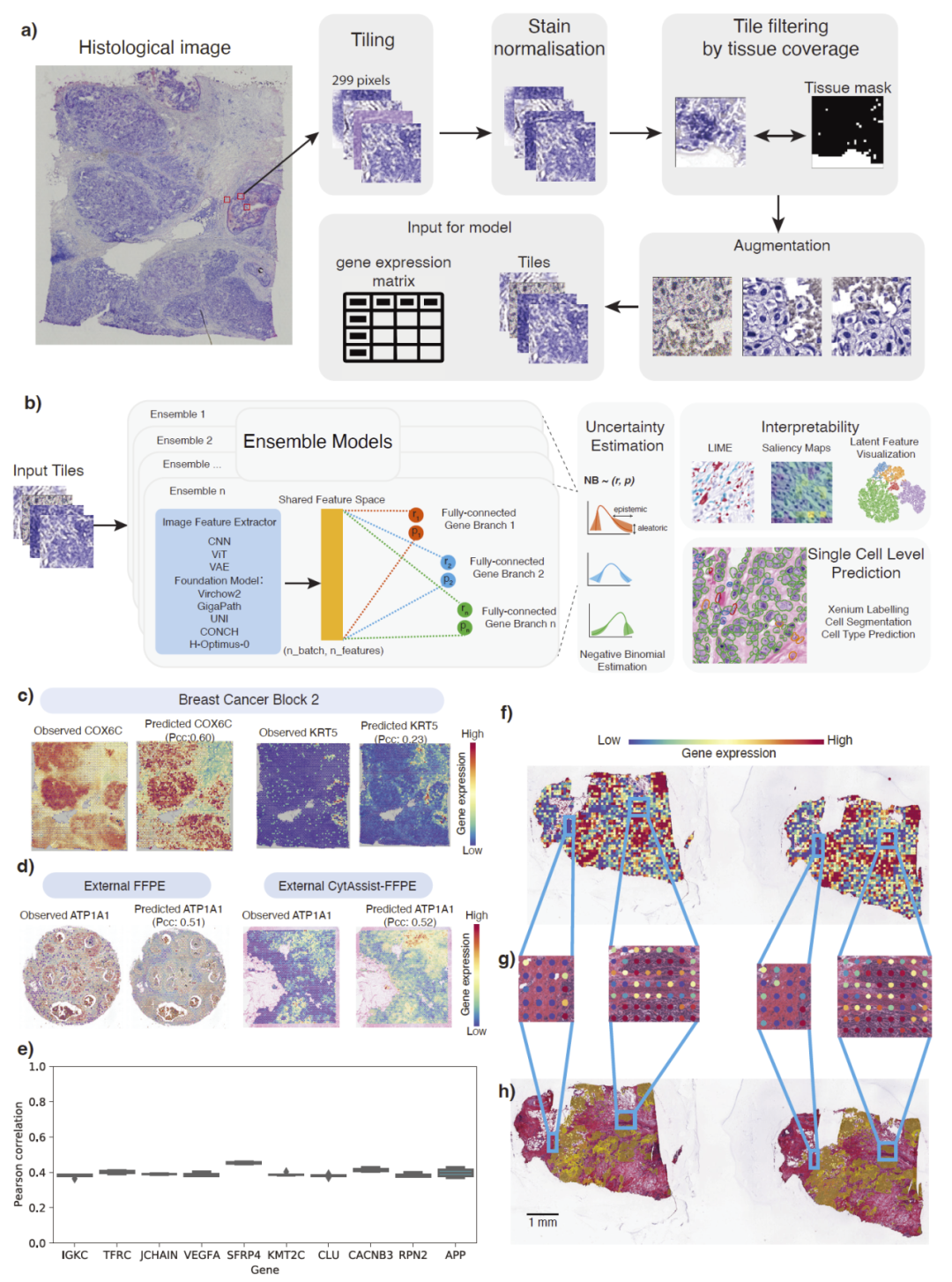
图1|STimage 的整体流程与模型架构。
空间基因表达预测的准确性
在乳腺癌等数据集中,STimage 对高表达与低表达基因均能重现真实的空间分布模式,预测结果在空间自相关指标上与实验测量高度一致。
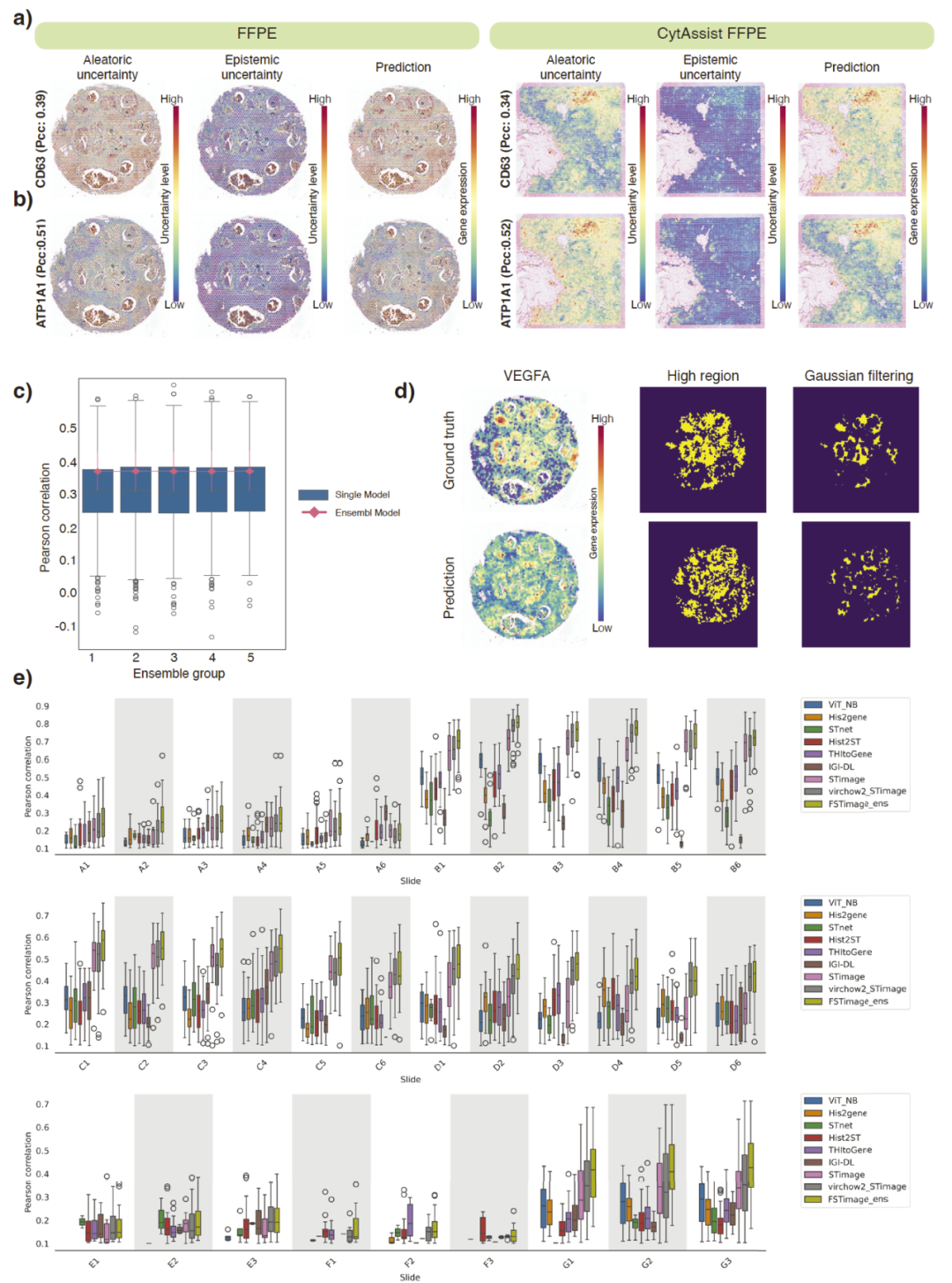
图2|真实与预测空间基因表达模式的对比。
跨数据集与跨技术平台的稳健性
研究人员将模型训练于一种实验条件下的数据,并应用于不同制备方式和不同实验平台的样本中。结果显示,STimage 在外部分布数据上仍能保持稳定的预测性能,优于多种现有方法。
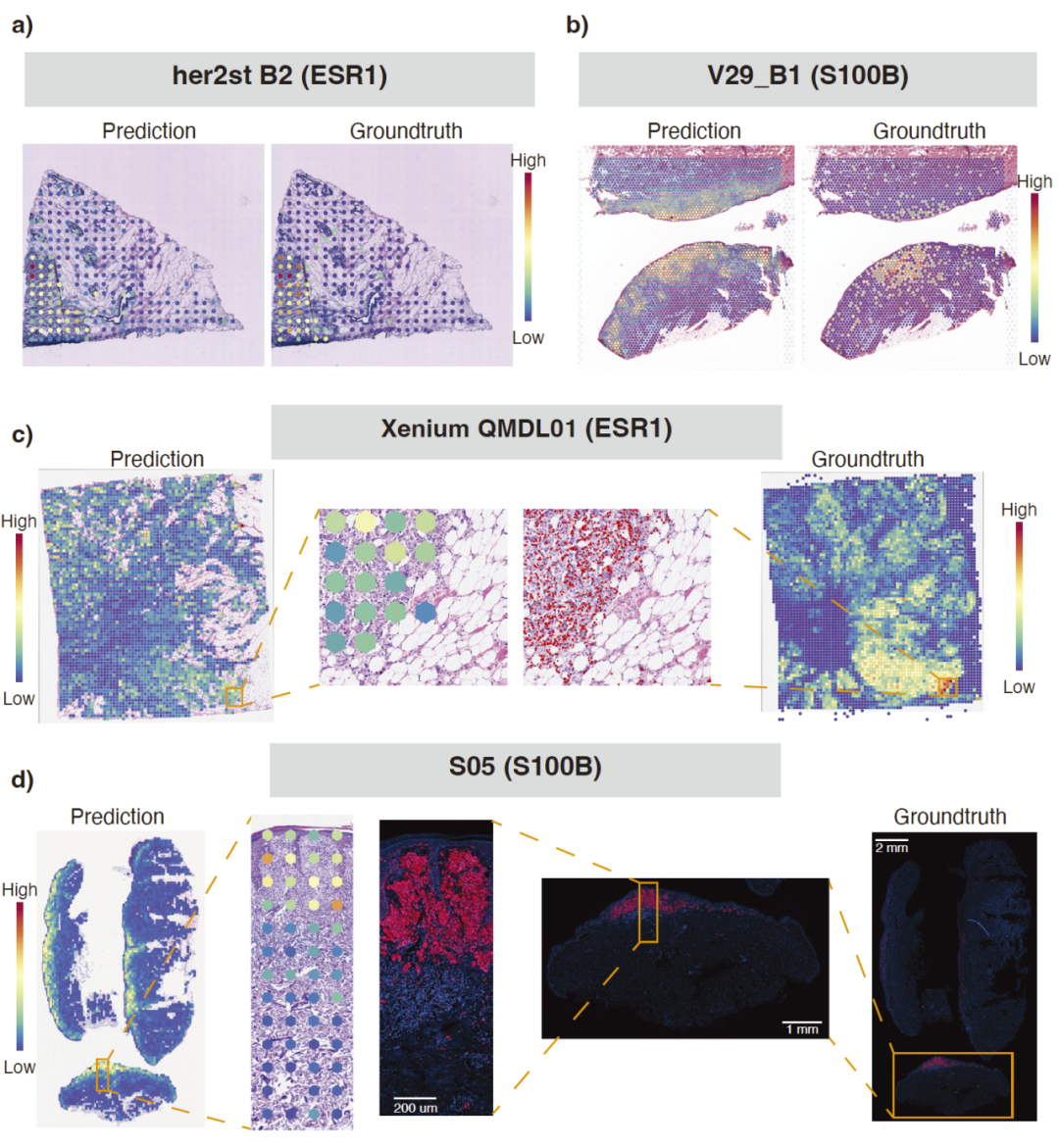
图3|跨平台与跨数据集预测性能评估。
不确定性量化与模型集成优势
通过集成多个模型,STimage 能够为每个空间位置和每个基因同时给出预测值及其不确定性估计。高预测误差区域通常对应较高不确定性,从而为结果解读提供可靠性指示。
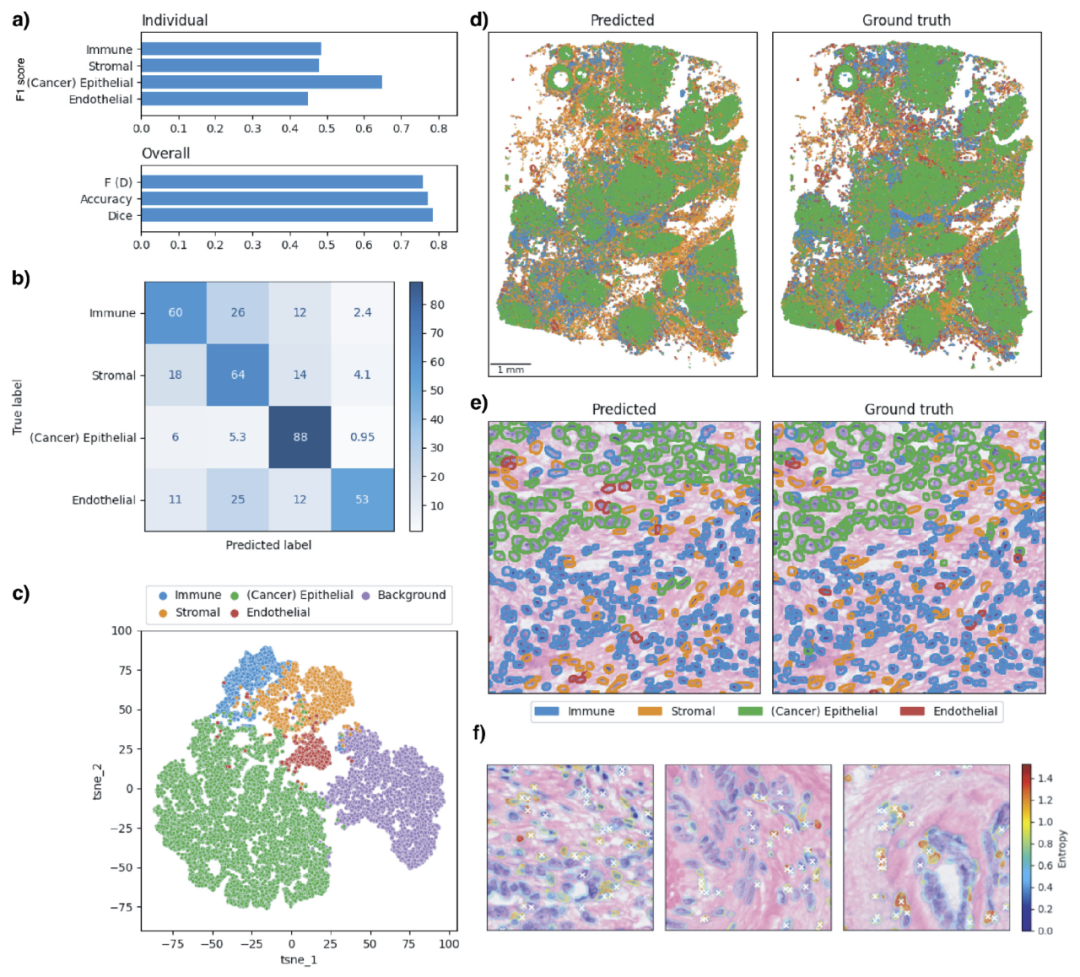
图4|基因表达预测及其不确定性空间分布。
可解释性分析与细胞类型预测
可解释性分析显示,不同细胞核在基因预测中贡献不同,且模型关注的形态学特征与已知病理学知识一致。进一步地,在单细胞分辨率数据上,STimage 能准确区分肿瘤细胞、免疫细胞和基质细胞等主要细胞类型。
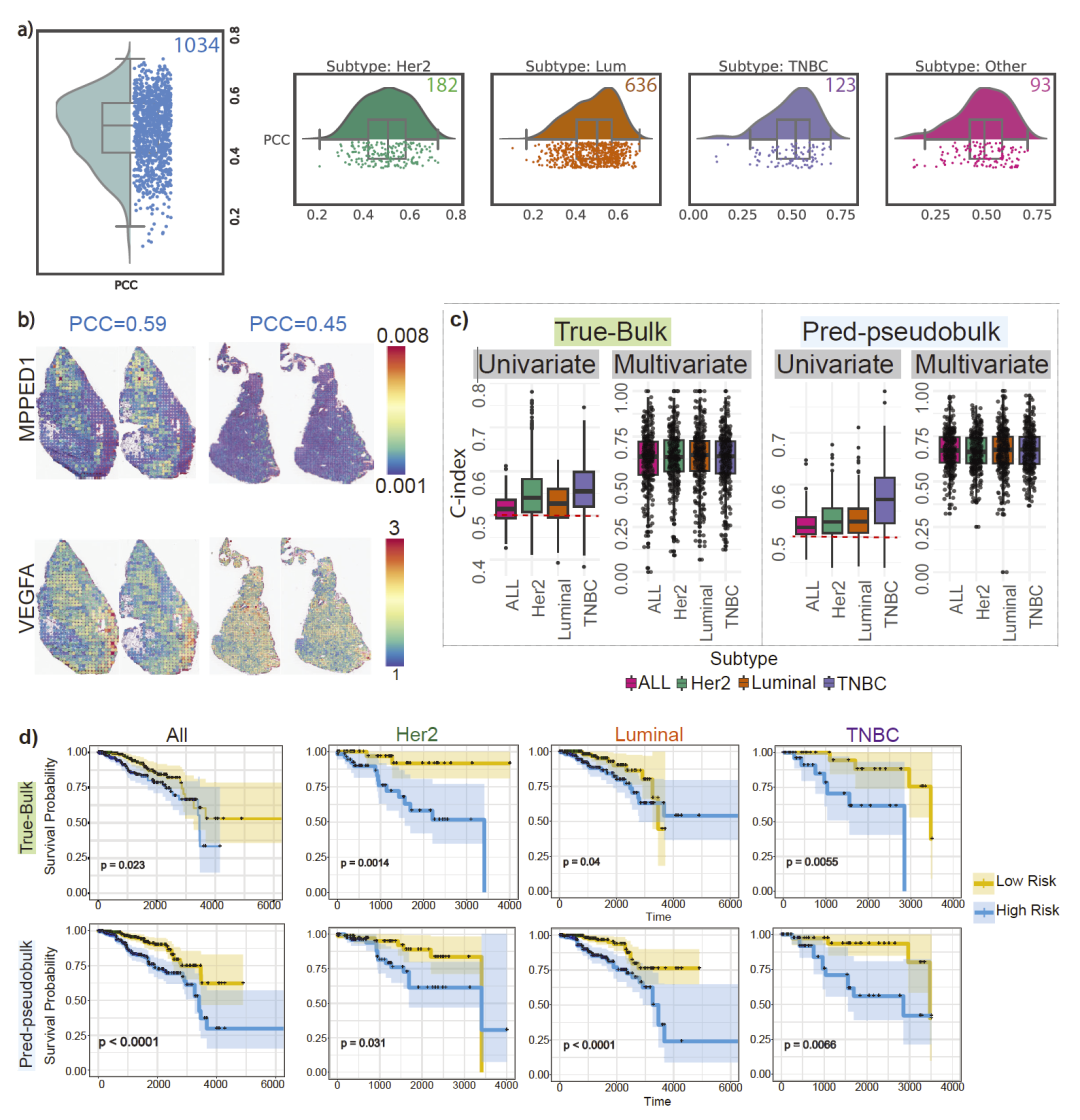
图5|单细胞尺度的可解释性分析与细胞类型预测结果。
讨论
STimage 展示了一种将深度学习、概率建模与病理可解释性相结合的空间转录组分析新范式。通过直接从常规 H&E 图像中推断空间基因表达和细胞类型,研究人员为降低分子病理分析成本提供了可行路径。
与以往方法相比,STimage 的核心优势在于:其一,显式量化预测不确定性,提高了模型在临床应用中的可信度;其二,提供单细胞尺度的可解释性,将模型决策与具体的组织学结构相联系;其三,在多癌种、多平台和多分辨率数据中表现出良好的泛化能力。
总体而言,STimage 为数字病理学和空间转录组数据分析提供了一种稳健、可解释且具有临床潜力的工具,为未来基于图像的分子诊断和精准治疗奠定了基础。
整理 | DrugOne团队
参考资料
Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun (2026).
https://doi.org/10.1038/s41467-026-68487-0
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-01-19,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

