Nat. Comput. Sci. | 上海交大团队推出 EMO,跨表观组图谱解锁非编码变异的基因调控机制
Nat. Comput. Sci. | 上海交大团队推出 EMO,跨表观组图谱解锁非编码变异的基因调控机制

DrugOne
发布于 2025-10-14 16:35:09
发布于 2025-10-14 16:35:09
DRUGONE
大多数与疾病相关的遗传变异位于非编码区,其潜在的调控作用难以直接解析。研究人员提出了 EMO框架,整合跨组织与单细胞尺度的表观组学数据,预测非编码变异对基因表达的影响。该方法结合开放染色质、组蛋白修饰、转录因子结合位点以及三维基因组结构信息,在多个组织和细胞类型中展现出更高的准确性与可解释性。研究结果显示,EMO 不仅能够捕捉组织与细胞特异性的调控模式,还能解释疾病相关变异的分子机制,为精准医学提供新思路。
非编码变异如何影响基因调控,是理解复杂疾病的重要科学问题。已有方法多依赖单一组织或群体水平的统计学推断,往往忽视了组织特异性与单细胞环境的复杂性。随着 ATAC-seq、ChIP-seq 以及单细胞组学的发展,研究人员能够获得更全面的表观组学图谱,为跨尺度预测模型提供了条件。挑战在于如何整合多源数据并提升预测的泛化能力。
结果
模型设计与多组学整合
研究人员提出的 EMO 框架结合了 ATAC-seq、ChIP-seq 与单细胞表观组数据,并引入 Hi-C 等三维基因组结构信息。深度学习模型将这些表观组特征与基因调控网络关联起来,能够预测非编码变异对基因表达的潜在影响。
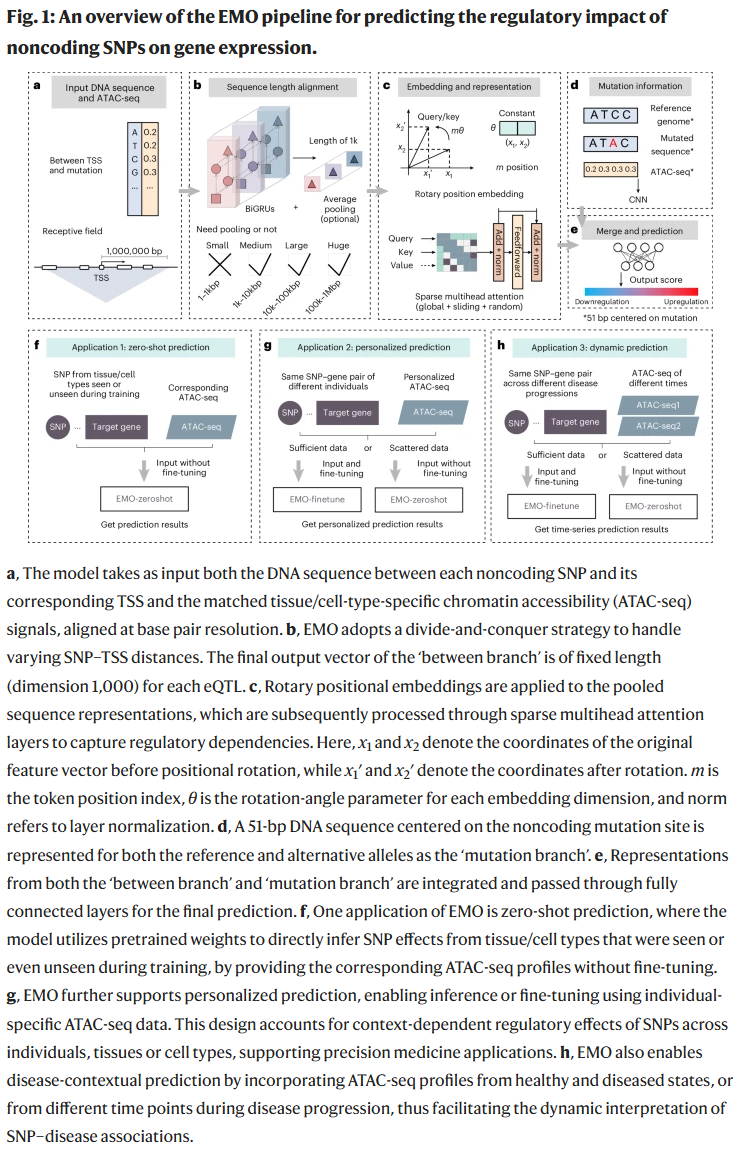
跨组织的预测性能
在肝脏、脑、免疫系统等多种组织中,EMO 成功捕捉了非编码变异的组织特异性调控效应。预测结果与实验数据高度一致,性能显著优于对照方法。
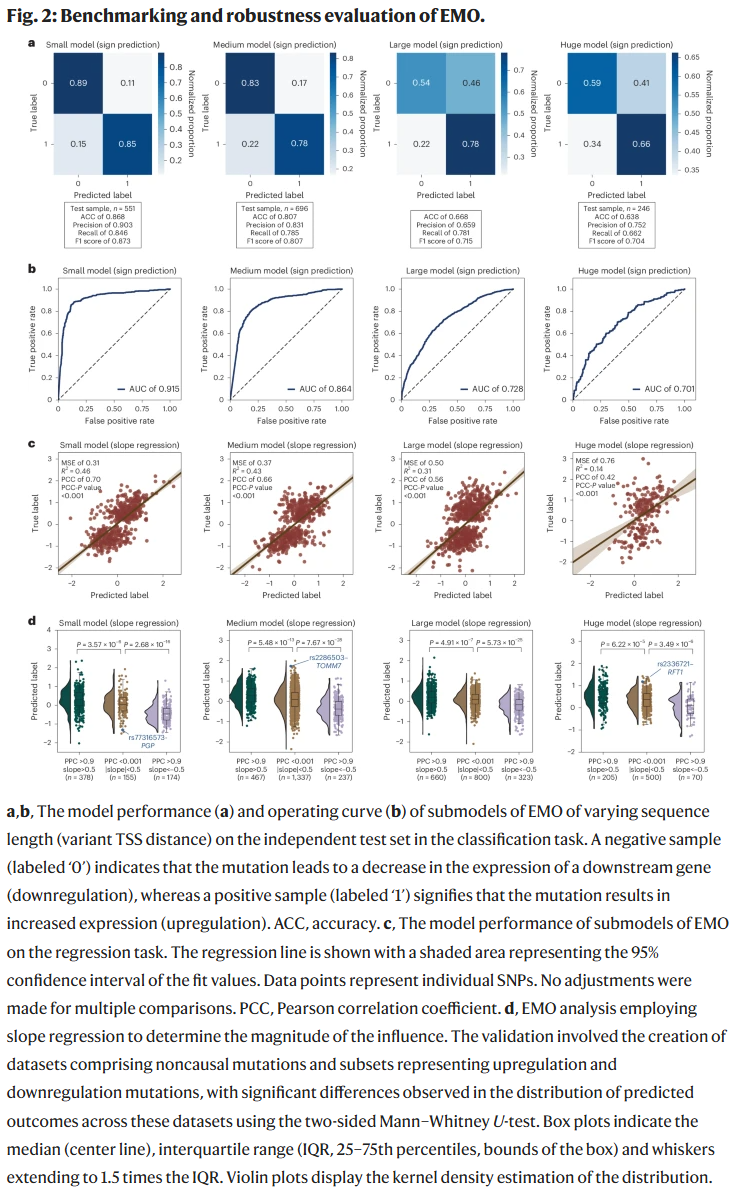
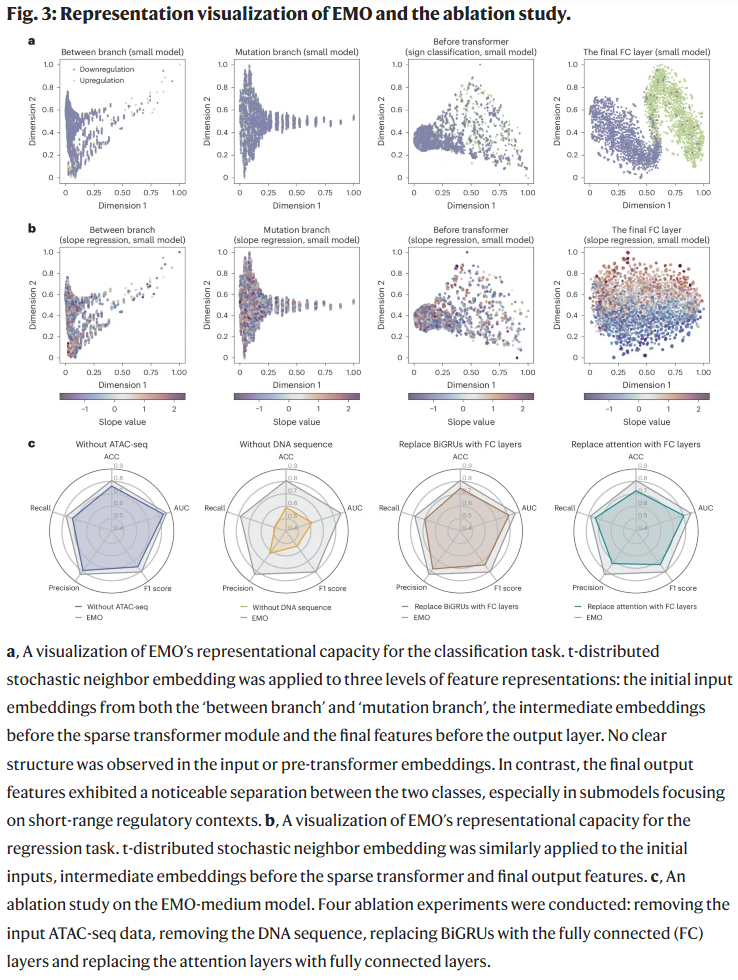
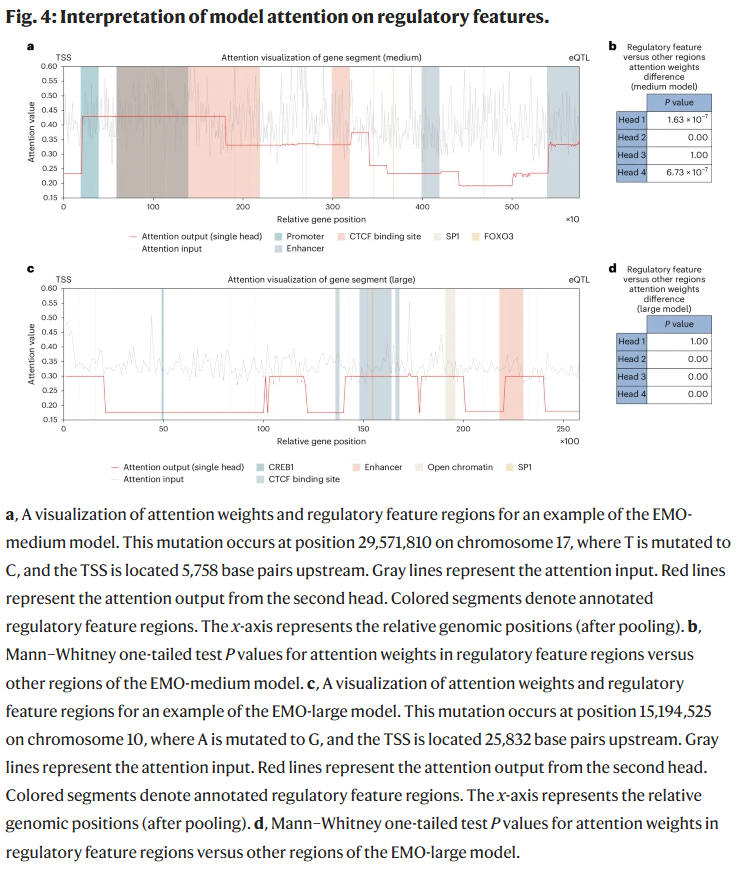
单细胞分辨率下的应用
研究人员将 EMO 应用于单细胞转录组与表观组联合数据,揭示了不同细胞类型间的调控差异。特别是在稀有细胞群体中,EMO 仍能保持较强的预测能力,说明其在复杂组织环境中具有独特优势。
疾病相关变异的功能解析
研究人员利用 EMO 对疾病相关的非编码变异进行解析,发现这些变异可能通过改变染色质状态或转录因子结合模式,直接影响基因表达。结果为复杂疾病的分子机制研究提供了新的线索。
与现有方法的比较
在多个基准测试中,EMO 的预测准确率与稳健性显著优于其他主流方法,尤其在跨组织和单细胞层面展现出更强的泛化能力。
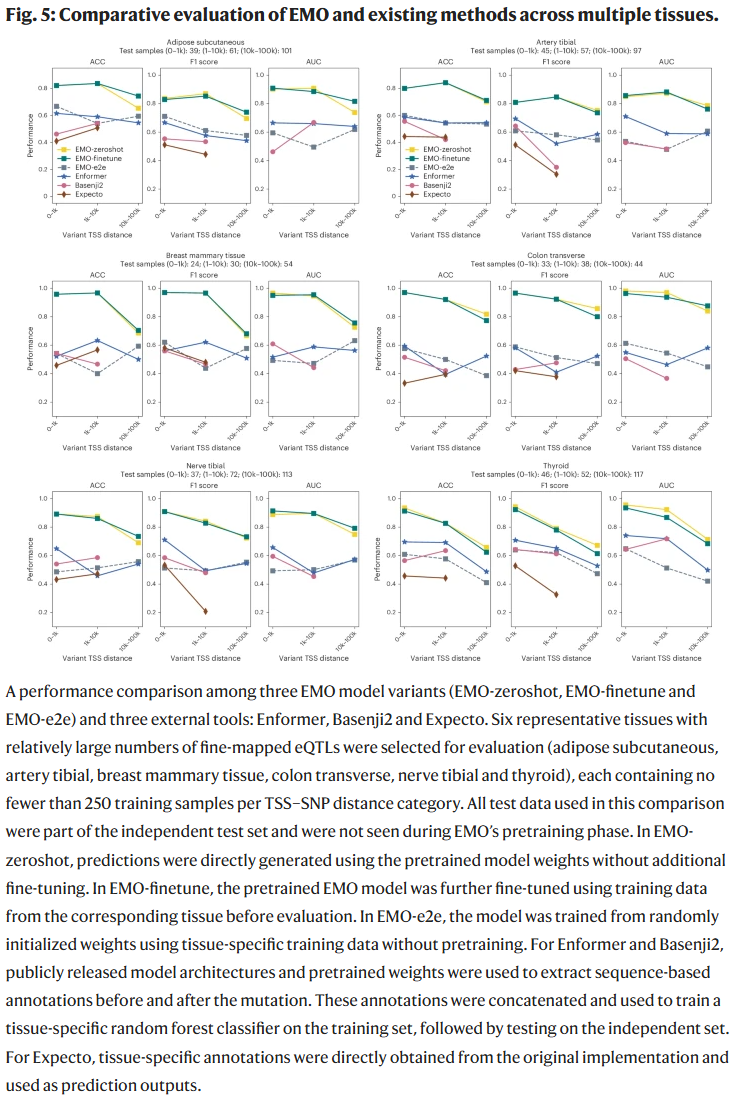
变异在调控网络中的作用模式
研究人员进一步构建了变异在跨组织与单细胞调控网络中的作用图谱,揭示了其如何通过调节增强子–启动子连接影响基因表达。该结果表明,非编码变异能够在不同生物学层级产生连锁效应。
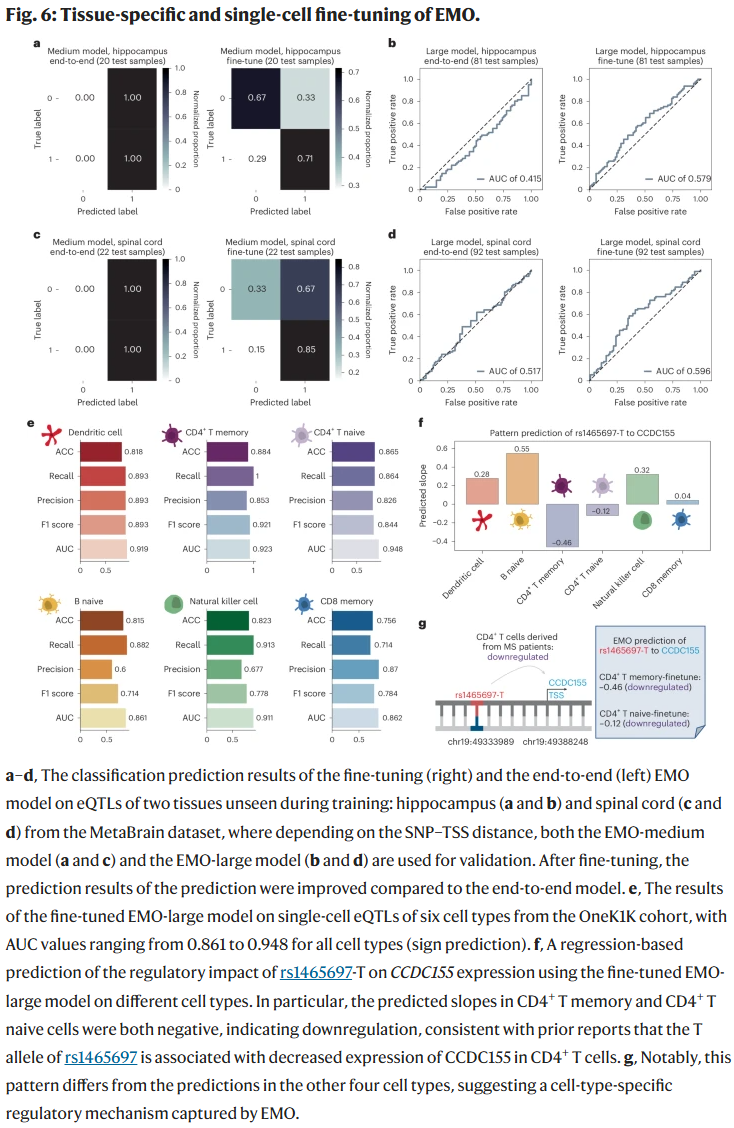
讨论
研究人员提出的 EMO 框架为预测非编码变异的调控作用提供了新的解决方案。通过跨组织与单细胞表观组的整合,并结合三维基因组结构,EMO 实现了更高的预测准确性与解释力。
这一框架在精准医学中具有广阔应用前景:
- 可帮助优先筛选潜在的致病变异;
- 揭示复杂疾病的分子机制;
- 为药物靶点发现与功能基因注释提供支持。
未来的改进方向包括:
- 扩展表观组学数据来源,如甲基化组;
- 优化模型以适应更复杂的细胞环境;
- 在大规模人群数据中验证其预测能力。
整体而言,EMO 为解码非编码变异的功能开辟了新路径,展示了跨尺度整合在基因组学研究中的巨大潜力。
整理 | DrugOne团队
参考资料
Liu, Z., Bao, Y., Gu, A. et al. Predicting the regulatory impacts of noncoding variants on gene expression through epigenomic integration across tissues and single-cell landscapes. Nat Comput Sci (2025).
https://doi.org/10.1038/s43588-025-00878-7
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-09-28,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

