Nat. Biotechnol. | 离体人肺数字孪生实现治疗效果的精准个体化评估
Nat. Biotechnol. | 离体人肺数字孪生实现治疗效果的精准个体化评估

DrugOne
发布于 2026-05-07 16:42:15
发布于 2026-05-07 16:42:15
DRUGONE
数字孪生作为一种新兴技术,旨在整合分子、功能、生理以及临床数据,从而构建生物系统的计算模型。然而,在医学领域,由于缺乏大规模多模态数据,这一概念长期难以真正落地。
研究人员利用离体肺灌注(EVLP)技术,构建了目前规模最大的临床人肺多模态数据集,并据此开发了高保真的人肺数字孪生模型。该模型能够同时刻画超过75项跨尺度指标,涵盖肺功能、生物化学、影像特征以及转录组、代谢组和蛋白组信息。进一步地,通过与真实实验数据的直接对比,研究人员证明该数字孪生系统能够准确评估治疗效果,例如在应用溶栓药物alteplase时,能够精确预测疗效与安全性。这些结果表明,人肺数字孪生为治疗评估提供了一种数据驱动且个体化的新路径。

数字孪生最早源于工程领域,通过构建物理对象的虚拟模型,实现设计优化与性能预测。在医疗领域,这一概念被引入用于疾病预测和个体化医疗,但目前大多数应用仍停留在简化的预测模型层面,缺乏真正跨尺度整合能力。
造成这一局限的核心原因在于数据缺失。构建高保真数字孪生需要同时整合分子、组织和器官层面的信息,而现实中难以在人体内获取如此全面的数据。
离体器官灌注技术为这一问题提供了解决方案。在EVLP系统中,人肺可以在体外维持接近生理状态的功能,同时允许持续采集多模态数据,包括影像、传感器信号以及分子样本。这种环境不仅提供了高度可控的实验条件,也使得构建完整的器官级数字孪生成为可能。
在这一背景下,研究人员提出构建“数字肺”,通过融合物理模型与数据驱动模型,实现对人肺功能的精准建模和预测。
方法
研究人员构建了一种融合机制模型与机器学习的混合数字孪生框架。该框架以EVLP系统采集的多模态数据为基础,包括高频呼吸机数据、影像数据以及多组学信息。
在建模过程中,首先利用生理学方程从呼吸机数据中计算关键力学参数,例如肺顺应性、气道压力等,以建立具有可解释性的物理模型。同时,研究人员引入机器学习模型(如GRU与XGBoost)来捕捉复杂的非线性关系,从而实现对未来肺功能的预测。
此外,系统设计了两种运行模式:静态数字孪生基于初始数据预测长期变化,而动态数字孪生则持续利用实时数据更新模型,实现短期精确预测。这种设计使系统兼具长期预测能力与实时响应能力。
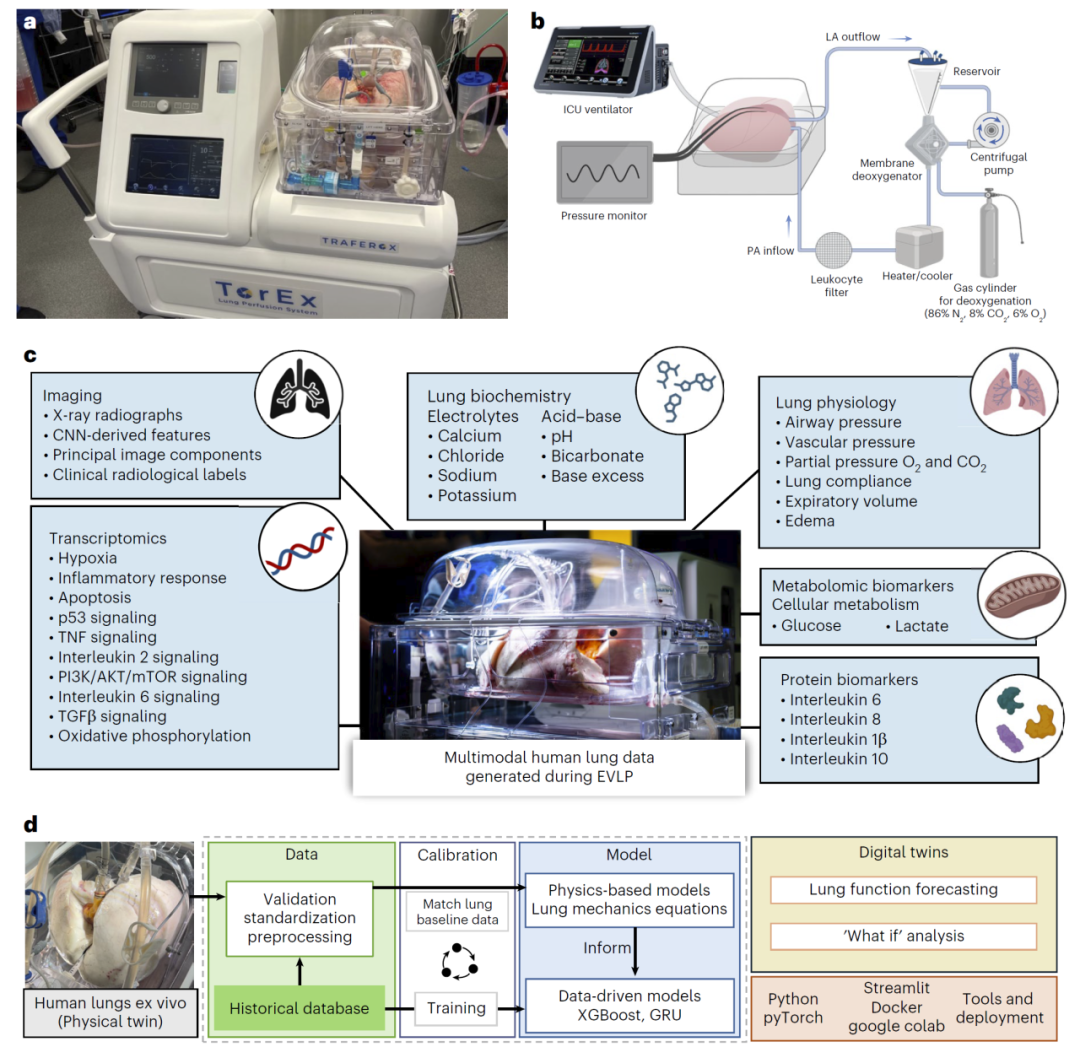
图1:EVLP多模态数据与数字肺构建框架。
结果
人肺数字孪生模型构建与数据特征
研究人员基于951例离体人肺数据构建模型,这些肺来源于无肺部疾病的供体,具有代表性的人群特征。EVLP过程中采集的数据覆盖多个尺度,包括生理参数、生化指标以及多组学信息。
这些数据构成了数字孪生模型的基础,使其能够全面刻画肺功能及其动态变化。
肺功能预测能力
数字孪生模型能够准确预测多项关键肺功能指标,包括气道压力、气体交换能力以及肺顺应性等。
根据论文第3页表1,模型预测误差通常在2–11%范围内。例如,对氧气和二氧化碳分压的预测误差仅约4–13%,而对肺水肿的预测误差约为30 ml,表现出较高精度。
动态数字孪生在大多数指标上优于静态模型,说明实时数据更新对于提高预测性能具有重要作用。
生化与多组学预测能力
除了生理参数,模型还能够预测电解质、酸碱平衡以及代谢指标。例如,对葡萄糖和乳酸浓度的预测误差较低,表明模型能够捕捉细胞代谢状态变化。
在转录组层面,模型能够准确预测多个疾病相关通路的变化趋势,包括缺氧反应、p53信号通路以及炎症反应等,预测误差仅约1–3%。
在蛋白组层面,模型同样能够预测炎症相关蛋白水平变化,尽管由于浓度范围差异较大,误差波动较高,但整体趋势仍然一致。
影像与多模态整合能力
研究人员进一步验证了模型在影像层面的表现。通过卷积神经网络提取影像主成分,模型能够准确预测后续时间点的影像特征,并与临床影像诊断结果(如肺实变、感染)高度相关。
这一结果表明,数字孪生能够在统一框架中整合影像、生理和分子信息,实现跨尺度建模。
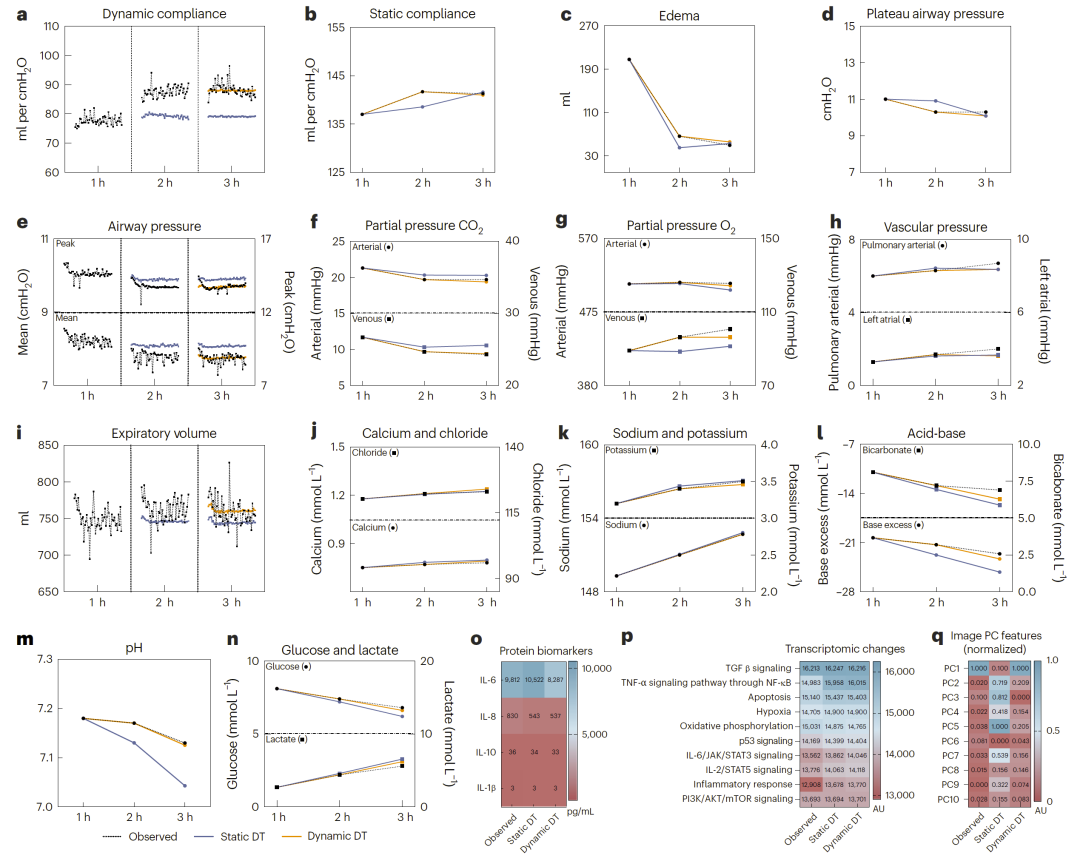
图2:多模态预测示例(生理、生化、组学与影像)。
模型精度与鲁棒性验证
研究人员通过多种方式验证模型性能,包括统计检验、模拟数据以及独立测试集评估。
结果表明,模型预测误差不存在系统性偏差,并且在独立数据集上保持稳定性能。此外,与传统小样本对照组相比,数字孪生模型的误差显著更低,说明其在统计效率和精度上具有优势。
治疗效果评估能力
研究人员进一步验证了数字孪生在治疗评估中的应用。以溶栓药物alteplase为例,模型能够模拟“未治疗”情况下的肺功能变化,从而作为个体化对照。
结果显示,在适合移植的肺中,治疗后肺动脉压力显著降低,而数字孪生预测的未治疗结果则未表现出该变化,从而清晰揭示药物疗效。
相比传统群体对照分析,数字孪生方法能够在更小样本量下检测到显著差异。例如,仅6例样本即可观察到显著效果,而传统方法需要约3倍样本量。
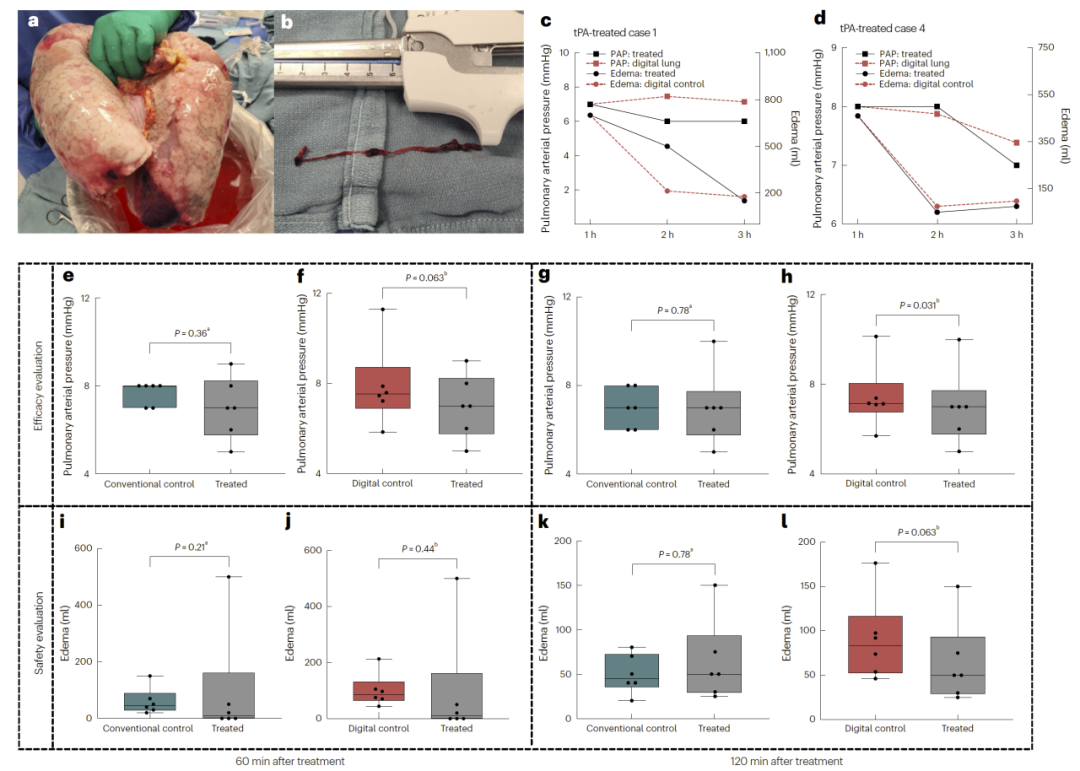
图3:基于数字孪生的个体化治疗评估。
讨论
本研究提出了一种基于离体器官的数字孪生新范式,实现了对人肺多尺度生物过程的高精度建模。通过融合物理模型与机器学习,研究人员成功构建了一个既具有可解释性又具备强预测能力的系统。
数字孪生的一个核心优势在于其能够作为“个体化对照”,通过模拟未治疗状态,实现更精准的因果推断。这种方法不仅提高了统计效率,还降低了实验成本,对于药物研发具有重要意义。
此外,该框架具有良好的扩展性,可以应用于其他器官或疾病模型,并结合更多传感器和数据类型进一步提升性能。
不过,研究人员也指出了一些局限,例如部分数据类型样本量较小、当前模型主要关注短时间预测以及缺乏全身水平的药物分布建模。
总体而言,该研究展示了数字孪生在精准医疗中的巨大潜力,为未来实现“个体级虚拟人体模型”奠定了重要基础,并有望深刻改变治疗评估与药物开发的方式。
整理 | DrugOne团队
参考资料
Zhou, X., Wang, B., Wei, Y. et al. Digital twins of ex vivo human lungs enable accurate and personalized evaluation of therapeutic efficacy. Nat Biotechnol (2026).
https://doi.org/10.1038/s41587-026-03121-4
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-05-05,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

