Nat. Commun. | 融合免疫原性筛选与克隆性新抗原图谱的免疫治疗响应精准预测框架
Nat. Commun. | 融合免疫原性筛选与克隆性新抗原图谱的免疫治疗响应精准预测框架

DrugAI
发布于 2026-01-27 15:17:53
发布于 2026-01-27 15:17:53
DRUGONE
尽管癌症免疫治疗显著改变了肿瘤治疗格局,但患者响应率仍然有限,亟需更精准的疗效预测方法。新抗原是抗肿瘤免疫反应的核心驱动因素,但传统指标如肿瘤突变负荷(TMB)忽略了新抗原的免疫原性质量及肿瘤异质性。
研究人员提出 NeoPrecis 计算框架,通过整合新抗原免疫原性评估与肿瘤克隆结构信息,构建“克隆性感知的新抗原景观”,以提升免疫治疗响应预测能力。该框架同时考虑 MHC-I 与 MHC-II 通路,并引入可解释的 T 细胞识别模型,揭示 MHC 分子不仅负责抗原呈递,还深度影响 TCR 识别过程。在黑色素瘤与非小细胞肺癌等队列中,NeoPrecis 显著优于现有指标,特别是在高度异质性肿瘤中表现突出,为精准免疫治疗提供了系统性新策略。

个体化癌症疫苗与免疫检查点抑制剂已成为两大核心免疫治疗方式,均依赖肿瘤特异性新抗原激活免疫系统。然而,无论是疫苗还是免疫治疗,临床响应率普遍不理想。
目前广泛应用的预测指标,如 TMB 和新抗原负荷,仅关注数量层面,未能有效反映:
- 新抗原是否真正具备免疫原性;
- 是否能被 T 细胞识别;
- 是否存在于肿瘤的主要克隆中。
同时,传统新抗原研究主要聚焦 MHC-I 通路,而越来越多证据显示 MHC-II 介导的 CD4⁺ T 细胞反应在抗肿瘤免疫中同样关键。
此外,肿瘤异质性使大量新抗原仅存在于亚克隆中,降低免疫系统对其整体清除能力。
因此,研究人员提出需要一个同时融合免疫原性质量、MHC呈递、T细胞识别与肿瘤克隆结构的综合新抗原评估体系。
方法
研究人员开发 NeoPrecis 框架,包含两个核心模块:
- NeoPrecis-Immuno:基于深度学习的新抗原免疫原性预测模型,融合 MHC 结合模式与 TCR 识别特征,同时覆盖 MHC-I 与 MHC-II 通路。
- 克隆性感知新抗原景观模型:结合肿瘤克隆结构信息,将免疫原性新抗原映射至不同肿瘤亚克隆,构建反映肿瘤异质性的免疫景观。
该框架在多个真实免疫治疗队列中进行系统评估,并与 TMB、新抗原负荷及其他克隆模型进行对比。
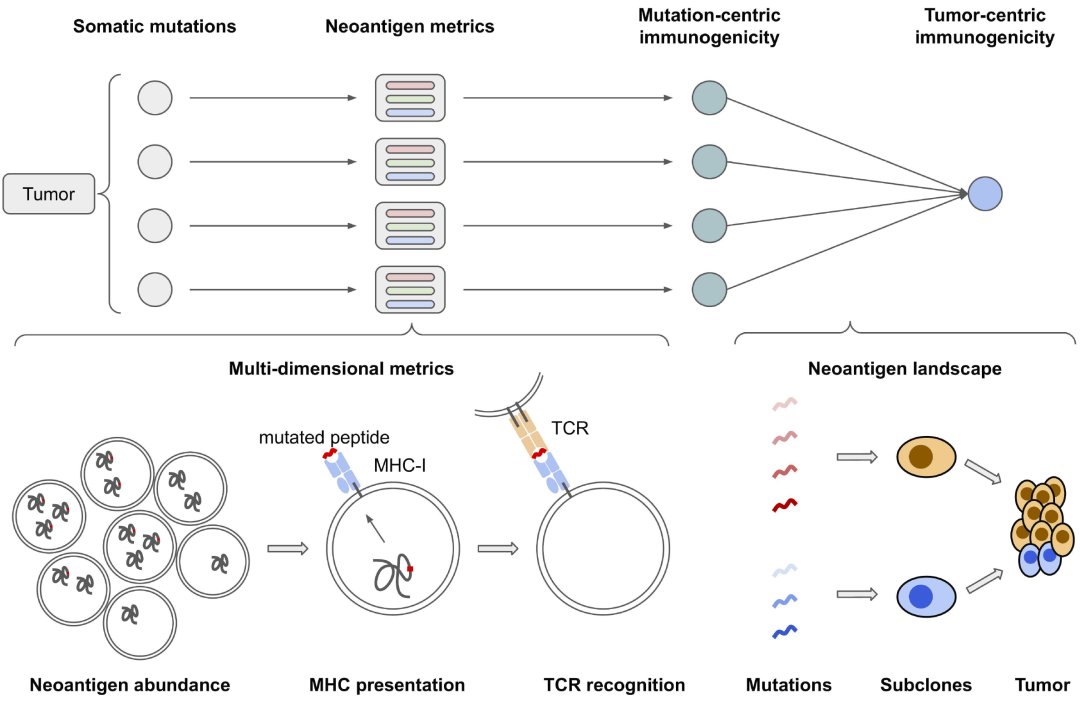
图1|NeoPrecis 肿瘤新抗原评估框架。
结果
构建可解释的T细胞识别免疫原性模型
研究人员提出 NeoPrecis-Immuno 模型,将:
- 新抗原与野生型肽段差异;
- MHC 结合模式;
- TCR 交叉反应特征。
统一嵌入深度学习框架中。该模型在多项内部与外部验证数据集上,与现有免疫原性预测方法相比表现相当或更优,并具备良好的跨 MHC 等位基因泛化能力。
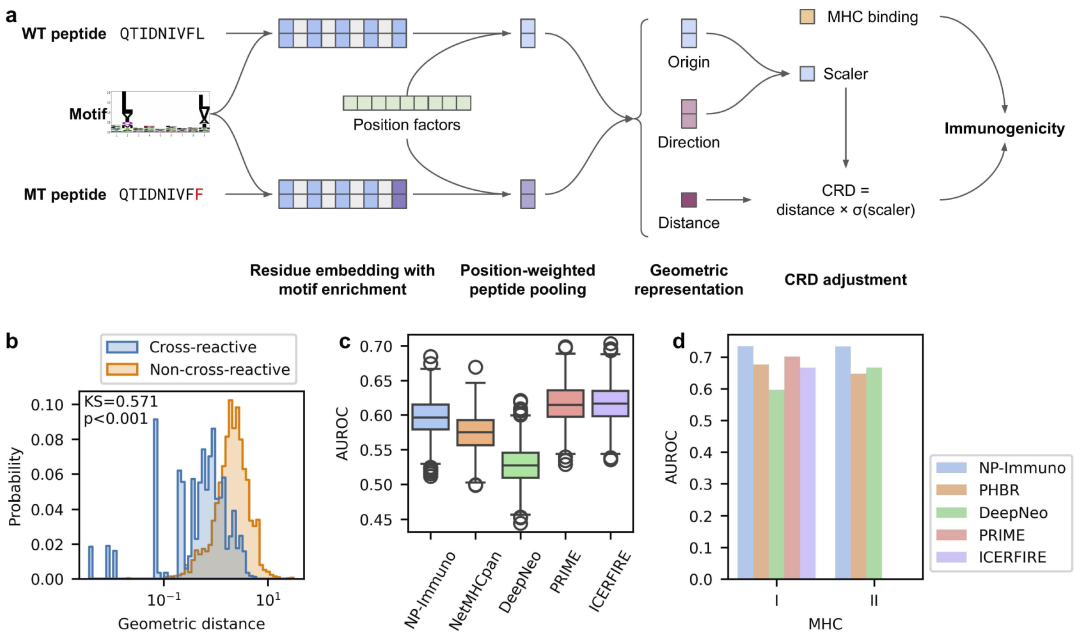
图2|T 细胞识别模型 NeoPrecis(NP)-Immuno 的构建与验证
MHC分子不仅呈递抗原,还影响TCR识别
模型解释性分析发现:
- MHC 结合位点对 TCR 识别贡献显著;
- 不同 HLA 等位基因对新抗原免疫原性具有系统性影响。
研究人员提出“有益 HLA 等位基因”概念,其组合与患者免疫治疗疗效显著相关。
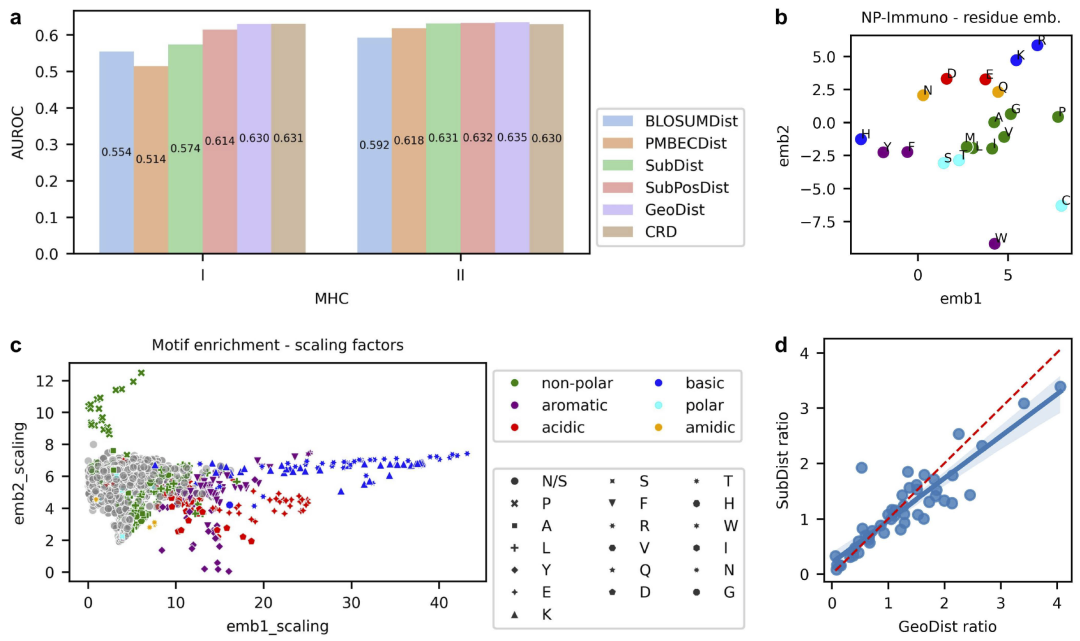
图3|NeoPrecis-Immuno 模型的可解释性分析。
多维度整合显著提升新抗原免疫原性预测
将以下三类特征整合:
- 新抗原丰度(突变频率、表达水平);
- MHC 呈递能力;
- TCR 识别概率。
形成综合免疫原性模型后,预测效果显著优于单一指标。其中,NeoPrecis-Immuno 本身已隐含 MHC 呈递信息,使其成为核心驱动因子。
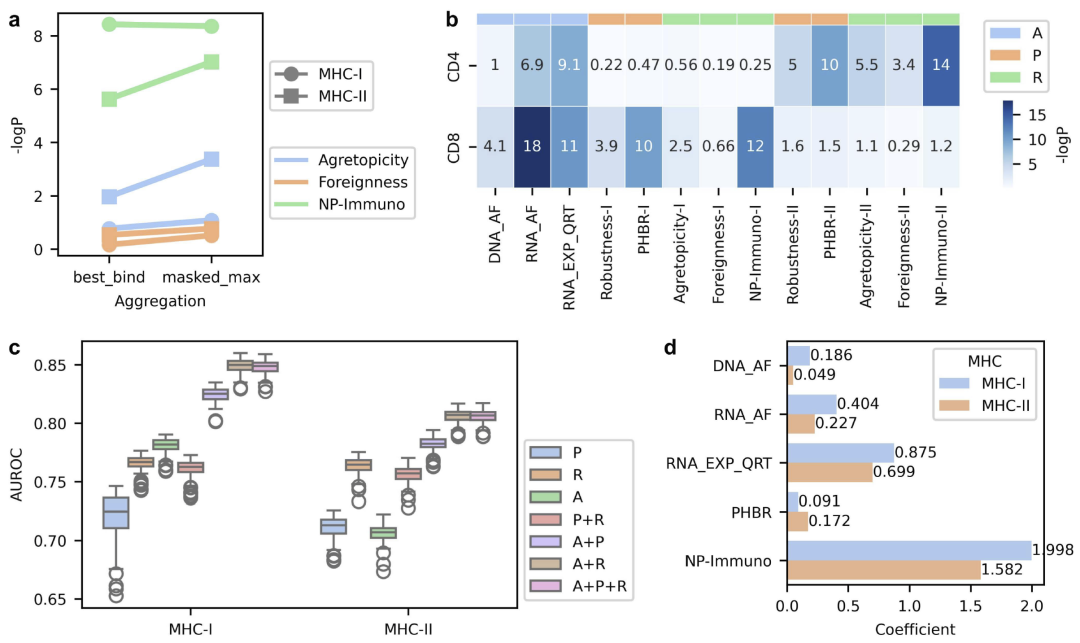
图4|多维度免疫原性指标的整合预测框架。
NeoPrecis 优于传统TMB与新抗原负荷指标
在黑色素瘤和非小细胞肺癌免疫治疗队列中:
- NeoPrecis 相关指标在区分响应者与非响应者方面显著优于 TMB;
- 预测的免疫原性新抗原总量与患者生存结局显著相关。
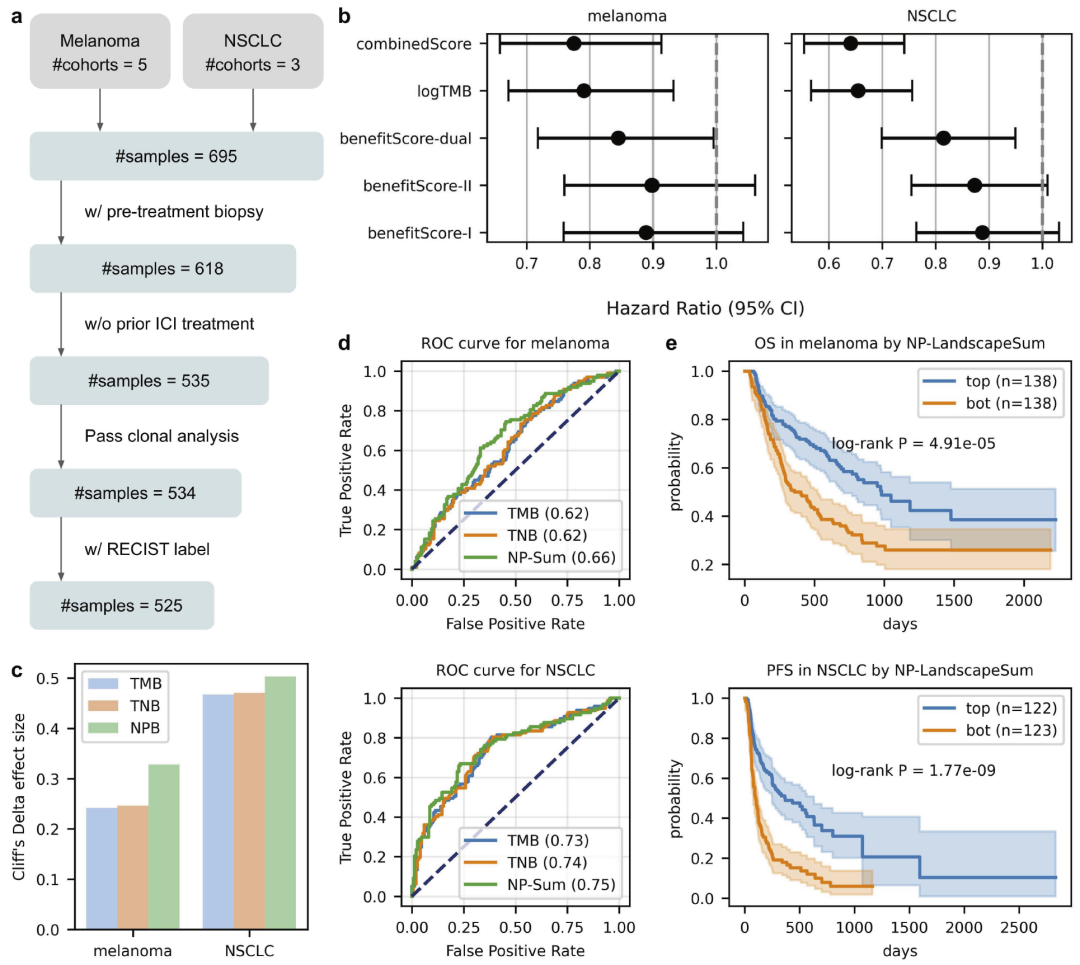
图5|基于新抗原景观模型的免疫检查点抑制剂(ICI)响应预测。
构建克隆性感知的新抗原景观
研究人员引入肿瘤克隆结构分析,将新抗原免疫原性映射到不同亚克隆中,形成:
- 不同亚克隆的免疫原性强度分布;
- 整体肿瘤免疫景观结构。
该方法不仅考虑数量,还关注免疫原性在肿瘤进化过程中的空间分布。
在高度异质性肿瘤中预测优势最明显
结果显示:
- 在肿瘤异质性高的 NSCLC 中,克隆性感知 NeoPrecis 模型显著优于所有对比方法;
- 在较均一肿瘤中,单纯免疫原性累积指标仍有效。
进一步分析发现:
- 同质肿瘤可能经历更强免疫编辑,免疫原性克隆新抗原被选择性清除。
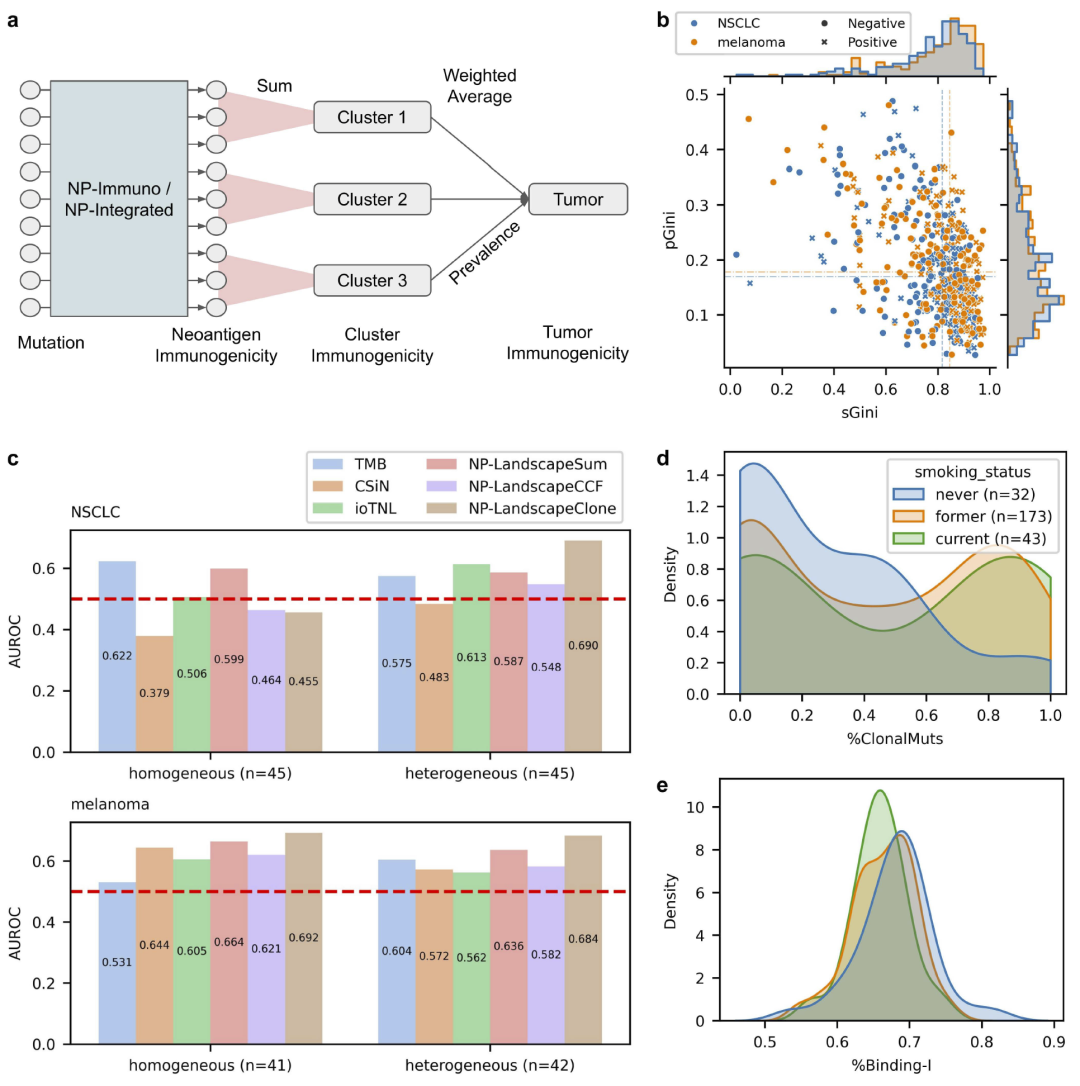
图6|融合肿瘤亚克隆结构提升免疫治疗响应预测能力。
讨论
本研究提出 NeoPrecis 框架,实现了新抗原评估从“数量导向”向“质量 + 结构导向”的转变。
核心创新包括:
将 MHC 结合模式引入 TCR 识别建模;
- 同时整合 MHC-I 与 MHC-II 通路;
- 构建克隆性感知的新抗原免疫景观。
研究表明,真正决定免疫治疗疗效的并非新抗原数量,而是免疫原性高的新抗原是否存在于关键肿瘤克隆中。
在临床层面,NeoPrecis 有望:
- 提高免疫治疗患者筛选精度;
- 优化个体化癌症疫苗设计;
- 揭示肿瘤免疫逃逸与免疫编辑机制。
研究人员也指出当前局限,如尚未纳入插入缺失突变、新抗原侧翼序列影响及肿瘤微环境因素,未来可进一步扩展模型以提升预测能力。
整理 | DrugOne团队
参考资料
Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun (2026).
https://doi.org/10.1038/s41467-026-68651-6
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-01-25,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

