Nat. Commun. | 郭天南/王宇/刘志艳团队发表中国人群甲状腺髓样癌多中心多组学研究结果,构建预后预测新模型,AUC达0.87!
Nat. Commun. | 郭天南/王宇/刘志艳团队发表中国人群甲状腺髓样癌多中心多组学研究结果,构建预后预测新模型,AUC达0.87!

DrugOne
发布于 2026-01-26 16:42:34
发布于 2026-01-26 16:42:34
在众多癌症中,甲状腺癌因进展缓慢、恶性程度低、治愈率高的特点被称为“懒癌”,但甲状腺髓样癌(MTC)却打破了这一认知。作为起源于滤泡旁C细胞的罕见神经内分泌肿瘤,MTC发病率仅占甲状腺癌的2%,却导致了8%的甲状腺癌相关死亡。该癌症具有侵袭性强、转移潜能高的特点,且对放射性碘治疗固有耐药,手术治疗后复发率也较高,严重影响了患者的生存和生活质量。
目前MTC术后预后评估主要依赖TNM分期系统,但该系统未纳入年龄、性别、降钙素水平等关键预后因素;国际MTC分级系统(IMTCGS)虽整合了增殖活性和肿瘤坏死指标可实现高低分级,但其在亚洲人群中的有效性待验证。基因组和转录组研究揭示了RET突变对MTC的核心驱动作用,但仍部分散发性病例驱动突变不明。近年来,蛋白质组学与泛素化研究为MTC带来新突破口,但受限于样本量等,该领域相关大规模研究仍较少。
近日,西湖大学郭天南、孙耀庭团队,与复旦大学王宇、上海市第六人民医院刘志艳团队合作,对来自10个中国临床中心的452名MTC患者的482份样本进行整合多组学分析,鉴定了10,092种蛋白质,并在87.0%的患者中检测到突变。研究团队明确IMTCGS分级、并发乳头状甲状腺癌(PTC)、淋巴结转移(LNM)是临床复发高危因素,RET M918T和RET S891A突变分别与散发性和遗传性MTC的高复发风险相关;并通过泛素组学发现E3泛素连接酶CUL4B和TRIM32下调与肿瘤结构性复发相关。此外,研究团队定义了3种具有不同预后的MTC分子亚型,并整合临床、基因组和蛋白质组特征构建了一个精准的MTC预后预测模型。总之,这项研究为MTC的复发风险分层、个体化管理及潜在治疗靶点发现提供了宝贵的多组学数据资源和实用工具。

该研究共纳入了452名MTC患者,分为发现数据集(347人,377份样本)和独立测试集(105人)。研究团队收集了12项临床指标,对28个基因进行靶向测序,并利用基于质谱的蛋白质组学和泛素化组学技术进行深度分析。患者基线特征显示,平均年龄约50岁,男性占比45.8%,遗传性MTC占17%。
在发现数据集的随访期内,20.7%的MTC患者出现结构性复发(SR),3.5%的患者死于MTC相关原因;从初次手术到SR或疾病特异性死亡(DSM)的平均时间分别为52.5个月和78.6个月。与非复发(NR)病例相比,SR、DSM患者在临床病理特征上更具侵袭性,如肿瘤体积更大、更常出现甲状腺外侵犯(ETE)和LNM等。
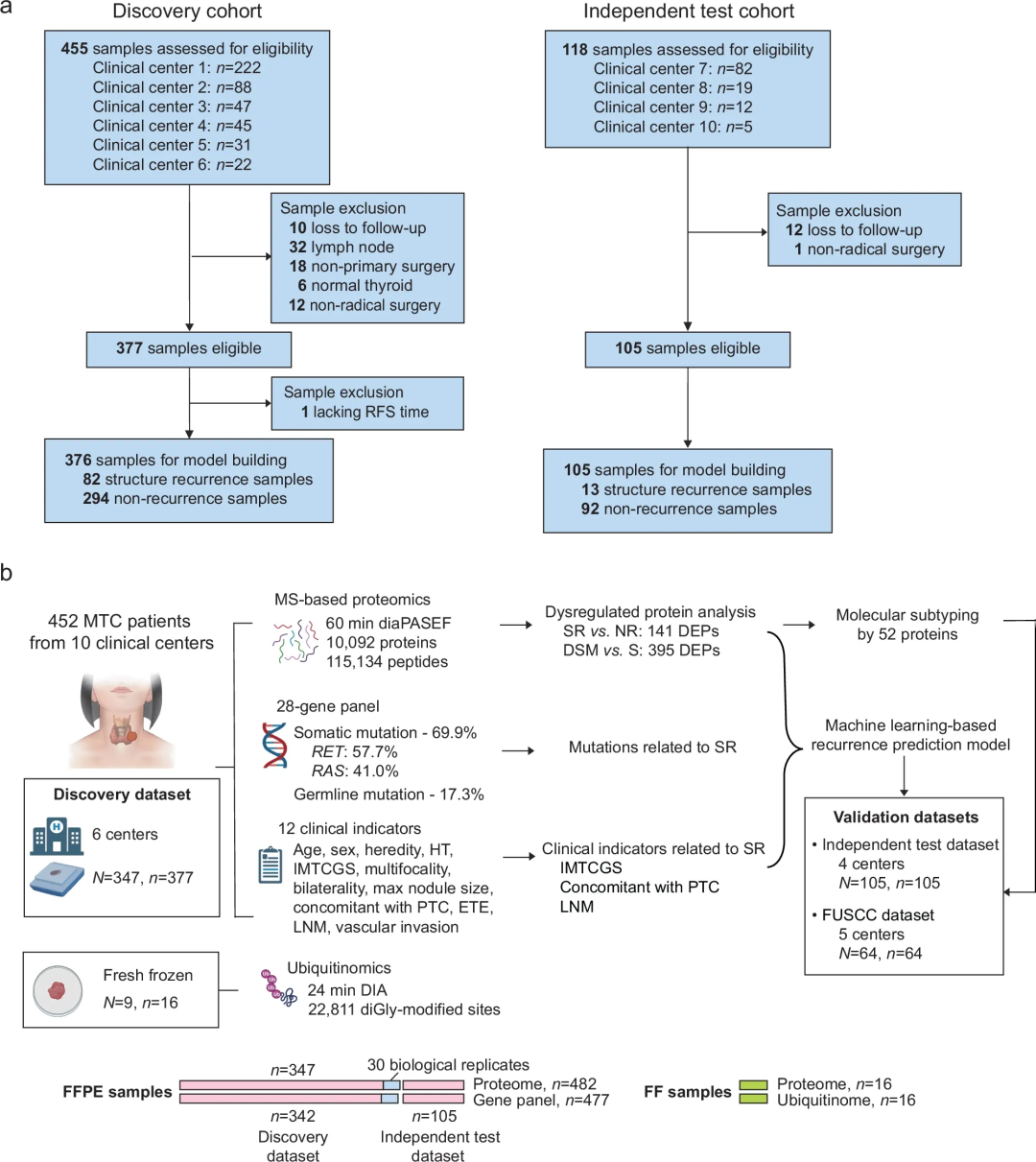
图1.研究概述
RET和RAS是MTC中最常突变的两个基因,研究团队探究了按RET和RAS突变状态分层的临床特征。与RET/RAS野生型病例相比,RET胚系和体细胞突变均与更高的ETE和LNM发生率相关,且体细胞突变患者复发率显著高于野生型。若不区分具体突变位点,RET/RAS突变状态与疾病特异性死亡无显著关联。进一步生存分析显示,散发性MTC中RET M918T突变者复发风险更高;遗传性MTC中,RET S891A突变是高复发因素,而RET C634突变则与低复发风险相关。
研究团队还比较了中国与西方MTC患者队列的基因突变位点频率。结果显示,中国MTC患者具有独特的突变模式:散发性病例中HRAS突变频率更高,遗传性病例中RET C634突变更常见,而西方队列常见的RET C609Y突变在中国队列罕见,且存在特有RET S891A突变。
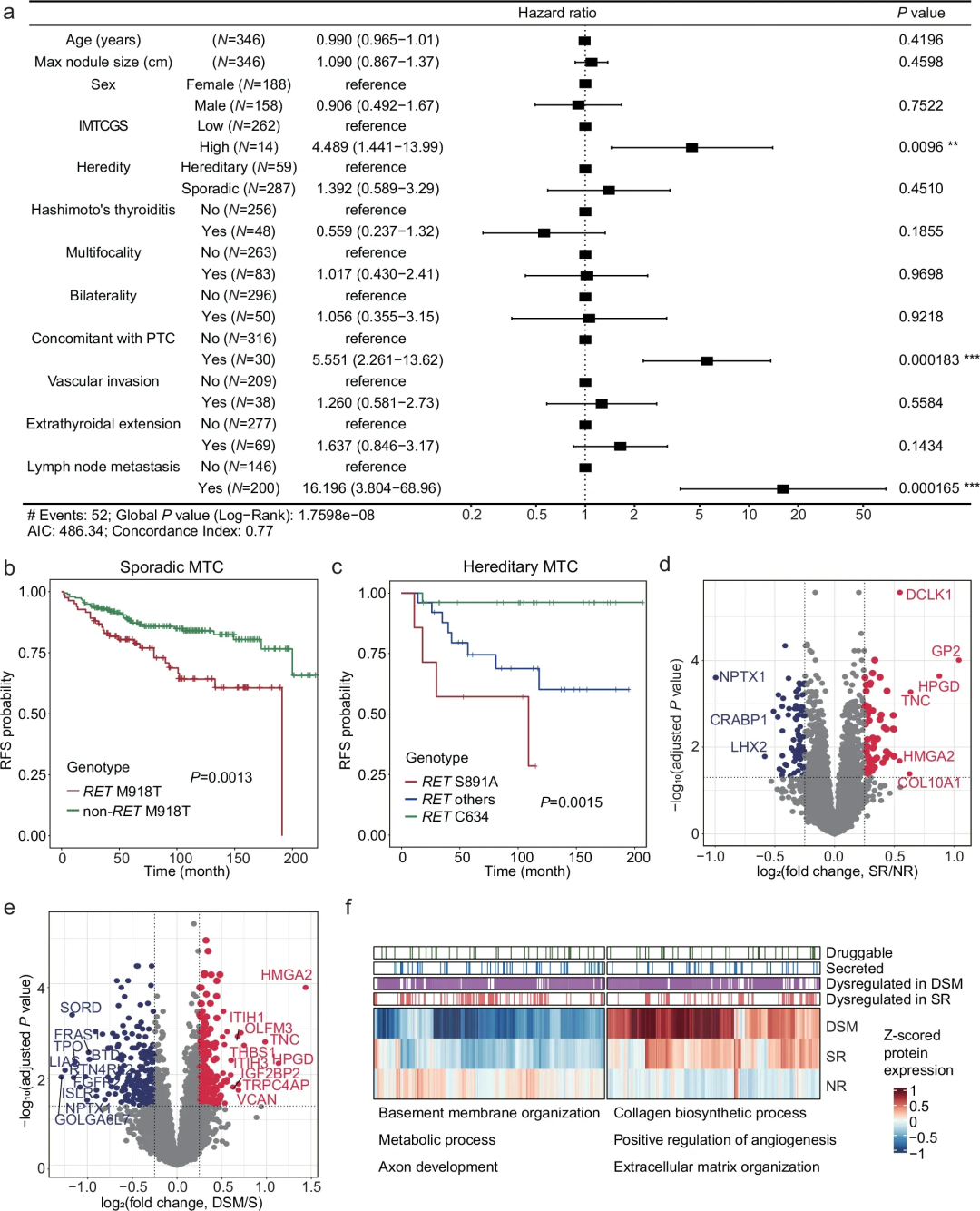
图2. 不同预后患者之间的临床、基因组和蛋白质组分析
为识别与MTC疾病预后相关的风险因素,研究团队对12项临床病理特征构建了分别单、多变量Cox比例风险模型,确定IMTCGS分级、并发PTC以及LNM是MTC结构性复发的独立临床风险因素。
研究团队采用特定质谱技术对发现集样本进行蛋白质组定量,鉴定出10,092种蛋白,将其筛选后进行蛋白质组学分析。结果显示,共识别出141种复发相关差异表达蛋白和395种死亡相关差异表达蛋白;在NR-SR-DSM疾病进展过程中,上调蛋白的表达呈现递增趋势,而下调蛋白则递减;RET、RAS突变患者中,NF1和SPRY4蛋白呈现相反的表达模式。富集通路分析显示,与不良预后相关的蛋白主要富集于细胞外基质重塑、胶原合成和血管生成等通路,其表达水平在疾病进展中呈现连续变化趋势。
接下来,研究团队对MTC进行了泛素组学分析,首次描绘了MTC的泛素化修饰全景。结果显示,共鉴定出22,811个双甘氨酸修饰位点和6,505个修饰蛋白;检测到MTC组织特有的K33连接泛素化,SR组显著降低的K11泛素化。通过比较复发与非复发样本,研究团队筛选出少数关键的差异泛素化位点,其相关通路涉及细胞运输,与肿瘤侵袭性相关。特别地,研究团队发现并验证了E3连接酶CUL4B和TRIM32在复发患者中表达持续下调,表明其可能参与 MTC复发机制。
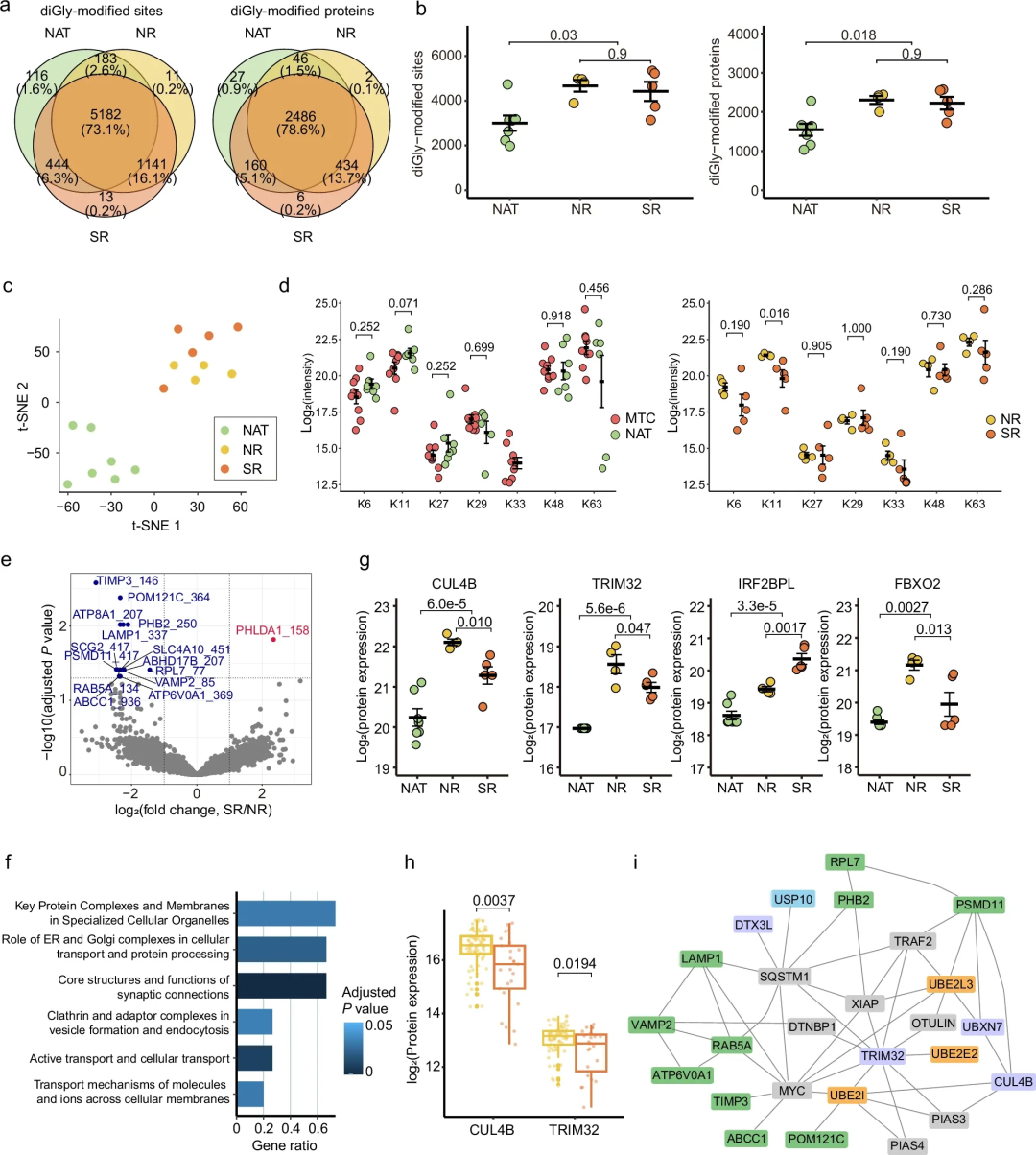
图3. MTC泛素化图谱
研究团队对上述差异蛋白进行无监督聚类分析,筛选52种关键蛋白并基于其将患者分为 M1、M2、M3三种分子亚型,各亚型临床病理、突变特征和蛋白谱差异显著。M1亚型预后中等,富集代谢过程相关蛋白且免疫浸润评分最高;M2亚型预后最差,具有更高的ETE和LNM发生率,RET M918T突变比例较高,上皮-间质转化(EMT)通路活性升高、免疫评分最低,临床病理特征更具侵袭性;M3亚型预后最佳,神经内分泌标志物高表达和突触信号通路增强,疾病特异性死亡率为零。
该分型在发现数据集、独立测试集和外部队列数据集中均得到验证,证明了其在不同预后分层中的稳健性。
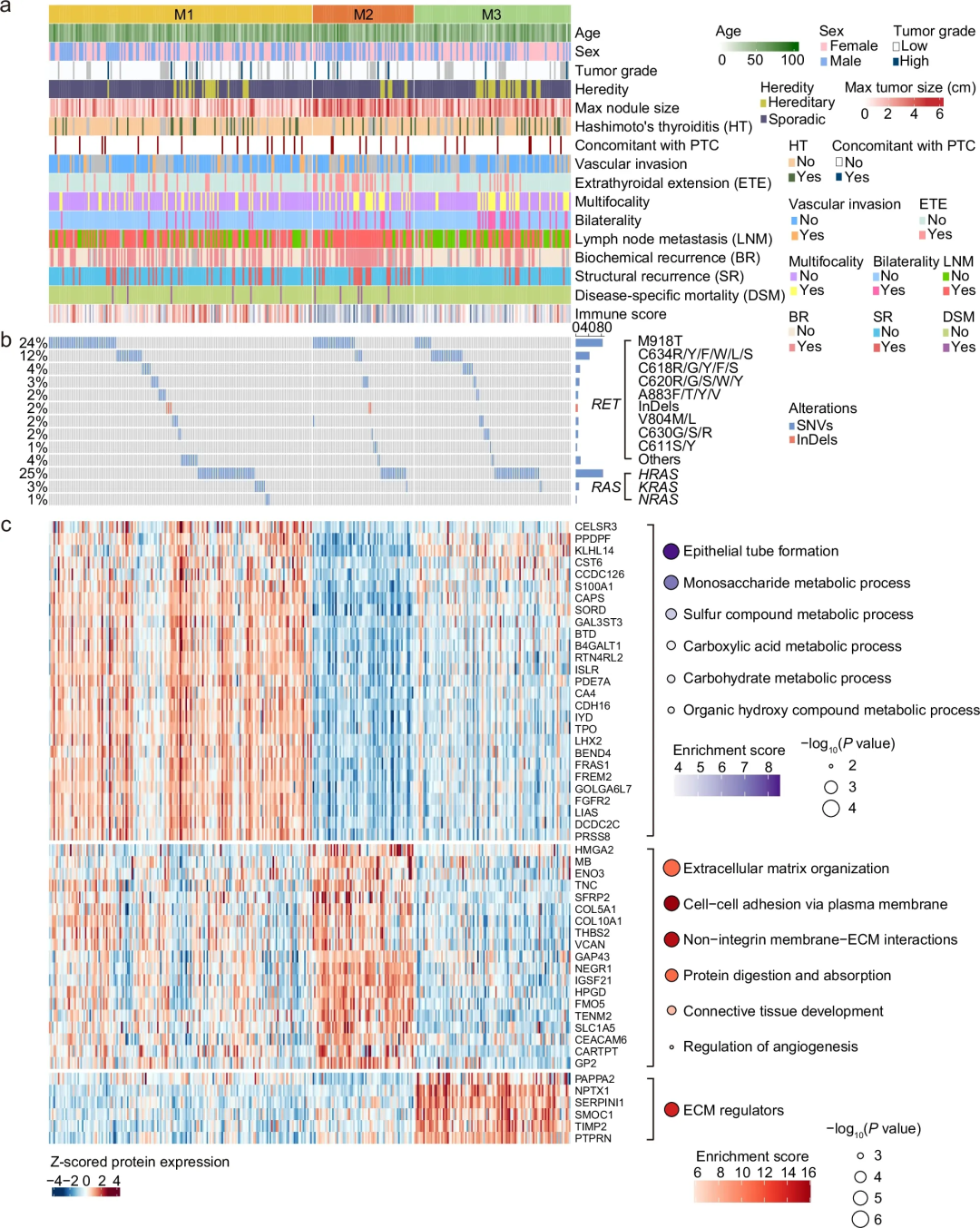
图4. MTC分子亚型
最后,研究团队整合了临床特征、基因突变和蛋白质组数据,开发了多个随机森林模型以预测MTC患者术后结构性复发风险。结果显示,在独立测试集和公开数据集中,整合模型(包含2项临床特征和18种蛋白质)和蛋白质模型的AUC分别为0.87和0.85、0.77和0.78,性能更优、稳健性更强;但整合模型的特征数量比蛋白质模型少31%,因此在性能相当的情况下,整合模型更具优势。
基于整合模型,患者可被有效划分为高风险组和低风险组,两组间的无复发生存期存在显著差异。此外,该模型的18种蛋白含多种甲状腺及癌症相关蛋白,部分富集于醚脂质代谢等通路,且受CDH1、CDKN1A等关键分子调控,这些分子表达与MTC侵袭转移相关。
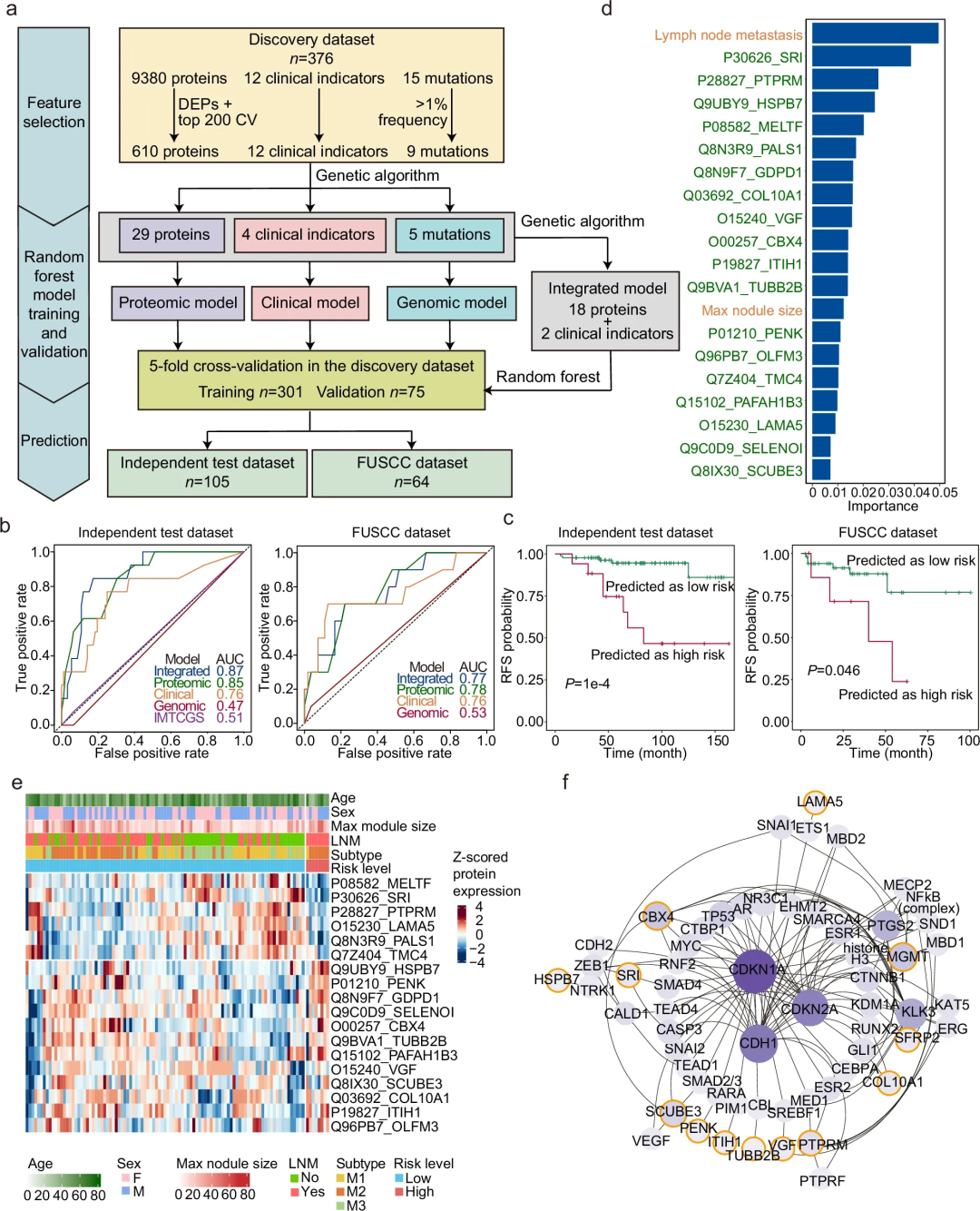
图5. 预后模型的开发与验证
综上所述,该研究构建了国内首个大规模MTC多中心多组学数据集,揭示了中国患者独特的分子特征,填补了亚洲人群MTC预后研究的空白。研究团队构建的蛋白质组分子分型框架和机器学习预后预测模型,不仅显著提升了复发风险预测的准确性,超越了现有临床分级体系,更为推动MTC的精准医疗实践迈出了关键一步。
参考文献:
Zhou, Y., Wang, Y., Shi, X. et al. Multi-center multi-omics integration predicts individualized prognosis in medullary thyroid carcinoma. Nat Commun 17, 432 (2026).
https://doi.org/10.1038/s41467-025-67533-7
·END·
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-01-18,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

