字节打造SeedFold:让生物分子复合物结构预测 又快又准 !
字节打造SeedFold:让生物分子复合物结构预测 又快又准 !

DrugIntel
发布于 2026-01-16 16:40:04
发布于 2026-01-16 16:40:04

在结构生物学与药物研发的交叉领域,生物分子结构预测的精度与效率直接决定了基础研究的推进速度和产业转化的落地周期。自AlphaFold2实现蛋白质单体结构的实验级预测以来,领域内的研究焦点逐渐转向更复杂的生物分子相互作用(如蛋白-配体、蛋白-核酸结合)及模型的规模化扩展。字节跳动Seed团队于2025年12月发布的SeedFold模型,通过创新性的模型缩放策略、高效注意力机制设计及大规模蒸馏数据集构建,在FoldBench基准测试中多项指标超越AlphaFold3,为生物分子基础模型的发展提供了全新范式。本文将从技术原理、核心创新、性能验证及领域影响四个维度,深度解析这一研究。
一、领域痛点与研究背景
生物分子结构预测的核心价值在于揭示分子功能的结构基础,为药物靶点筛选、抗体设计、酶工程等应用提供支撑。尽管AlphaFold3实现了蛋白质、DNA、RNA及配体的统一建模,但现有模型仍面临三大核心瓶颈:
1. 模型容量的瓶颈约束
大多数折叠模型的缩放策略多聚焦于增加Pairformer层数(深度缩放),但AlphaFold的循环机制(训练阶段3次、推理阶段9次)已形成等效深层架构,进一步增加物理层数的边际收益递减。研究发现,成对表示的隐藏维度(AlphaFold系列为128)才是限制模型特征表达能力的关键瓶颈,无法充分编码复杂的分子间相互作用。
2. 计算复杂度的指数级增长
AlphaFold3中Pairformer的三角注意力机制计算复杂度随分子长度呈立方增长(O(n³d)),导致长序列分子(如长链蛋白质、复杂复合物)的预测面临严重的内存与时间开销,难以满足大规模应用需求。
3. 训练数据的稀缺与泛化性不足
实验测定的生物分子结构(如PDB数据库)远无法满足深度学习模型的训练需求。AlphaFold3用通用Transformer替代了AlphaFold2的不变置换注意力(IPA)模块,虽提升了建模灵活性,但丧失了旋转和平移不变性等归纳偏置,在数据不足时泛化能力显著下降。
SeedFold针对上述痛点,从模型、架构、数据三个维度构建规模化解决方案,实现了预测精度与计算效率的双重突破。
二、核心技术创新:三位一体的规模化策略
1. 模型缩放:宽度优先的容量扩展范式
SeedFold团队通过系统性实验验证了三种模型缩放路径的有效性,最终确立了以Pairformer宽度缩放为核心的扩展策略:
(1)缩放路径对比
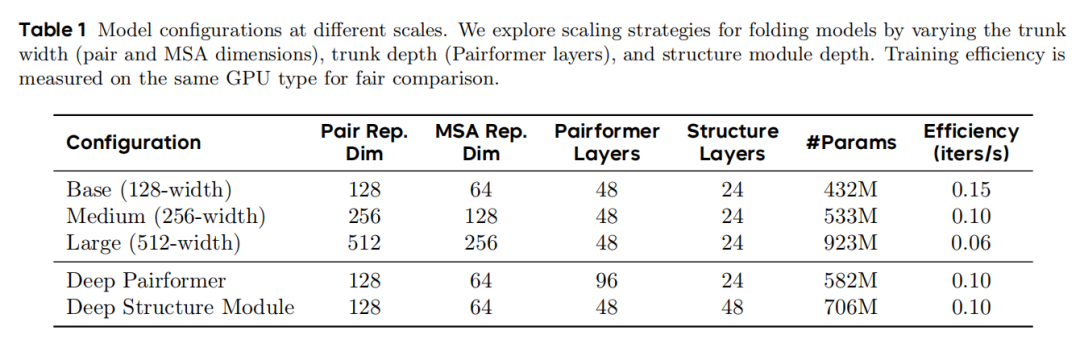
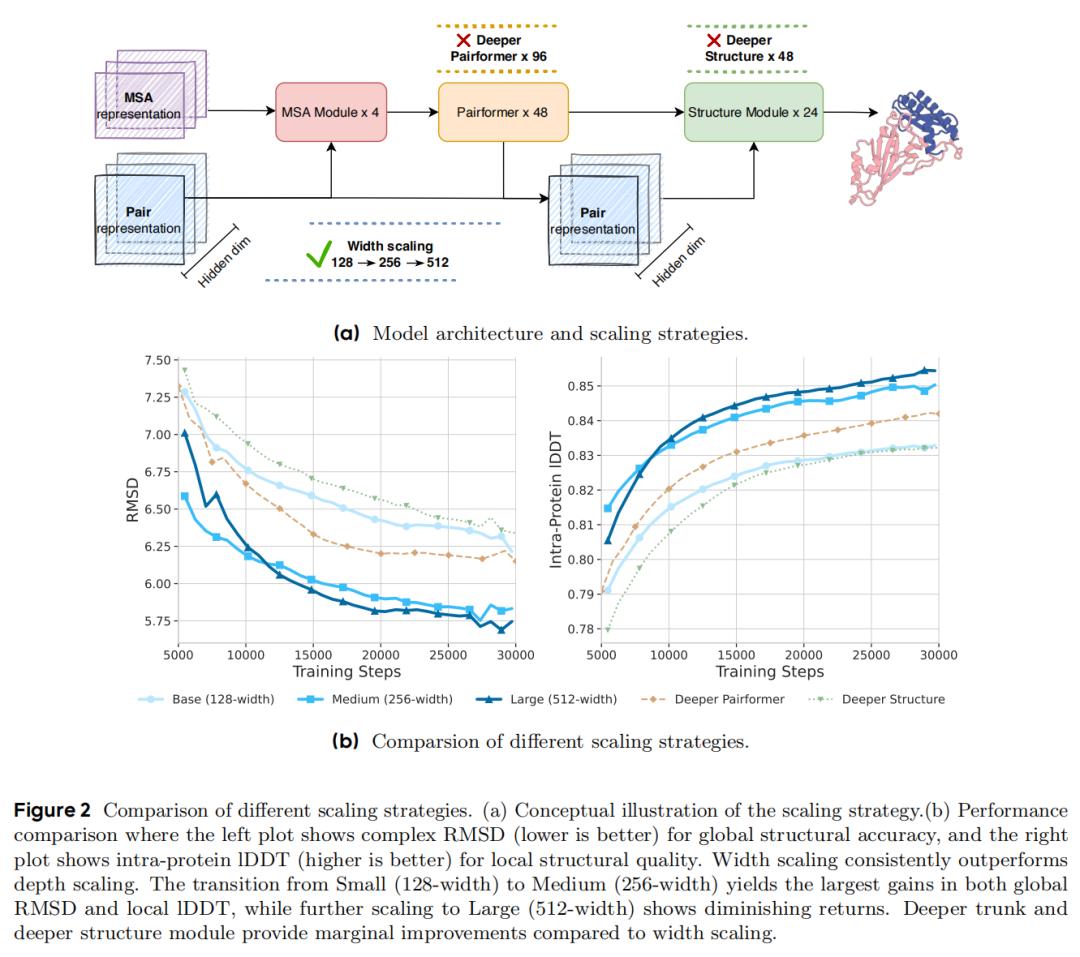
- 宽度缩放:将Pairformer的成对表示维度从128逐步提升至256、512,同步扩展MSA模块的隐藏维度(64→256),模型参数从432M增至923M;
- 深度缩放:Pairformer层数从48增至96(Deep Pairformer),或结构模块层数从24增至48(Deep Structure Module);
- 实验结果:宽度缩放的性能提升显著优于深度缩放,其中128→256维度扩展带来全局结构精度(RMSD)和局部质量(lDDT)的最大增益,512维度虽仍有提升但边际收益递减,符合深度学习模型的缩放定律。
(2)核心原理
成对表示维度的提升直接增强了模型编码分子间复杂相互作用的能力,这与DeepSeek-V3(671B参数,隐藏维度7168)的设计理念一致——在足够深的架构基础上,宽度扩展是提升模型容量的更高效路径。而结构模块的深度缩放收益有限,因其核心功能是将成对表示转换为原子坐标,而非特征学习。
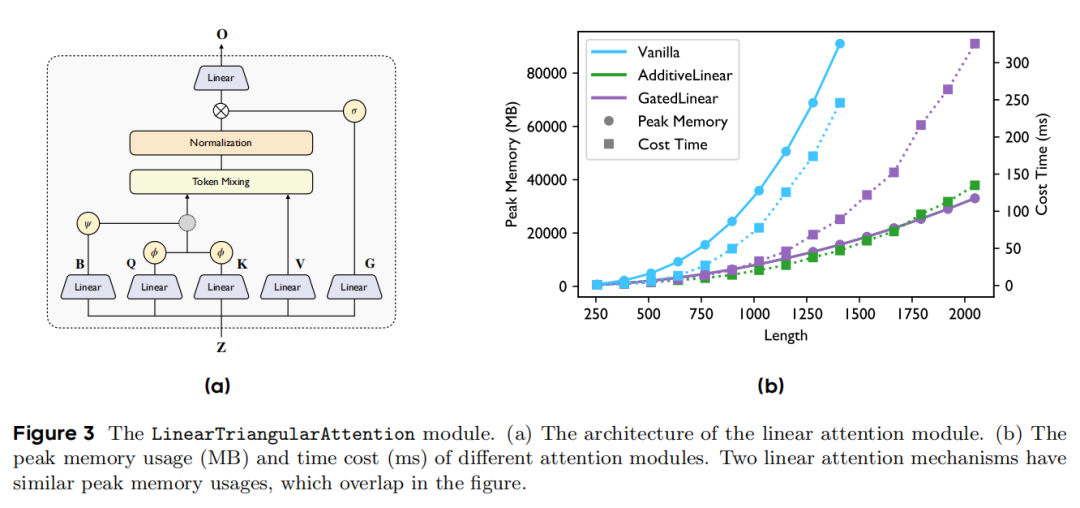
2. 架构创新:线性三角注意力的高效计算方案
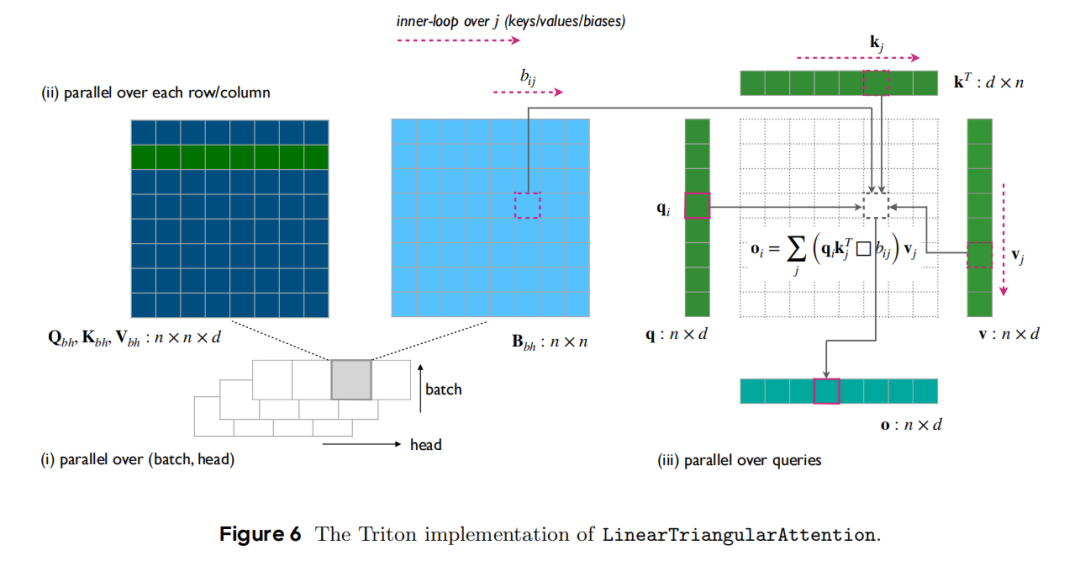
为解决三角注意力的立方级复杂度瓶颈,SeedFold提出线性三角注意力(LinearTriangularAttention),通过融合大语言模型的线性注意力技术与折叠模型的几何推理需求,实现复杂度从O(n³d)到O(nd²)的量级降低:
(1)技术设计
- 核心改造:用非线性特征映射(φ=relu)替代softmax,将注意力计算从
softmax(QK^T+B)V重构为φ(Q)φ(K^T)□ψ(B)V,保留几何推理必需的偏置项B; - 两种变体:
- 加法型(AdditiveLinearTriAtt):通过
+运算融合偏置项,继承原始注意力的优势,内存占用可分摊; - 门控型(GatedLinearTriAtt):通过
⊙运算(sigmoid门控)控制信息流动,在核酸相关任务中表现更优,配合Triton内核优化实现内存高效计算。
- 加法型(AdditiveLinearTriAtt):通过
(2)性能优势
实验显示,线性注意力与原始注意力在多数任务上性能相当,且峰值内存占用和计算时间显著降低(如图3所示),为长序列分子预测提供了可行性。门控型变体在蛋白-RNA、蛋白-DNA相互作用预测中表现突出,验证了其处理多样化分子类型的能力。
3. 数据构建:26.5M大规模蒸馏数据集的工程化实现
为解决实验数据稀缺问题,SeedFold构建了由实验数据和蒸馏数据组成的混合训练集,总规模达26.5M(是实验数据集0.18M的147倍):
(1)数据集构成
数据集 | 类型 | 样本量 | 权重 | 核心作用 |
|---|---|---|---|---|
PDB | 实验 | 180,540 | 0.50 | 保证基础数据质量,提供真实结构约束 |
AFDB | 蒸馏 | 3,326,991 | 0.08 | 补充短链单体结构(中位长度95),提升基础折叠能力 |
Mgnify | 蒸馏 | 23,075,211 | 0.42 | 提供高多样性长序列(中位长度435),仅200万样本与AFDB重叠 |
(2)构建逻辑
- 蒸馏策略:基于AlphaFold2的官方权重,通过OpenFold生成高质量结构,利用知识蒸馏将强正则化模型的学习成果迁移至SeedFold,弥补Transformer架构归纳偏置的缺失;
- 数据筛选:AFDB筛选pLDDT>0.8的结构,Mgnify过滤小于200残基的序列,通过MMSeqs2聚类保证序列多样性,避免过拟合。
4. 训练优化:稳定性与精度的平衡方案
宽度缩放带来的训练不稳定性(梯度爆炸、损失坍塌)通过以下技术解决:
- 两阶段训练:先以384 token裁剪尺寸、64 batch size训练60k迭代,再以640 token裁剪尺寸、32 batch size训练40k迭代,兼顾效率与长序列处理能力;
- 精度适配:MSA模块和Pairformer采用bfloat16,结构模块采用float32,避免局部距离指标(lDDT)的精度损失;
- 超参调整:扩展热身周期(1000→3000步),降低大模型(512-width)的学习率(0.0018→0.001),确保稳定收敛。
三、性能验证:FoldBench基准的全面超越
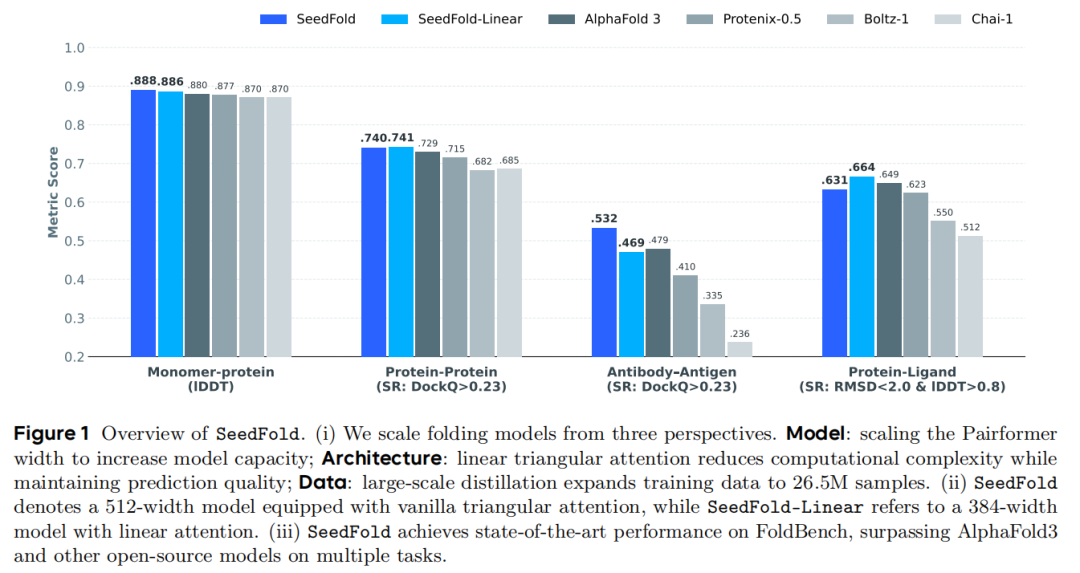
SeedFold在包含1522个生物组装体的FoldBench基准测试中,覆盖9类预测任务(单体、蛋白-蛋白、抗体-抗原、蛋白-配体等),大多数展现出state-of-the-art性能:
1. 核心指标对比
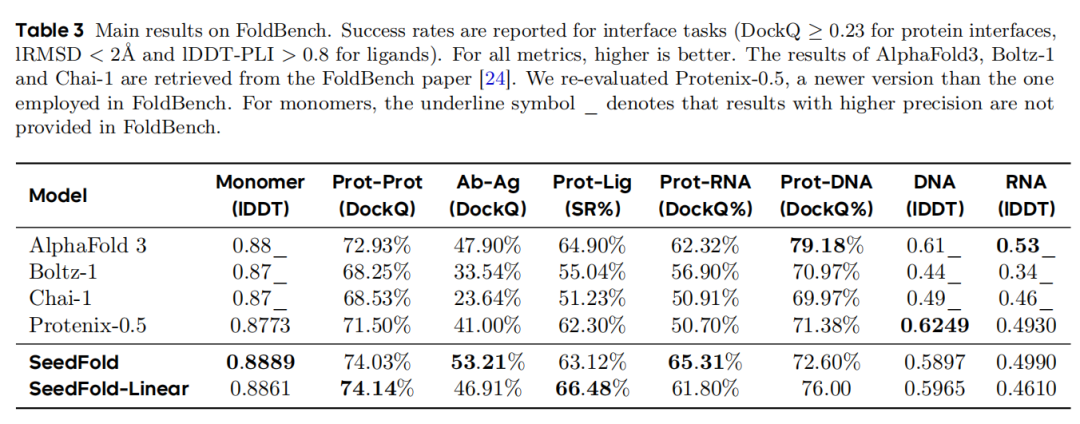
关键结论:
- SeedFold(512-width+原始注意力)在蛋白单体、抗体-抗原、蛋白-RNA相互作用中超越AlphaFold3;
- SeedFold-Linear(384-width+门控线性注意力)在蛋白-配体(66.48%)和蛋白-蛋白(74.14%)任务中表现最优;
- 两种变体的任务特异性优势,验证了异构注意力机制融合的价值。
2. 界面预测的细粒度分析
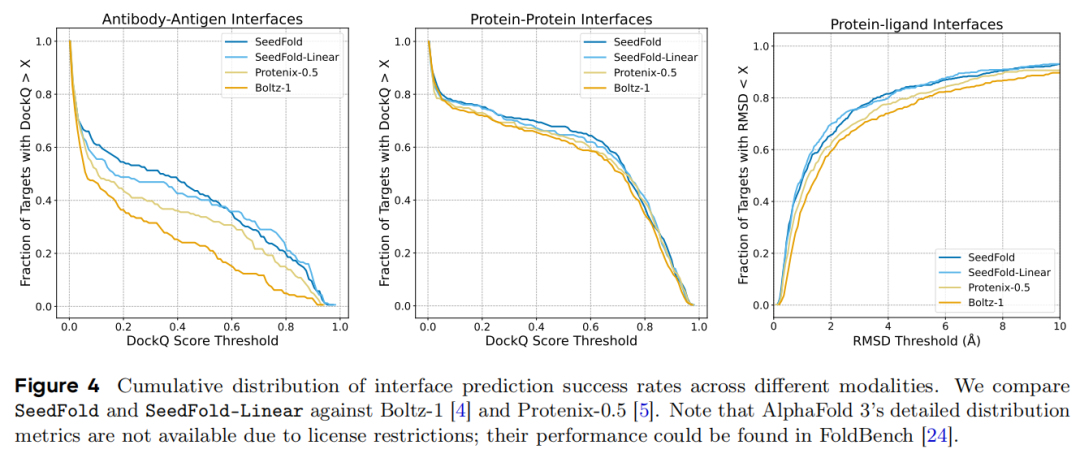
通过累积分布曲线(图4)可见:
- 抗体-抗原界面:SeedFold在全DockQ分数区间领先,展现出对复杂免疫分子相互作用的精准建模能力;
- 蛋白-配体界面:SeedFold-Linear在低RMSD阈值下的目标覆盖率更高,对药物设计至关重要;
- 蛋白-蛋白界面:两模型均优于Protenix-0.5和Boltz-1,且在高DockQ分数段保持优势,说明其预测的可靠性。
3. 消融实验验证核心组件价值
- 注意力机制对比:门控型线性注意力在核酸相关任务中显著优于加法型和原始注意力,在抗体-抗原、蛋白-配体任务中略有优势;
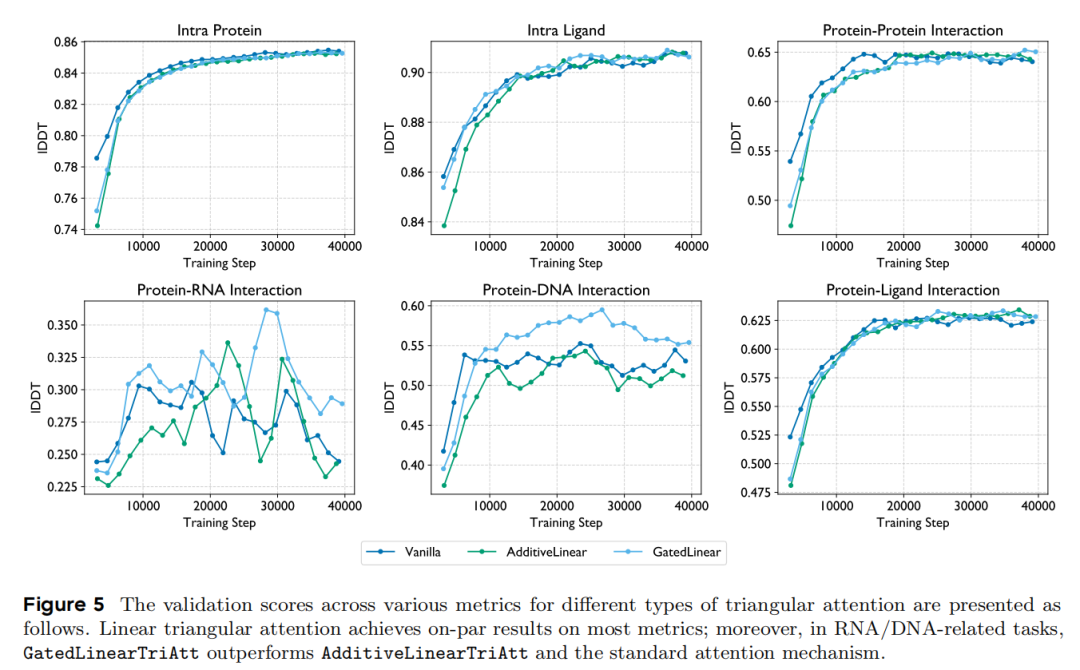
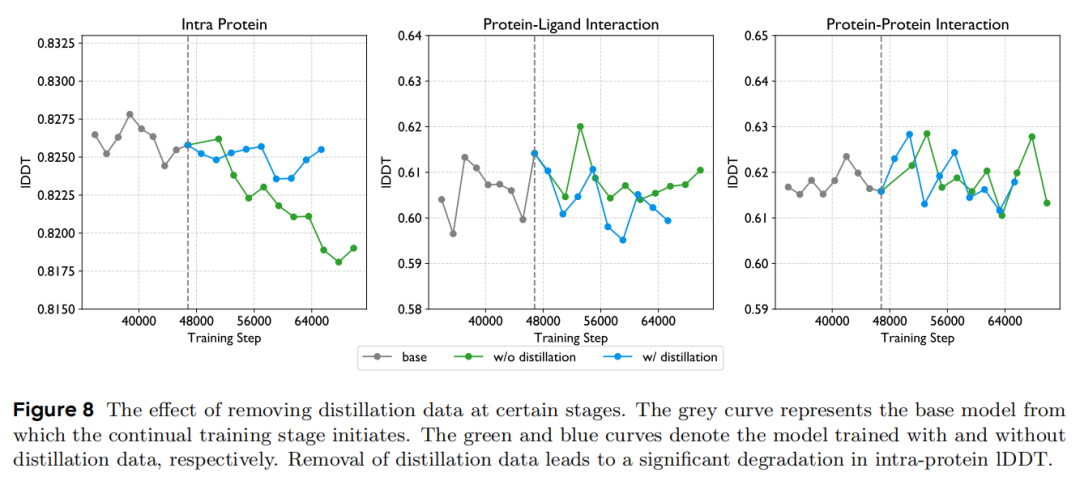
- 蒸馏数据必要性:移除单体蒸馏数据后,蛋白内部结构预测的lDDT显著下降,验证了蒸馏数据对模型基础折叠能力的支撑作用,避免知识衰减。
四、领域影响与未来方向
1. 技术范式的革新意义
- 确立宽度缩放为折叠模型的核心扩展路径,打破 深度至上 的传统认知,为后续模型设计提供参考;
- 线性注意力与折叠模型的融合,为解决长序列、复杂复合物预测的计算瓶颈提供了可复用方案;
- 大规模蒸馏数据的构建策略,缓解了生物分子结构实验数据稀缺的行业痛点,为无监督/半监督学习奠定基础。
2. 产业与科研应用价值
- 药物研发:高精度的蛋白-配体、抗体-抗原结合预测,可缩短靶点验证、分子设计周期,降低临床试验失败率;
- 基础研究:支持长链蛋白质、核酸-蛋白复合物的结构解析,助力理解疾病相关分子机制;
- 算力普惠:线性注意力降低了模型部署的硬件门槛,使中小实验室能够开展复杂生物分子结构研究。
五、总结
SeedFold通过 宽度缩放+线性注意力+大规模蒸馏 的三位一体策略,实现了生物分子结构预测的精度与效率双突破,其核心创新不仅在于超越AlphaFold3的性能表现,更在于为生物分子基础模型的规模化发展提供了清晰的技术路径。该研究验证了大语言模型的缩放理念在生物计算领域的适用性,同时结合领域特性进行了架构与数据的定制化设计,为跨学科融合提供了典范。
参考文献:Yi Z, Chan L, Yiming M, et al. SeedFold: Scaling Biomolecular Structure Prediction[J]. arXiv preprint arXiv:2512.24354, 2025.
项目链接:https://seedfold.github.io/
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-01-13,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

