波士顿大学团队 探究AlphaFold3赋能隐蔽位点预测:配体・AI・隐蔽位点
波士顿大学团队 探究AlphaFold3赋能隐蔽位点预测:配体・AI・隐蔽位点

DrugIntel
发布于 2026-01-16 16:36:32
发布于 2026-01-16 16:36:32

隐蔽位点(cryptic pockets)的精准预测一直是突破“不可成药”蛋白靶点的关键瓶颈。这类位点仅在蛋白质发生构象变化时才会形成或暴露,其独特的动态特性使其成为拓展可成药靶点库的核心资源,尤其在变构调节、PROTACs设计等创新药物研发方向中具有不可替代的价值。
近日,波士顿大学Diane Joseph-McCarthy团队在bioRxiv发表的研究《The Influence of Ligands on AlphaFold3 Prediction of Cryptic Pockets》,通过系统的实验设计与深度数据分析,揭示了AlphaFold3(AF3)在隐蔽位点预测中的潜在应用价值。当给定蛋白质的隐秘位点配体时,AF3主要预测出能够结合该配体的构象;而在缺乏配体的情况下,缺失隐秘口袋的构象通常占主导地位。尽管结果可能反映了对记忆结构先验的偏好,但作者认为这种有害记忆的程度似乎有限。
一、研究背景:隐蔽位点预测的科学挑战与技术演进
1. 隐蔽位点的生物学意义与成药价值
隐蔽位点是蛋白质在天然状态下隐藏、经构象重排(如侧链翻转、环区运动、结构域移位等)后形成的功能性结合位点,其核心价值体现在三方面:
- 拓展可成药靶点范围:使传统方法无法识别的“无明显活性位点”蛋白成为药物靶点;
- 提升药物特异性:相比天然活性位点,隐蔽位点的结构特异性更高,可减少脱靶效应;
- 支持创新药物形式:为变构抑制剂、分子胶、PROTACs等新型药物提供结合靶点。
然而,隐蔽位点的动态性与依赖性(依赖配体结合或构象变化)使其预测面临双重挑战:一是蛋白质构象系综的采样难度,二是位点形成与配体结合的协同关系难以建模。
2. AlphaFold3的技术革新与研究动机
AF3其采用统一的扩散模型框架,将蛋白质、配体等分子组件视为整体系统进行建模,具备直接预测配体结合与未结合的蛋白结构的能力。这一技术革新为解决隐蔽位点预测的核心痛点提供了可能——既能够捕捉蛋白质构象变化的动态范围,又能整合配体对构象的诱导效应。
本研究基于前期AlphaFold2的隐蔽位点预测研究基础,进一步聚焦三大核心科学问题:AF3能否复现隐蔽位点形成所需的构象变化尺度?配体存在与否及配体类型如何影响预测结果?AF3预测的配体-蛋白结合模式准确性及可靠性如何?通过对16种已知隐蔽位点的蛋白进行系统验证,为上述问题提供了明确答案。
二、研究设计:严谨的实验体系与多维度验证框架
1. 测试集构建:覆盖多样化隐蔽位点类型
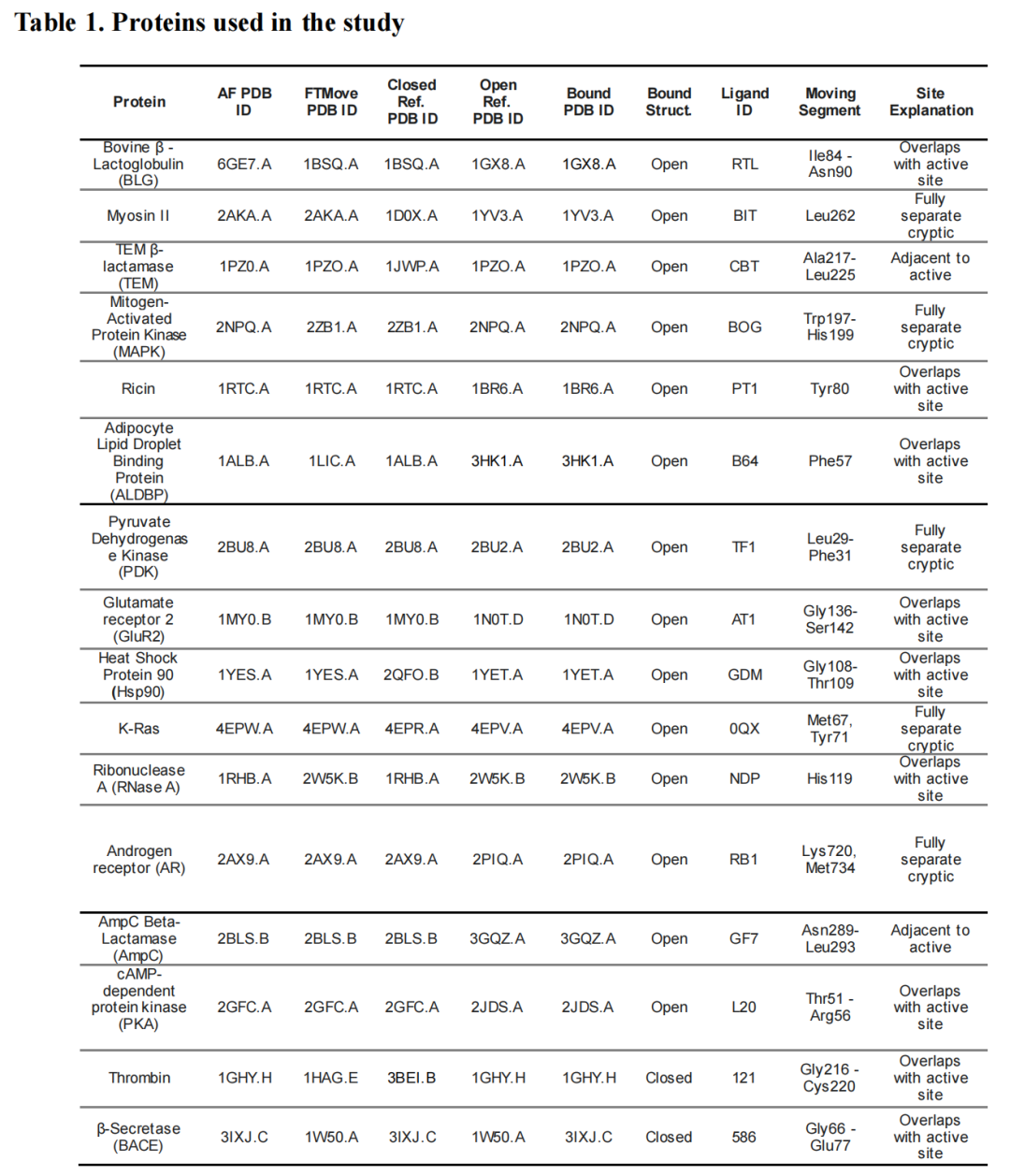
研究选取16种代表性蛋白(含15种来自CryptoSite数据库及1种K-Ras蛋白),其隐蔽位点具有明确的结构特征与分类:
- 位点关系:与活性位点重叠(如BLG、RNase A)、相邻(如TEM、AmpC)或完全独立(如MAPK、K-Ras);
- 构象变化类型:侧链重排(如RNase A的His119)、环区运动(如PKA的Thr51-Arg56)、螺旋移位(如K-Ras的Met67-Tyr71);
- 结合状态特征:14种蛋白的结合态为开放构象,2种(凝血酶、BACE)为闭合构象(配体结合诱导位点闭合)。
测试集的多样性确保了研究结论的普适性,为不同类型隐蔽位点的预测提供了参考标准。
2. 预测与分析方法:
- AF3预测设置:采用无模板建模策略,通过100个随机种子生成500个模型,分别进行配体存在(输入对应SMILES)与不存在两种条件下的预测;
- 构象评估指标:以蛋白质数据库(PDB)中实验解析的结合态/未结合态结构为参考,计算移动片段(与隐蔽位点形成相关的氨基酸片段)的RMSD(均方根偏差),量化预测构象与实验结构的一致性;
- 配体结合评估:通过配体构象RMSD、口袋识别准确性、配体-蛋白空间位阻冲突等指标,评估配体定位的准确性;
三、核心发现:AF3在隐蔽位点预测中的优势与特性
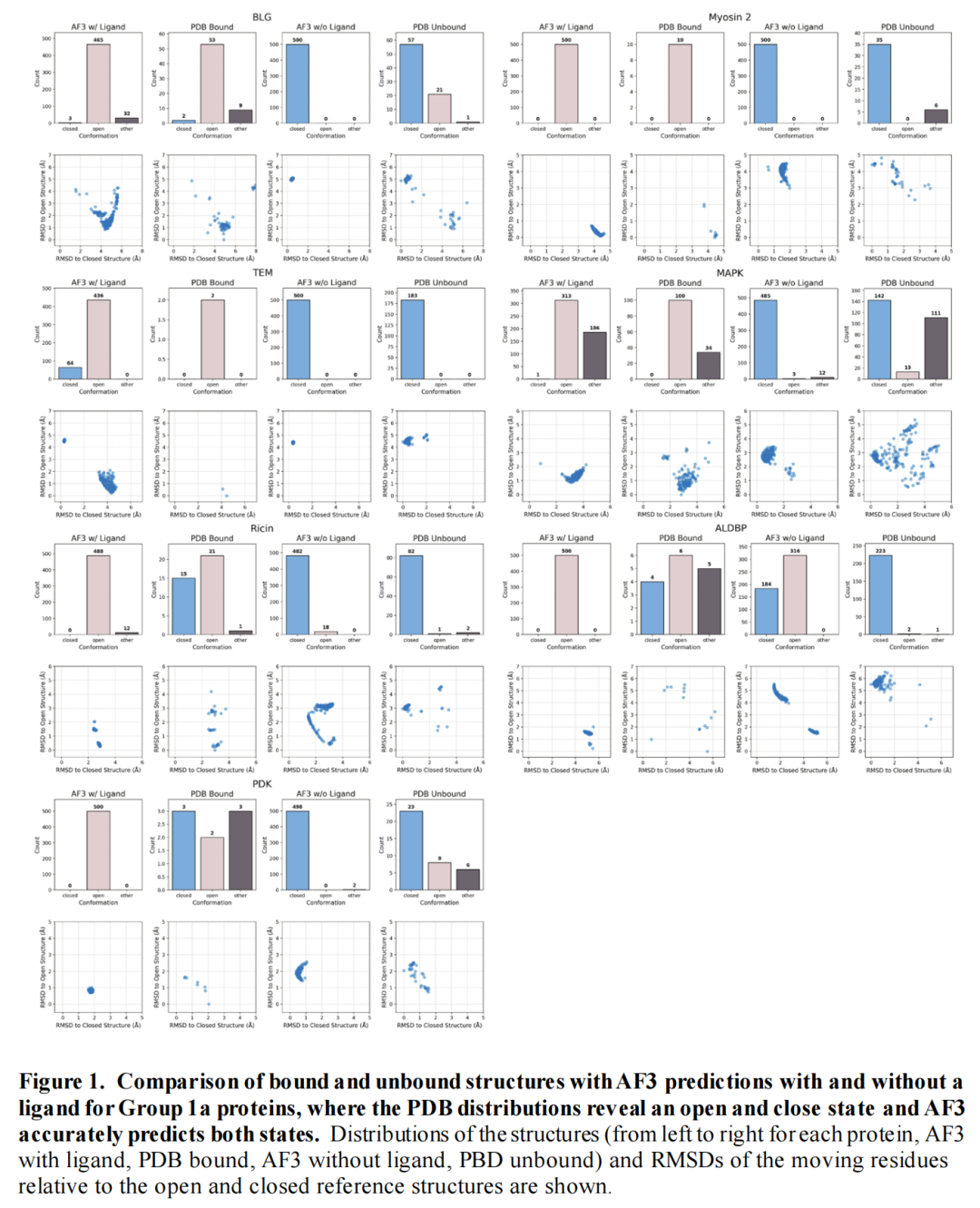
1. 构象变化的精准复现:匹配实验分布的动态范围
AF3展现出卓越的构象采样能力,能够准确复现隐蔽位点形成所需的构象变化尺度:
- 配体存在时:16/16的蛋白预测分布与PDB中结合态结构分布完全吻合,且以开放构象(含隐蔽位点)为主;
- 配体不存在时:13/16的蛋白预测分布与PDB中未结合态结构分布一致,以闭合构象(无隐蔽位点)为主;
- 构象覆盖度:同一多序列比对(MSA)可支持侧链移动、环区摆动、螺旋移位等多种构象变化,且变化幅度与实验观测完全匹配。
这一结果表明,AF3突破了AlphaFold2对优势构象的依赖,能够通过配体信号调控构象采样方向,为隐蔽位点的动态形成机制提供了精准模型。
2. 配体的双重调控作用:存在性与类型的关键影响
研究明确配体对AF3预测的双重调控效应,为预测策略优化提供了关键依据:
- 配体存在性的决定作用:配体作为“构象选择信号”,可引导AF3优先采样能容纳配体的开放构象;而无配体时,模型倾向于采样能量更低的闭合构象,与蛋白质的天然构象分布一致;
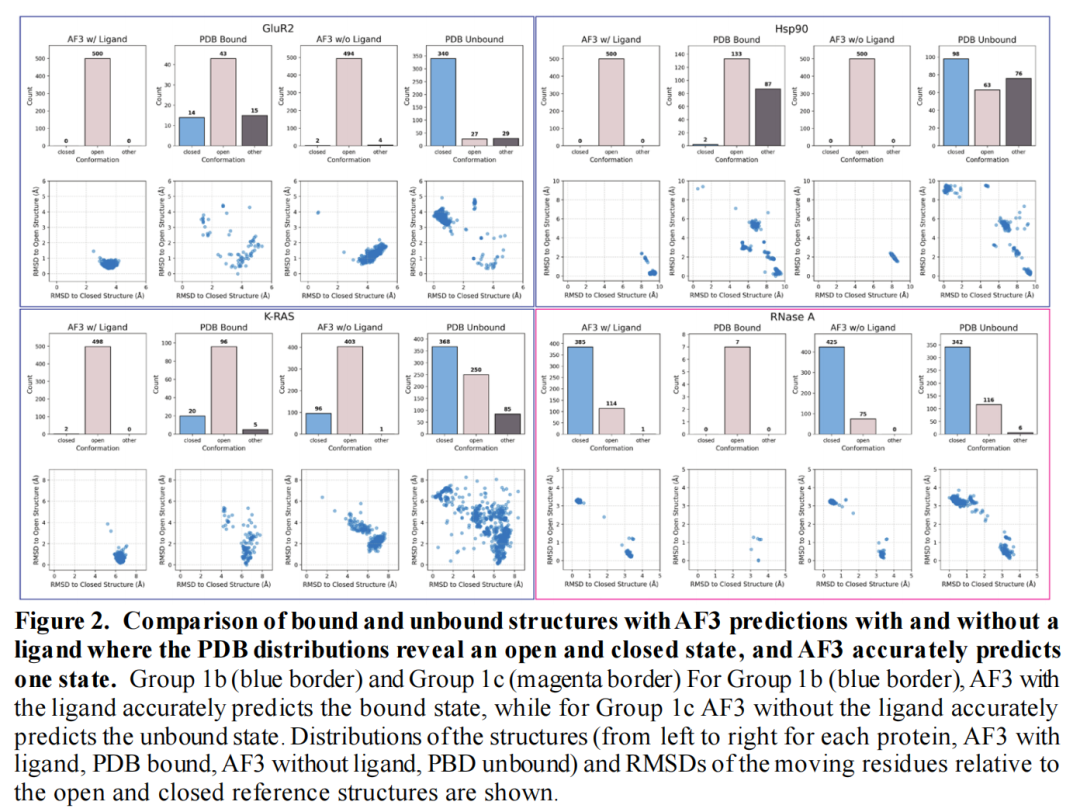
- 配体类型的调控效应:不同配体可诱导不同构象状态。例如,GluR2蛋白在输入小分子谷氨酸(无法打开隐蔽位点)时,AF3预测为闭合构象;而输入参考配体ATPO(可诱导位点开放)时,预测为开放构象;TEM蛋白与3个氙原子结合时,AF3可预测氙原子在隐蔽位点的重叠结合模式。
这一发现为针对性设计预测策略提供了可能——通过选择合适的配体分子,可定向诱导AF3采样目标构象。
3. 配体结合预测的高准确性与可靠性指标
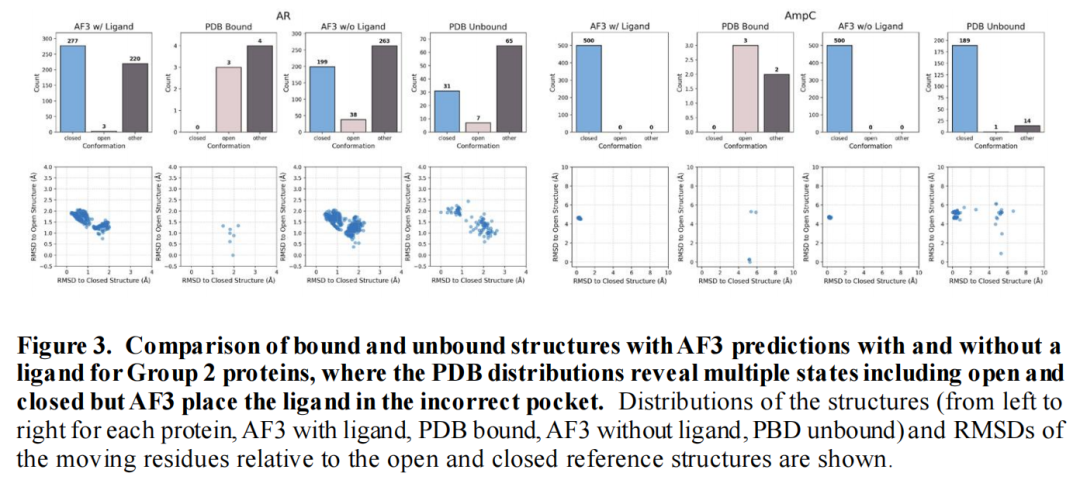
AF3在配体定位与口袋识别方面表现出高准确性,同时提供了可量化的可靠性评估标准:
- 口袋识别准确性:14/16的蛋白中,AF3能正确识别隐蔽位点;仅AR和AmpC因模型记忆偏差,将配体错误定位至活性位点(正构位点);
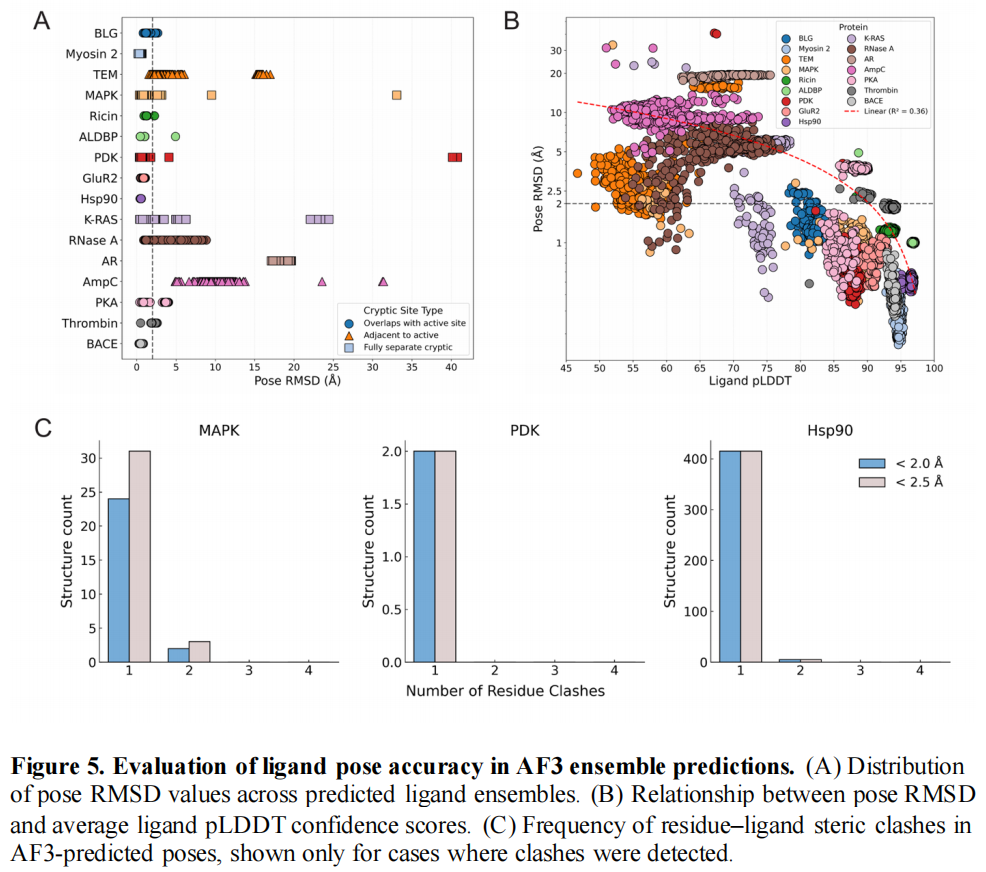
- 配体构象准确性:10/16的蛋白中,≥94%的模型配体构象RMSD≤2.5Å(接近实验解析精度),其中Myosin II、GluR2等蛋白的正确构象比例达100%;
- 可靠性关联:配体的pLDDT分数(局部距离差异测试分数)与构象准确性呈正相关(R²=0.35),高pLDDT模型(>95)的配体定位错误率显著降低。
值得注意的是,MAPK、PDK、Hsp90等蛋白的预测中出现配体与蛋白的空间位阻冲突(Hsp90中占比达80%),且冲突模型的pLDDT分数仍较高,提示AF3对物理约束的建模仍有优化空间。
4. 记忆偏差的改善:相比AlphaFold2的核心进步
AlphaFold2的主要局限在于对PDB中优势构象的“记忆偏差”,导致难以预测小众构象(如隐蔽位点开放构象)。而本研究表明,AF3的记忆偏差降低:
- 即使PDB中开放构象占比极低(如TEM、Ricin),AF3仍能在配体存在时优先采样开放构象;
- 在少数蛋白(如BACE、RNase A)中出现轻微记忆偏差,且影响程度低于AlphaFold2。
这一进步源于AF3的扩散模型框架对构象系综的高效采样能力,减少了对单一优势构象的依赖。
四、应用价值与技术启示:对药物研发的实质性推动
1. 隐蔽位点药物发现的技术赋能
AF3的预测能力为药物研发提供了多维度支撑:
- 靶点筛选:通过AF3生成的构象系综,可快速识别潜在隐蔽位点,拓展“不可成药”蛋白的成药可能性;
- 机制研究:揭示配体-构象-位点形成的协同关系,为变构调节机制提供结构基础。
例如,在K-Ras、Hsp90等热门靶点的研究中,AF3可预测小分子结合诱导的隐蔽位点开放构象,为针对这些“难成药”靶点的药物设计提供直接参考。
2. 预测策略优化的建议
基于研究结果,提出针对AF3隐蔽位点预测的优化策略:
- 配体选择:优先使用能诱导隐蔽位点开放的特异性配体,避免构象误判;
- 多种子采样:通过增加随机种子数量生成足够的构象系综,覆盖配体结合的多种可能模式;
3. 现存局限与未来方向
研究同时明确了AF3的应用边界,为后续技术改进提供了方向:
- 物理约束建模不足:部分模型存在配体-蛋白空间位阻冲突,需整合分子力学力场进行约束优化;
- 多配体协同预测缺陷:当同时输入活性位点配体与隐蔽位点配体时(如AR的DHT与RB1),AF3难以同时正确定位两种配体;
- 小众构象采样效率:对于PDB中极少出现的隐蔽位点构象(如AR的开放构象),预测准确性仍有提升空间。
未来,通过整合物理模拟与AI模型、扩大隐蔽位点训练数据、优化多配体建模策略,有望进一步提升AF3的预测性能。
五、小结
本研究证了AlphaFold3生成的蛋白质-配体结构系综可以为隐蔽位点的识别提供了可靠工具。使用 AF3 进行广泛采样生成结构集合能够揭示对药物发现有用的隐性口袋。但挑战在于从生成的众多构象中识别那些具有可操作隐性口袋的构象。
文献核心信息
- 标题:The Influence of Ligands on AlphaFold3 Prediction of Cryptic Pockets
- 作者单位:波士顿大学生物医学工程系、化学系
- 文献链接:https://doi.org/10.64898/2026.01.04.697564
- 代码与数据:https://github.com/J-MLab/af3_cryptic
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-01-07,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

