Nat. Methods | GHIST:深度学习驱动的单细胞空间基因表达绘制新方法
Nat. Methods | GHIST:深度学习驱动的单细胞空间基因表达绘制新方法

DrugAI
发布于 2026-01-06 12:41:16
发布于 2026-01-06 12:41:16
DRUGONE
空间转录组学的快速发展为理解疾病机制带来了新的视角,但高昂的成本和实验复杂性限制了广泛应用。研究人员提出了 GHIST,一种基于深度学习的框架,能够结合亚细胞空间转录组数据和多层生物学信息,预测单细胞分辨率的空间基因表达。GHIST 在公开数据集与 TCGA 数据上验证表现优越,展现了在不同分辨率下的灵活性,并能够通过计算方式为已有数据集增加空间组学维度,为多组学分析和生物标志物发现提供了新途径。

空间转录组学(SRT)能在空间层面描绘基因表达分布,极大推动对多细胞系统的理解。但目前主流的点位级(spot-based)平台,如 10x Visium,只能捕获多个细胞的混合信号,难以精确到单细胞。新兴的亚细胞级平台(如 Xenium、CosMx、MERSCOPE)通过细胞分割实现了单细胞空间基因表达,但其成本高昂且获取难度大。相比之下,H&E 组织切片在临床上被广泛采集,若能直接从这些图像中推断单细胞空间基因表达,将为探索细胞异质性和组织空间模式提供极大价值。
现有方法(如 ST-Net、Hist2ST、HisToGene 等)多针对点位级预测,且精度有限,难以在转化医学中应用。因此,研究人员设计了 GHIST,以多任务深度学习的方式结合细胞类型、邻域组成、细胞核形态和单细胞表达等多层信息,提升预测的合理性和准确性。
结果
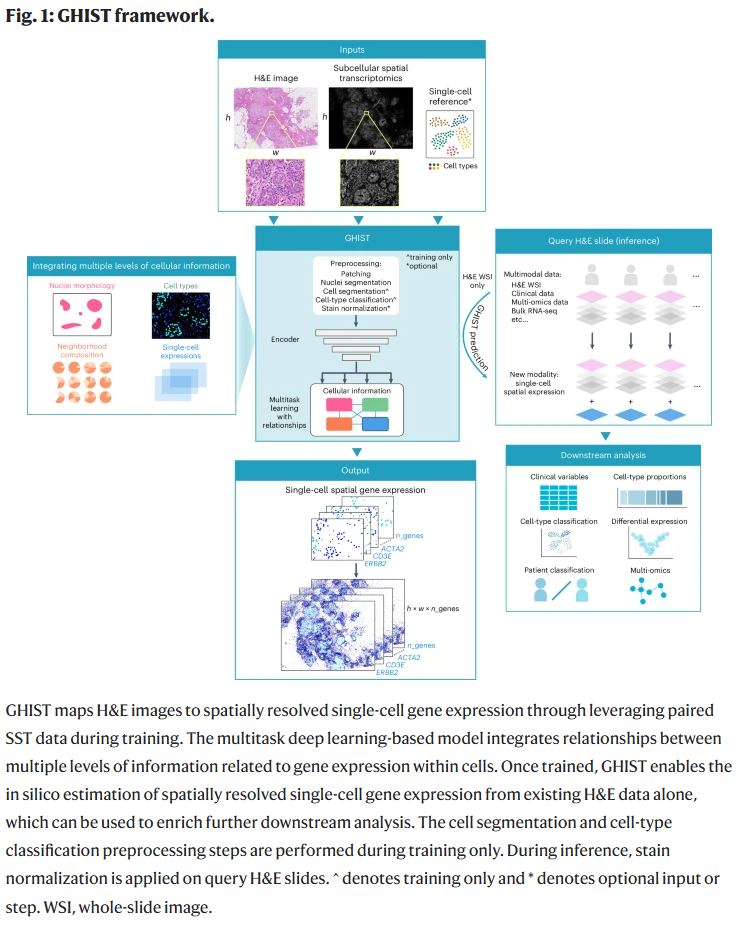
GHIST 框架
GHIST 将 H&E 图像映射到单细胞空间基因表达图谱。其多任务架构包含四个预测模块:
- 细胞类型
- 邻域细胞组成
- 细胞核形态
- 单细胞基因表达
这些模块通过联合学习捕捉多层信息之间的依赖关系,例如利用邻域组成辅助基因表达预测,或利用基因表达信息提升细胞类型分类的准确性。
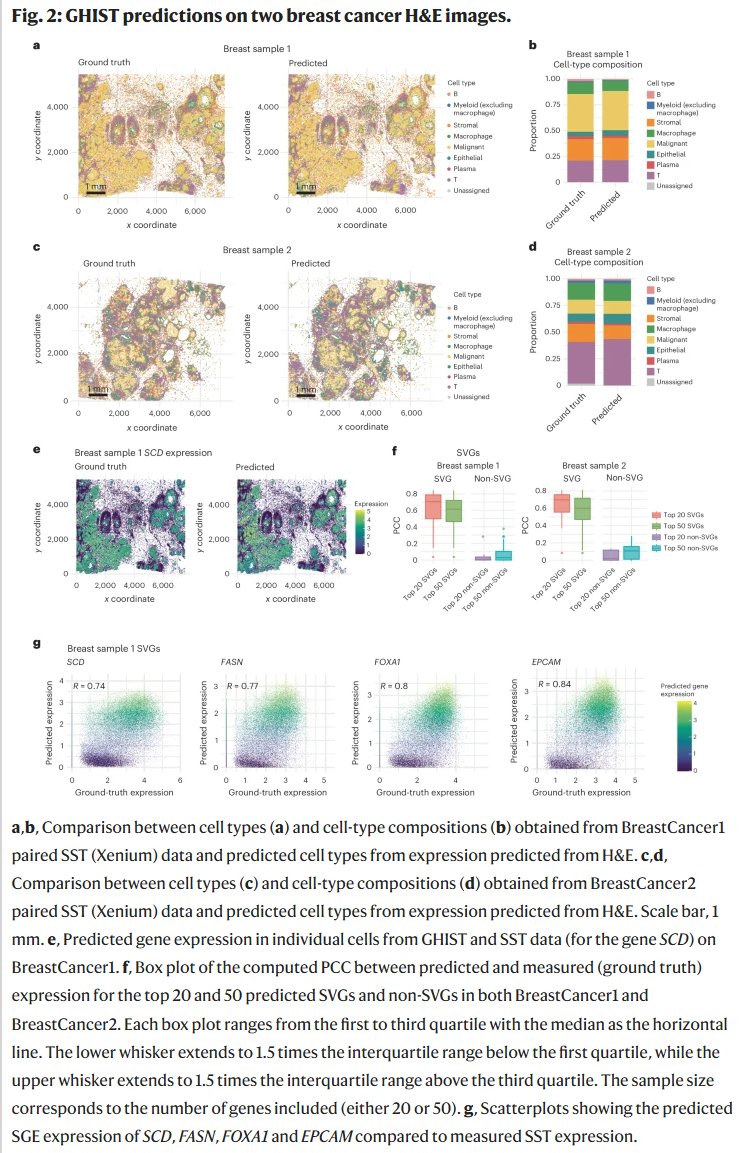
单细胞水平的预测能力
研究人员在乳腺癌样本上展示,GHIST 预测的细胞类型分布与真实值高度一致(准确率 0.66–0.75)。在高变异基因与空间可变基因的相关性分析中,GHIST 预测值与真实值达到 0.6–0.8 的相关性,显著优于现有方法。
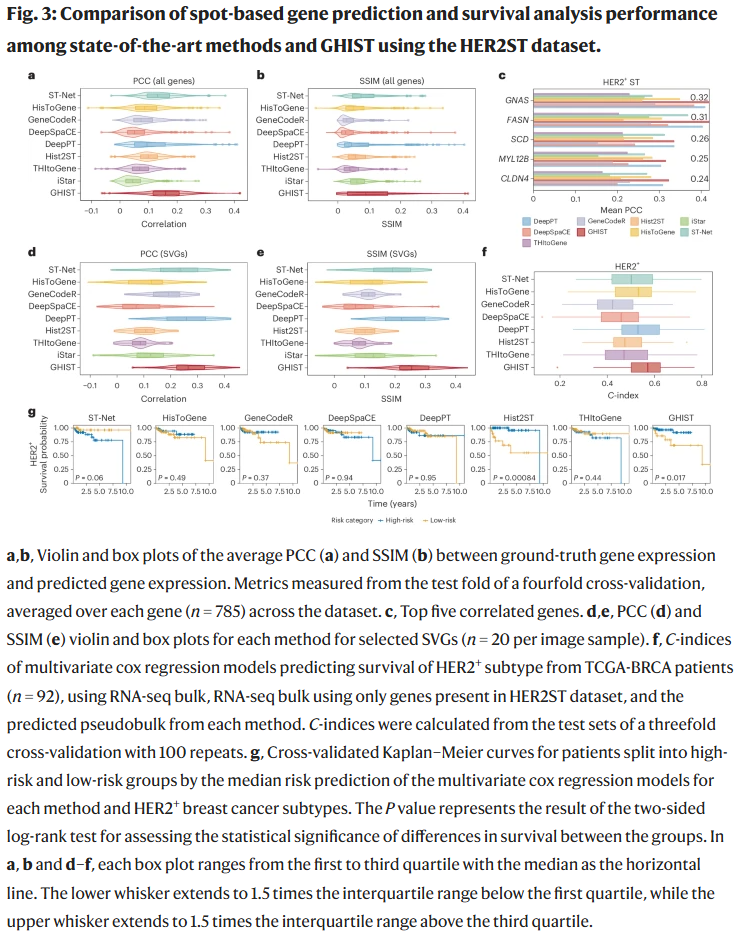
点位级任务中的表现
GHIST 亦可适配点位级数据。在 HER2 阳性乳腺癌数据集中,GHIST 在相关性与结构相似性指标上均优于 ST-Net、DeepPT 等方法。其预测结果更接近真实空间分布,尤其在生物学意义较强的基因上表现更突出。
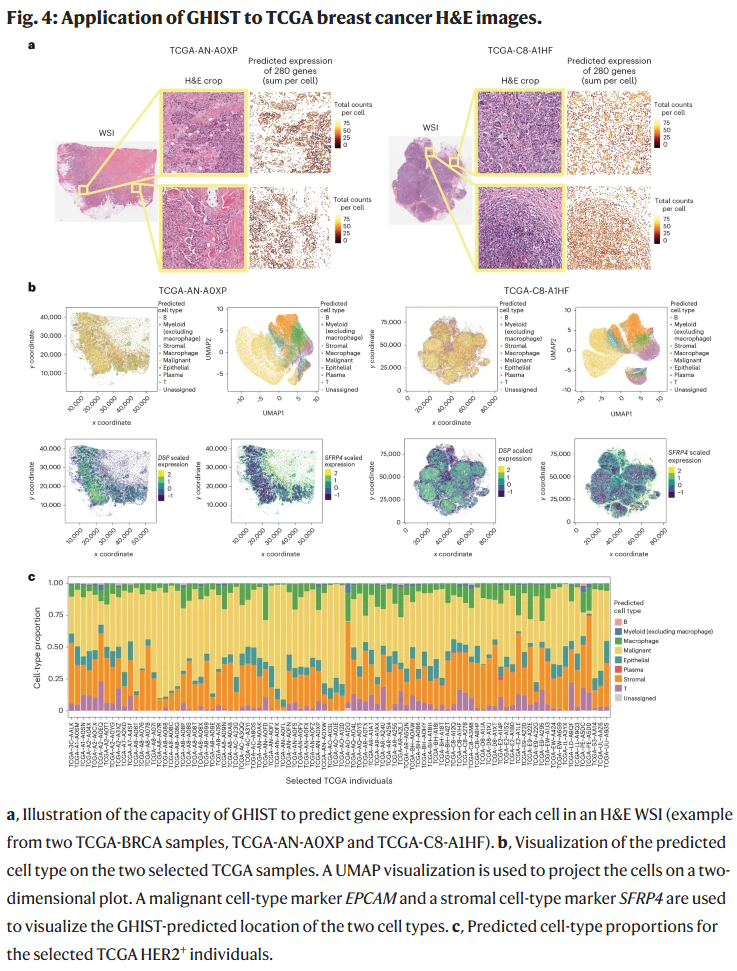
在 TCGA 数据集中的应用
研究人员将 GHIST 应用于 TCGA 乳腺癌队列,预测了 280 个基因的单细胞空间表达。结果显示,恶性细胞标志物 EPCAM 与基质相关基因 SFRP4 在预测图谱中的空间分布与预期一致。不同亚型样本的细胞类型组成与组织病理学特征也得到准确捕捉。
下游分析与临床相关性
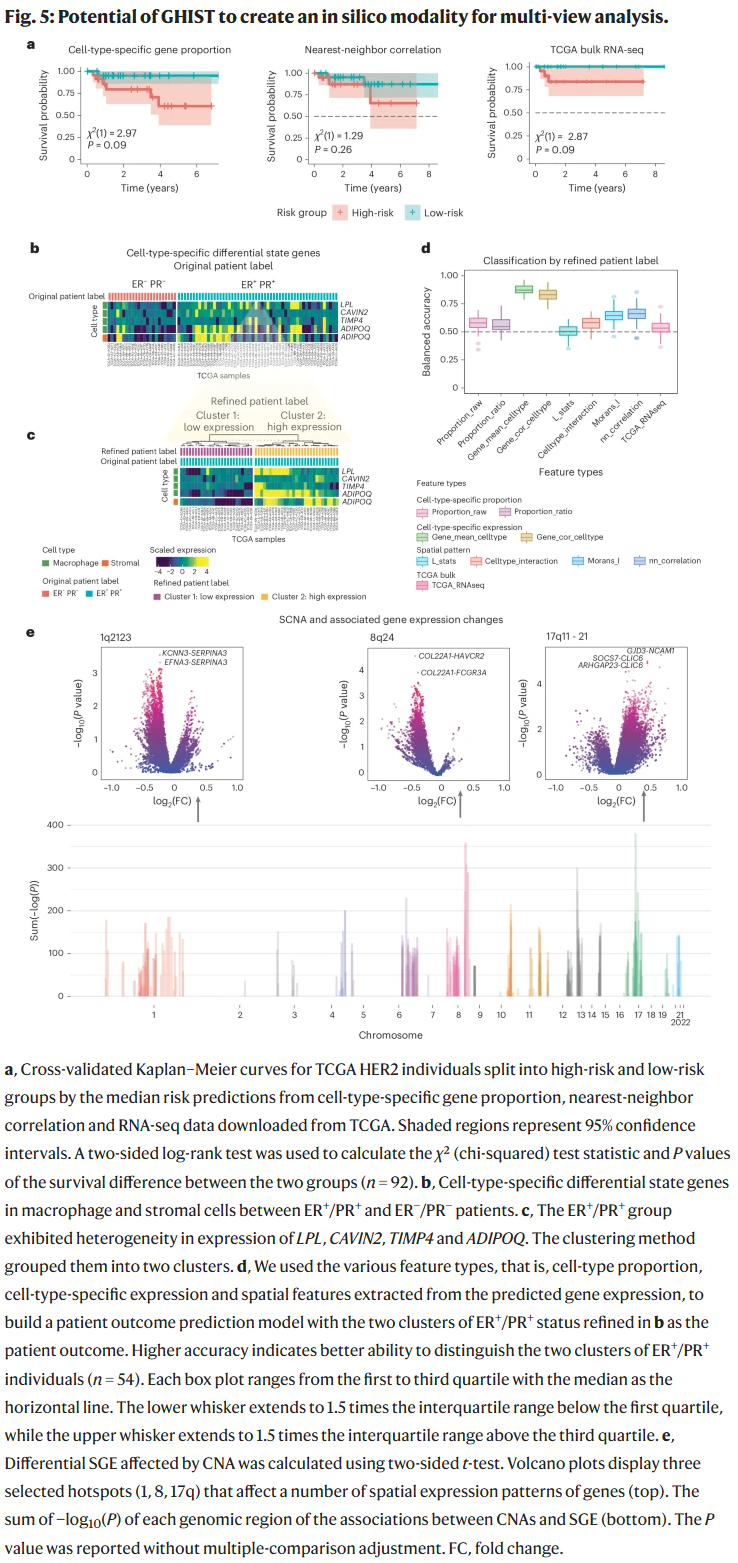
研究人员进一步展示了 GHIST 在预后分析和亚型分层中的应用:
- 生存分析:基于 GHIST 预测的空间基因表达,构建的 Cox 模型能显著区分高危与低危患者。
- 亚型异质性:在 ER+/PR+ 人群中,GHIST 揭示了基因表达的空间异质性,将患者分为两类,其中一类具有更佳生存结果。
- 拷贝数变异关联:GHIST 预测的空间模式揭示了染色体 8q24 和 17q 等热点区域的基因表达差异,与已知的癌症风险区域一致。
讨论
GHIST 是第一个专门设计用于从 H&E 图像推断单细胞空间基因表达的深度学习框架。其优势包括:
- 融合多层生物学信息,实现更合理的预测;
- 同时适用于单细胞与点位级任务;
- 可作为计算手段为大型组织学数据库增加空间组学维度;
- 在 TCGA 等临床数据集上展现转化潜力。
研究人员指出,H&E 切片质量差异会影响预测结果,因此未来需结合标准化染色流程和质量控制。同时,基因面板设计的局限也提醒研究人员,针对不同研究目的定制化面板将进一步提升 GHIST 的精度和应用范围。
GHIST 的能力不仅在于预测单个基因的表达,更在于揭示其在空间上的定位与模式,从而为癌症亚型划分、患者预后预测以及潜在治疗靶点发现提供新的可能性。
整理 | DrugOne团队
参考资料
Fu, X., Cao, Y., Bian, B. et al. Spatial gene expression at single-cell resolution from histology using deep learning with GHIST. Nat Methods (2025).
https://doi.org/10.1038/s41592-025-02795-z
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-09-15,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

