Nat. Med. | 数字孪生与体内模拟试验在药物开发中的兴起
Nat. Med. | 数字孪生与体内模拟试验在药物开发中的兴起

DrugAI
发布于 2026-05-08 19:49:52
发布于 2026-05-08 19:49:52
药物评估的监管格局正在发生深刻变化。数字孪生与体内模拟试验(in silico trials)作为基于计算模拟的创新方法,正从早期用于研发决策的工具,逐步迈向可用于药物审批的证据体系。研究人员指出,这一转变标志着药物开发模式的关键拐点,但其安全、可靠与规范应用仍高度依赖监管机构与公共部门的参与与引导。

药物研发体系的结构性困境
传统药物研发长期面临高成本、低成功率的问题。从临床一期到三期的完整周期通常耗时约七年,平均成本高达数亿美元,但最终成功上市的比例却不足十分之一。这种效率瓶颈使得现有研发模式难以满足临床需求。
与此同时,监管体系也在发生变化。例如,美国监管机构已开始逐步减少某些药物(如单克隆抗体)的动物实验要求,并扩大真实世界证据在审批中的应用范围。这一趋势表明,药物评价体系正在向更加多元化的证据来源转变。
在这一背景下,数字孪生与体内模拟试验逐渐成为提升研发效率与成功率的重要技术路径。
数字孪生:从个体患者建模出发
数字孪生是一种针对单个患者构建的计算模型,用于在真实给药之前预测药物在该患者体内的表现。这类模型通过整合多源数据,包括电子病历、实验室检测结果、基因组信息、医学影像以及可穿戴设备数据,同时结合关于药物作用机制、代谢路径和疾病进展的科学知识,实现个体化预测。
在计算层面,人工智能和机器学习算法用于从复杂数据中提取变量之间的关系,从分子水平一直延伸到器官与系统层面。最终,这些模型能够预测药物疗效、不良反应以及最优治疗方案。
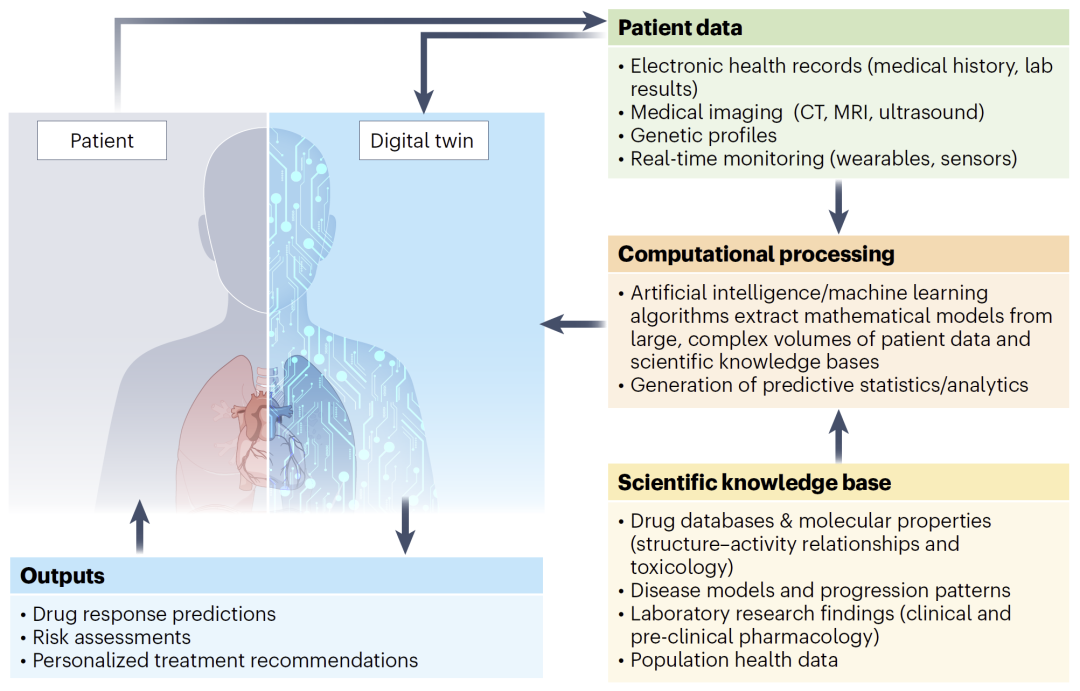
图1:数字孪生构建流程(患者数据→知识库→计算建模→个体化预测)。
体内模拟试验:从个体到群体的扩展
如果说数字孪生关注单个患者,那么体内模拟试验则将这一理念扩展到人群层面。研究人员通过整合多个数字孪生模型,或构建符合统计特征的“虚拟患者”,形成虚拟队列,从而模拟临床试验过程。
这种方法可以用于补充甚至部分替代传统临床试验中的对照组,尤其是在某些难以开展真实试验的场景中,例如孕期用药、罕见疾病或高风险人群研究。此外,它还可以用于探索不同剂量方案、入组标准及终点指标,从而在正式试验前优化设计。
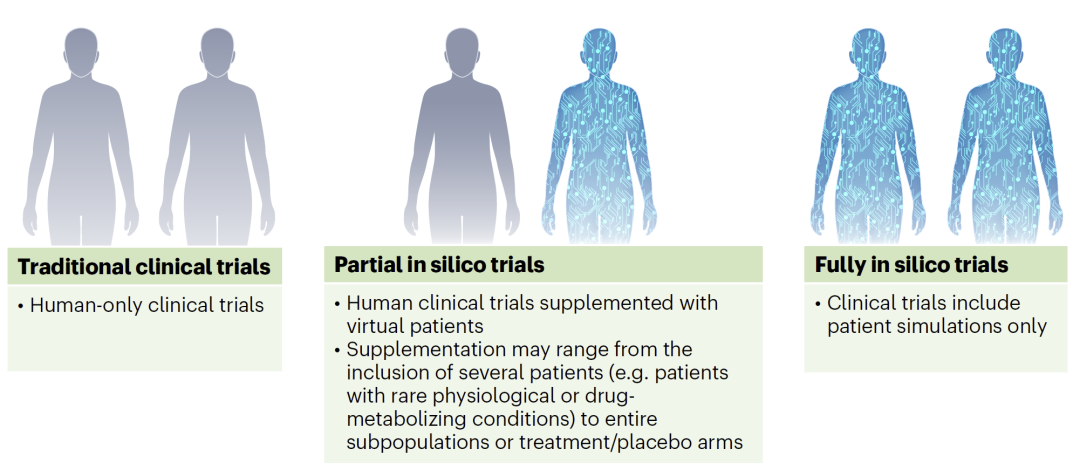
图2:体内模拟试验形式(传统试验、部分虚拟试验与完全虚拟试验)。
应用前景:从预测到优化
数字孪生与体内模拟试验在多个关键环节展现出应用潜力。首先,在风险评估方面,研究人员已经利用器官级数字孪生(如心脏或肝脏模型)预测药物可能引发的心律失常或肝毒性,从而在人体试验前筛除高风险候选物。
其次,在临床试验设计方面,这些技术能够通过虚拟对照组减少所需样本量,提高试验效率,使更多患者能够接受潜在有效治疗。
此外,在特殊人群研究中,体内模拟试验可以填补传统试验的空白。例如儿童、孕妇或具有特殊代谢特征的人群,往往难以纳入常规试验,而计算模型可以在不增加风险的情况下提供预测结果。
进一步地,数字孪生还支持高度个体化试验设计。在某些精准医疗场景中,一个患者的“虚拟自身”甚至可以作为对照,从而实现真正意义上的个体化评估。
方法基础:机制模型与数据驱动模型
数字孪生与体内模拟试验依赖两类核心建模方法。一类是机制模型,通过显式描述生物学过程(如药物与受体结合、代谢路径等)来预测结果。这类模型具有较强的可解释性,但依赖大量先验知识。
另一类是统计或数据驱动模型,通过机器学习从数据中自动学习模式。这类方法能够捕捉复杂关联,但往往缺乏透明性。
在实际应用中,两类方法通常结合使用,以在预测能力与可解释性之间取得平衡。
技术挑战:准确性与证据体系
随着这些方法逐步进入监管视野,一个核心问题变得尤为关键:模型需要达到怎样的准确性,才能作为药物审批依据?
与传统临床试验不同,计算模型缺乏统一的验证标准。其可接受性取决于具体应用场景。例如,用于剂量优化的模型与用于替代对照组的模型,在监管要求上应有不同标准。
此外,不同模型之间可能产生相互矛盾的预测结果,而当前尚缺乏明确的规则来判断应优先采信哪种证据。这种不确定性增加了监管难度,也影响技术的可信度。
伦理与监管挑战:信任与公平
除了技术问题,这些方法还带来一系列伦理与监管挑战。首先是数据使用与知情同意问题,当模型基于真实患者数据构建时,其使用边界尚不明确。
其次是公平性问题。如果模型训练数据来源不均衡,可能导致对某些人群预测不准确,从而引发医疗不公平。
此外,计算模型在审批中的应用可能带来不确定性风险。研究人员认为,需要明确规定可接受的不确定性范围,并通过上市后研究进行验证。
建立公众与临床医生的信任,也需要提高模型透明度并加强监管监督。
监管路径:迈向规范化应用
为了推动数字孪生与体内模拟试验的规范应用,研究人员提出需要建立一系列监管原则。这包括根据风险设定验证标准、明确不同监管部门之间的职责划分,以及建立处理证据冲突的框架。
同时,应明确基于计算证据获批药物是否需要上市后验证,以及如何开展相关研究。此外,通过试点项目推动监管机构与企业的早期合作,将有助于形成可复制的实践经验。
实现这些目标还需要持续投入,包括建设专业人才队伍、完善计算基础设施以及提升监管能力。
走向“虚拟临床试验时代”
数字孪生与体内模拟试验为解决药物研发长期存在的问题提供了重要机遇。它们有望降低研发成本、提高成功率,并使更多患者更早获得有效治疗。
然而,这一技术路径的成功应用依赖于完善的监管框架与跨机构协作。研究人员强调,当前正处于关键窗口期:如果能够及时建立规范,这些技术将推动药物研发进入一个更加高效、安全和个性化的新时代;反之,则可能因缺乏监管而失去信任。
最终,数字孪生与体内模拟试验不仅是技术创新,更代表着药物开发范式的深刻转变。
整理 | DrugOne团队
参考资料
Eadie, A.L., Lynch, H.F., Scheinerman, N. et al. The arrival of digital twins and in silico trials in drug development. Nat Med (2026).
https://doi.org/10.1038/s41591-026-04344-3

本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-04-28,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

