Nat. Biomed. Eng. | 跨物种知识迁移驱动的深度学习光谱图像分析新范式
Nat. Biomed. Eng. | 跨物种知识迁移驱动的深度学习光谱图像分析新范式

DrugAI
发布于 2026-01-29 12:36:33
发布于 2026-01-29 12:36:33
DRUGONE
光学成像技术,尤其是结合机器学习分析的高光谱成像,在临床手术导航与组织识别方面具有巨大潜力。然而,该领域面临一个关键瓶颈:缺乏规模足够大、具有代表性的临床训练数据。相比之下,动物实验能够在标准化条件下获取大量数据,并可人为诱导多种病理状态,但这些实验在人体中因伦理限制难以实施。
研究人员提出 Xeno-learning(跨物种学习) 概念,通过在不同物种之间迁移光谱变化规律,实现跨物种知识转移。基于来自人类、猪和大鼠共 14,013 张高光谱图像的数据集,研究发现,尽管不同物种器官的绝对光谱特征差异显著,但由病理变化或手术操作引起的相对光谱变化具有高度一致性。通过一种“基于生理机制的数据增强”方法,研究人员成功将动物模型中学习到的光谱变化迁移至人类数据,显著提升了组织分割与状态识别性能,为临床应用释放了大量动物实验数据价值。

在手术过程中,医生需要实时区分健康组织与病变组织,并避免损伤关键结构。然而,传统 RGB 成像系统受限于人眼视觉,仅捕捉红绿蓝三色信息,难以揭示组织的功能状态。
高光谱成像可记录数百个波段的反射信息,为解析组织类型与生理状态提供丰富特征。结合深度学习,该技术已在组织分类与手术导航中显示出巨大潜力。
但现实应用受到严重制约:
- 临床数据规模有限;
- 难以系统获取不同病理状态;
- 受伦理与手术流程限制。
相比之下,动物实验可以在高度可控环境下诱导缺血、灌注异常或造影剂注射等状态,产生丰富高质量数据。
因此,研究人员提出跨物种知识迁移理念,借鉴异种器官移植思想,将动物数据中蕴含的生理变化规律“移植”至人类应用场景。
方法
研究人员构建 Xeno-learning 框架,通过学习病理状态或手术操作引起的相对光谱变化模式,并将这些变化映射至目标物种数据中,形成基于生理机制的数据增强策略。
具体流程包括:从源物种中成对采集生理与异常状态图像,学习光谱转变规律;再将该转变应用于目标物种的生理数据,生成模拟异常状态样本,用于训练深度分割网络。该方法避免直接迁移绝对光谱值,从而绕开不同物种固有生物组成差异带来的干扰。
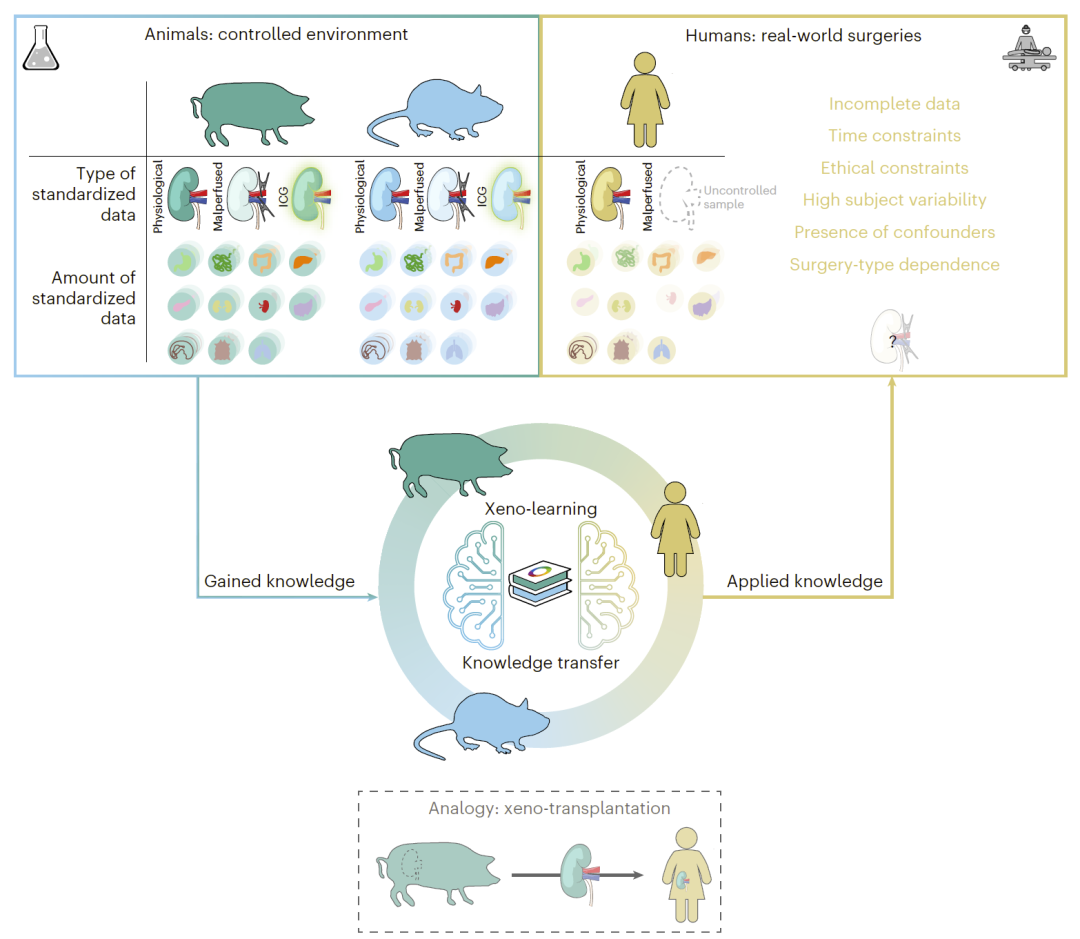
图1|受异种器官移植理念启发,提出跨物种知识迁移的 Xeno-learning 框架。
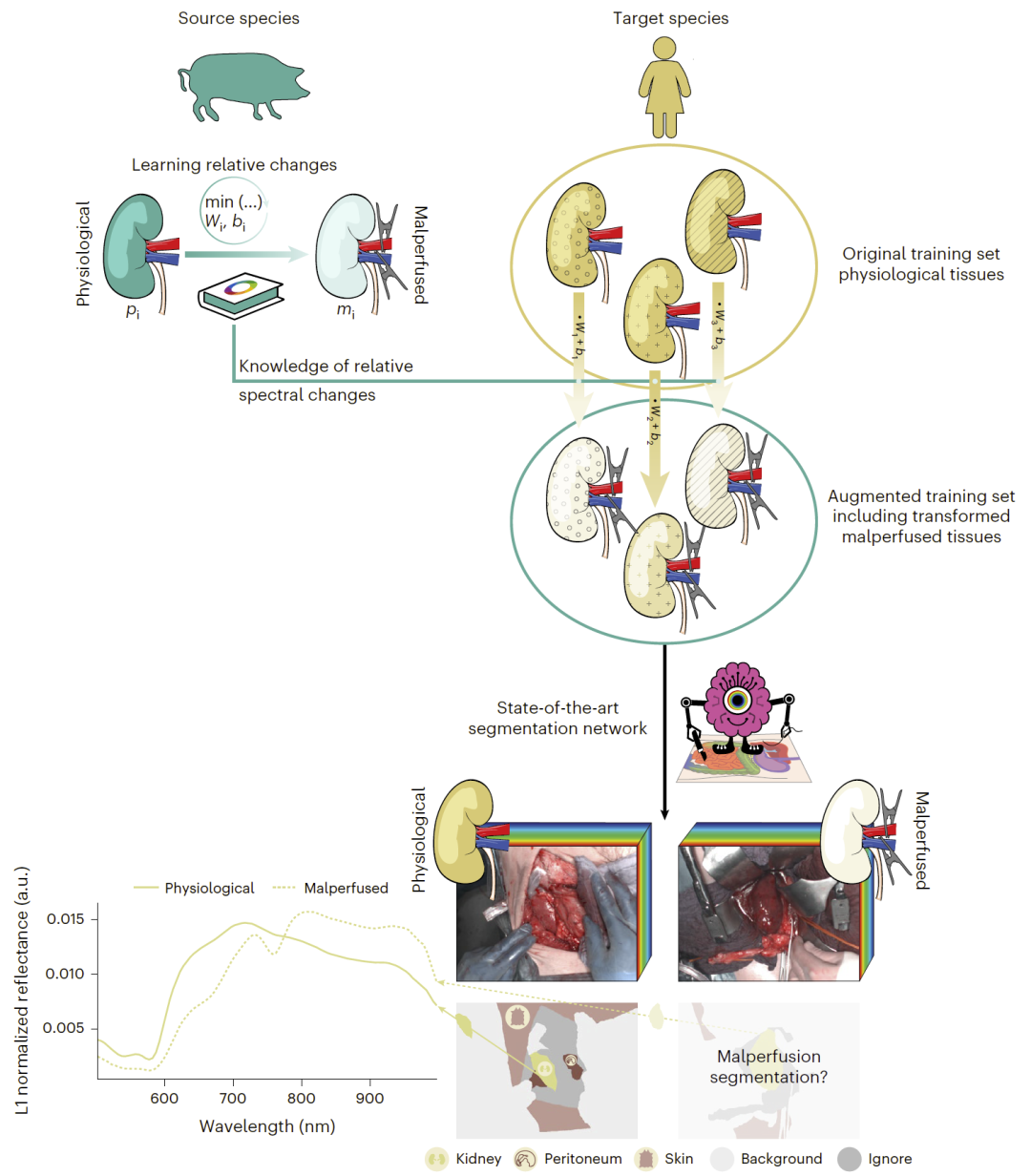
图2|通过基于生理机制的数据增强方法迁移灌注状态变化知识。
结果
不同物种器官光谱特征差异显著
系统分析显示,人类、猪与大鼠的器官光谱“指纹”存在显著差异。神经网络在单一物种上训练表现良好,但在跨物种应用时性能大幅下降,部分任务准确率降低超过 50%。这表明直接跨物种训练或混合训练难以实现有效泛化。
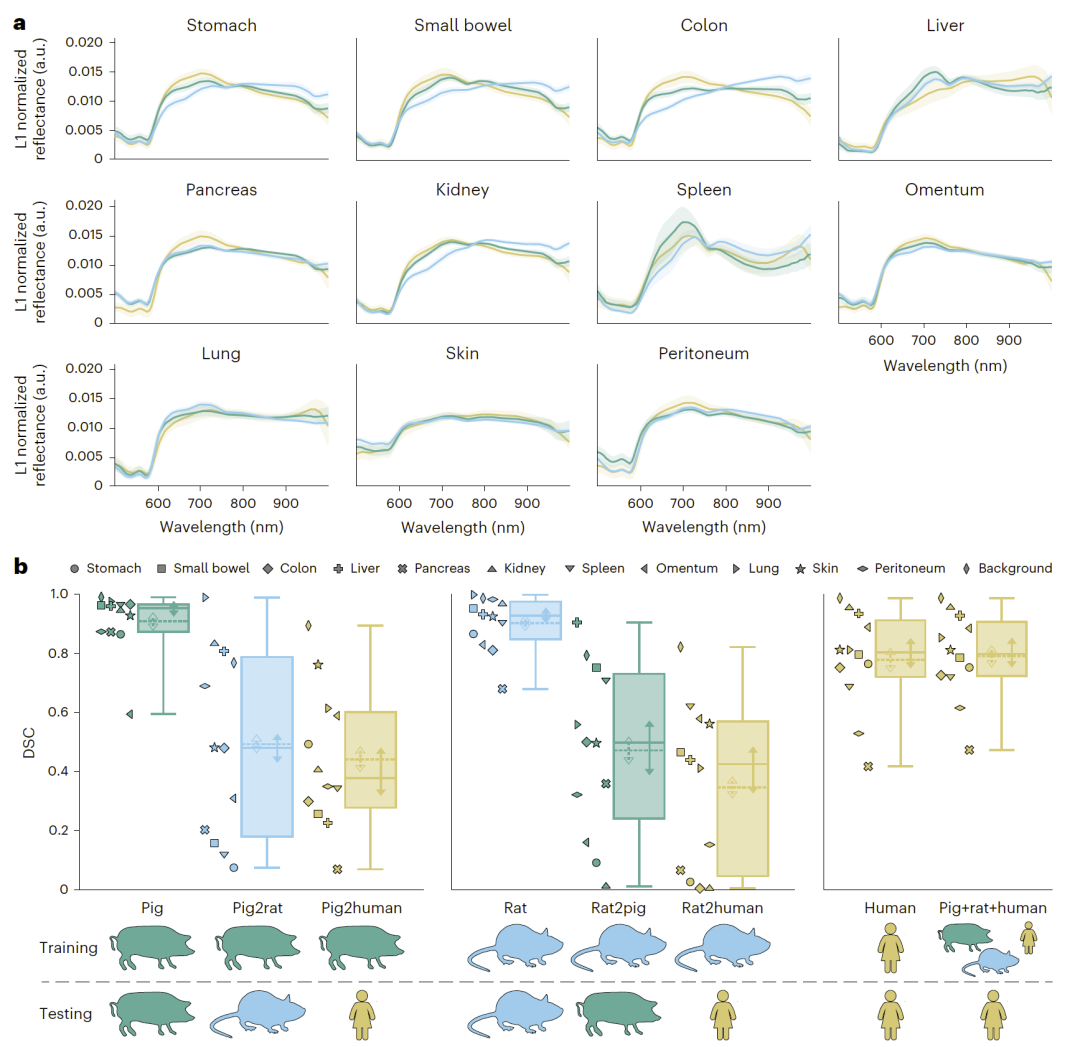
图3|不同物种具有差异显著的器官光谱指纹,导致单一物种训练的分割网络难以泛化至新物种。
绝对光谱差异是跨物种失败的主要原因
方差分解分析表明,物种因素在多个器官和波段上是主要变异来源,远高于成像角度或个体差异。
邻域分析进一步显示,不同物种相同器官的光谱往往更接近其他器官类别,而非自身对应器官。
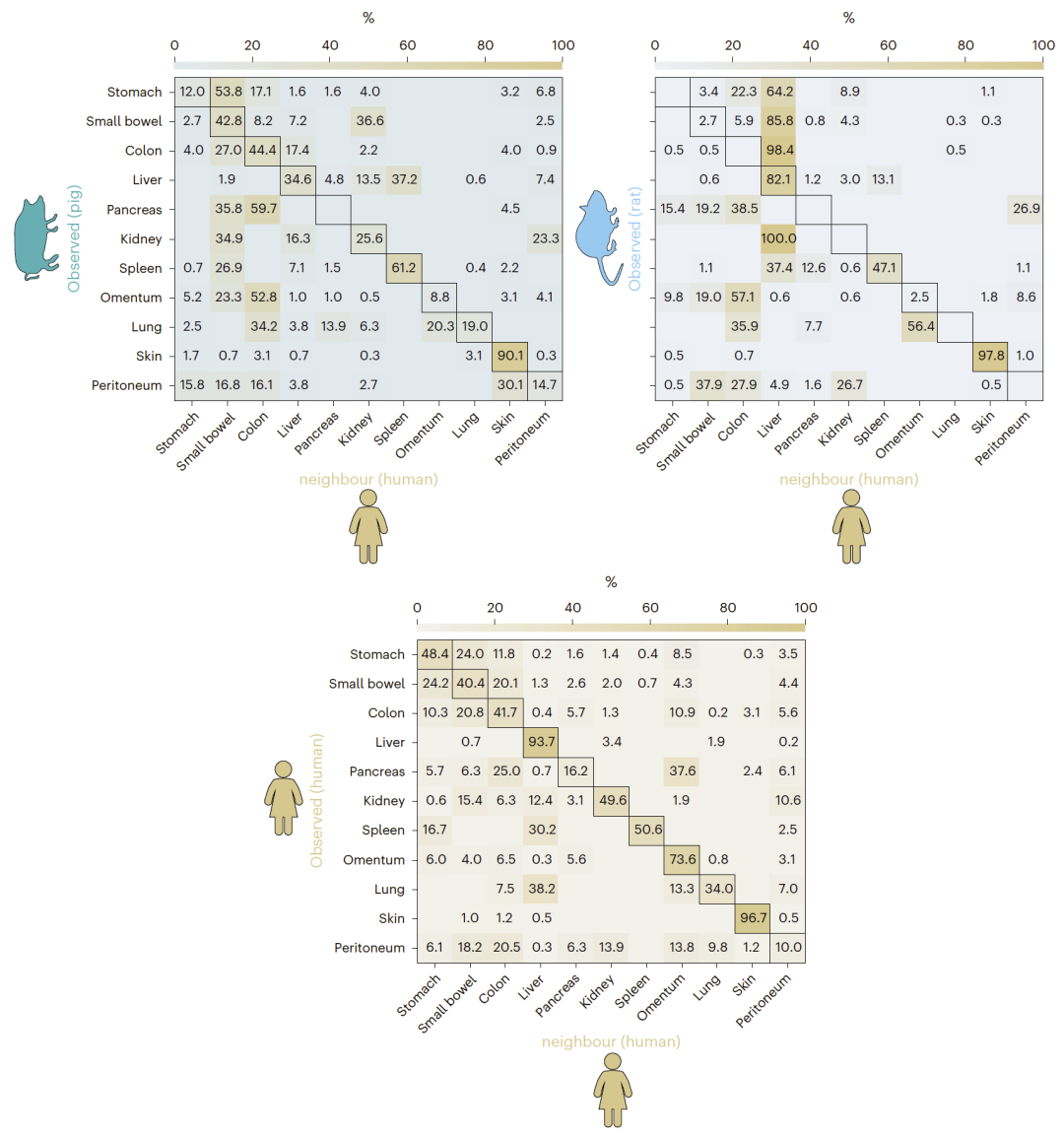
图4|跨物种同类组织光谱并非彼此的最近邻特征。
病理状态引起的相对光谱变化在不同物种中一致
尽管绝对光谱差异明显,但当组织经历缺血或造影剂注射时,光谱变化方向在三种物种中高度一致。
例如,肾脏缺血状态下均出现特定波段反射率系统性下降,并在主成分空间中呈现相似迁移轨迹。
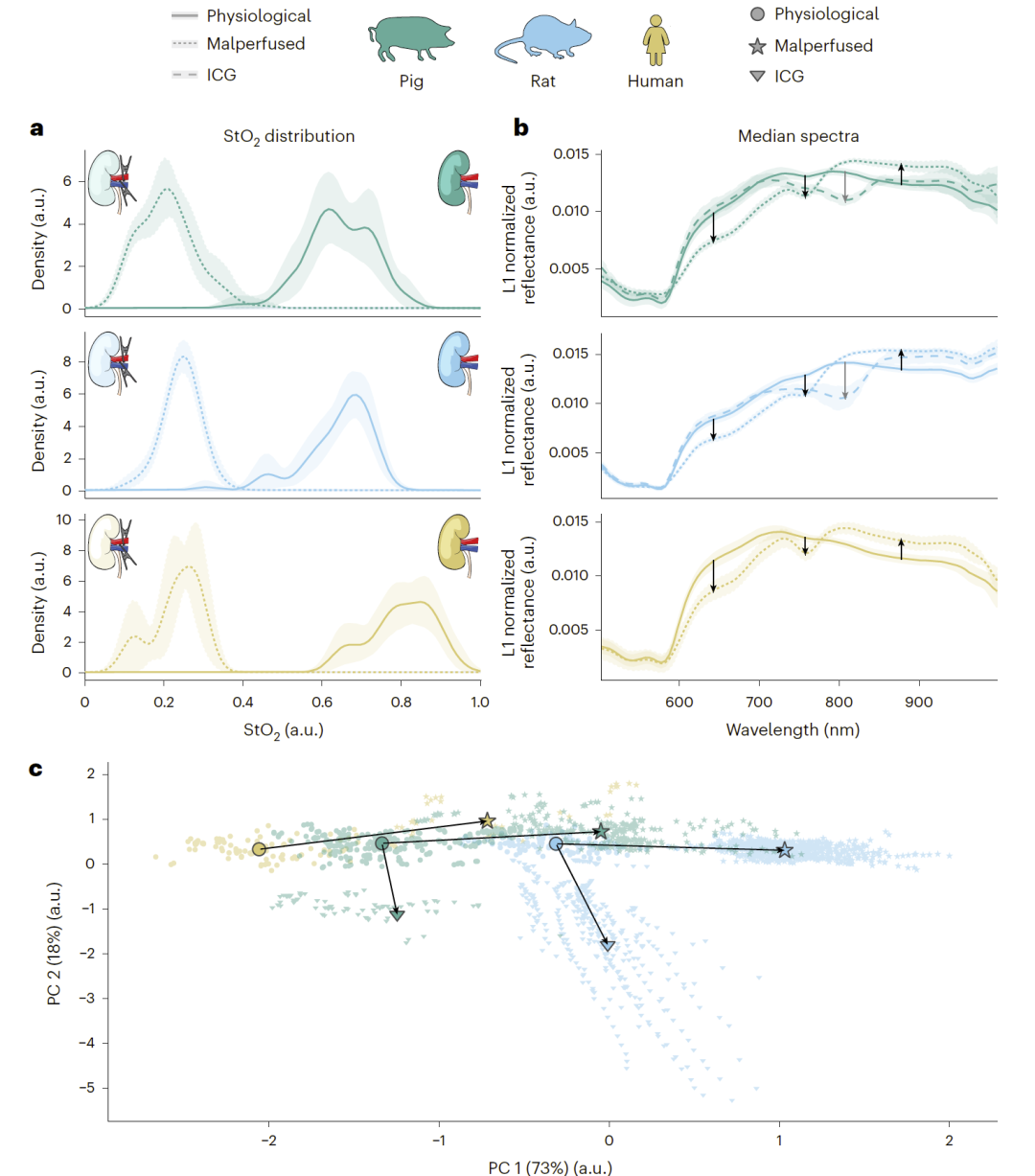
图5|尽管不同物种光谱特征存在差异,病理状态或手术操作仍引发一致性的系统性光谱变化。
Xeno-learning 成功迁移灌注异常知识
利用动物模型学习缺血状态的光谱变化后,研究人员将该变化迁移至人类数据,使深度分割模型在异常组织识别上显著恢复性能。在肾脏分割任务中,模型在低氧状态下准确率大幅提升。
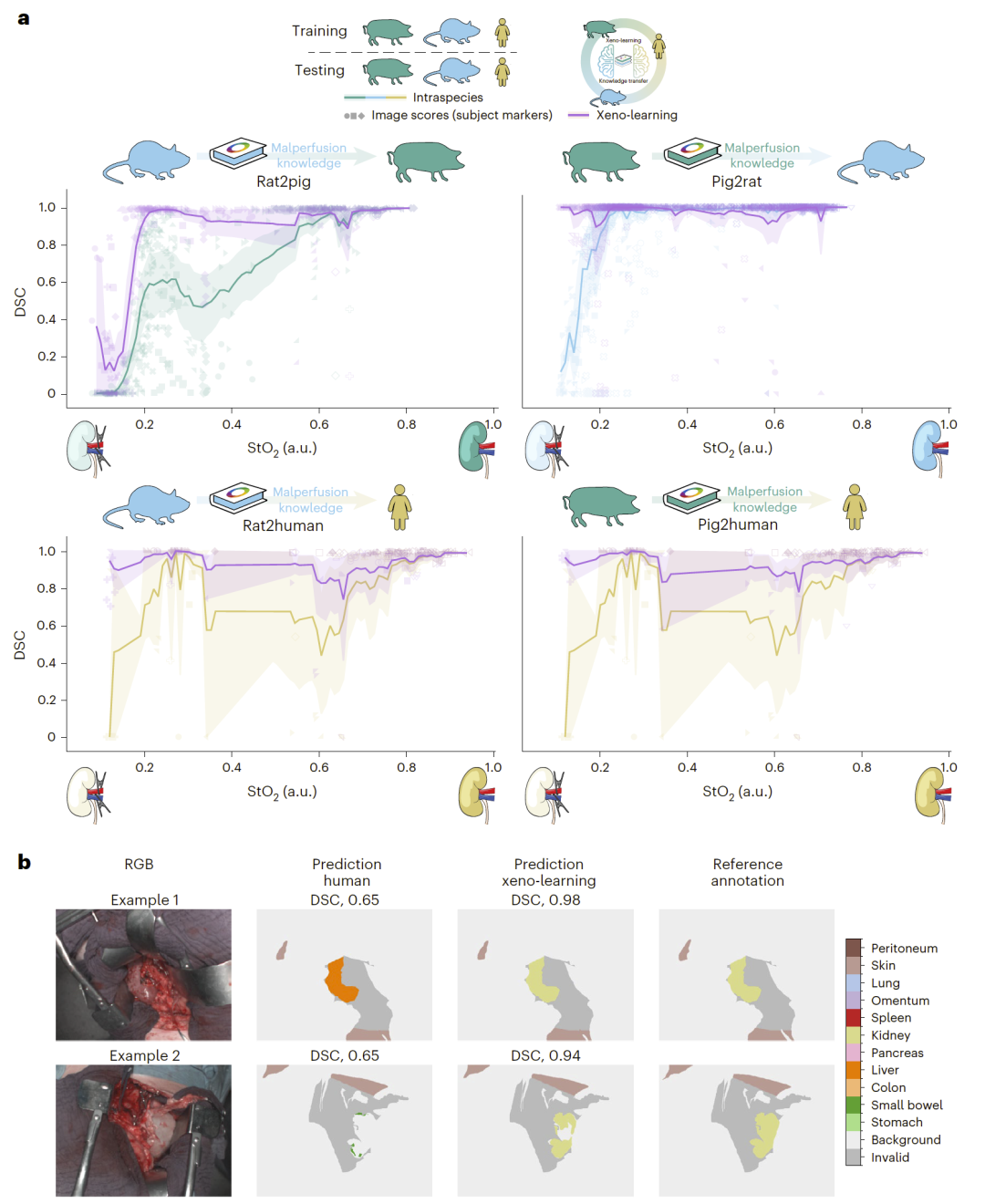
图6|Xeno-learning 实现跨物种知识有效迁移。
数据增强显著扩展训练分布覆盖范围
在主成分空间中,增强后的训练数据成功覆盖原始训练集中缺失的异常状态区域,使模型不再面对“分布外”样本。训练样本与测试样本之间的距离平均降低约 20%–30%。
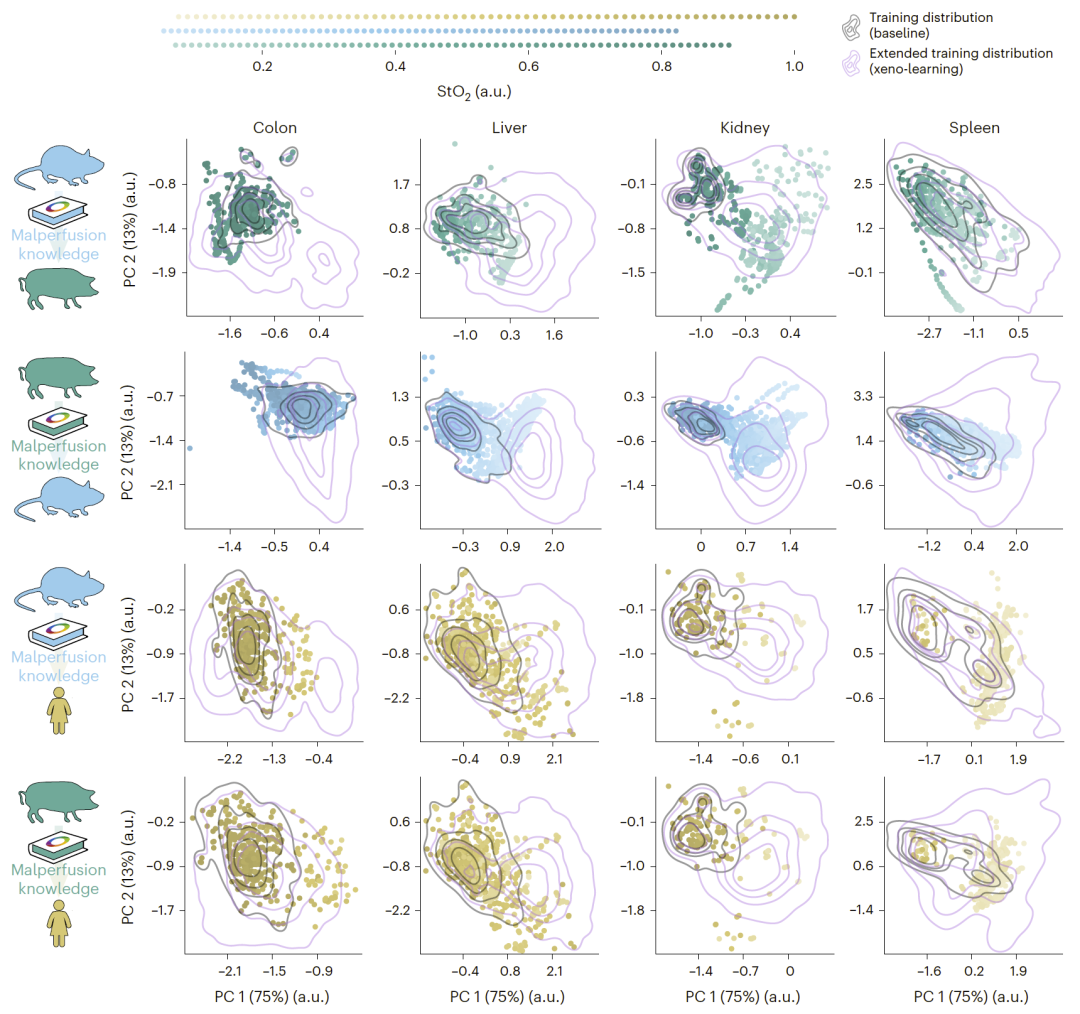
图7|Xeno-learning 扩展训练数据分布以覆盖多器官的广泛灌注状态。
方法可推广至造影剂注射等复杂变化
在另一任务中,研究人员迁移造影剂引起的光谱变化规律,同样成功恢复跨状态分割性能,在多个器官上均实现显著提升。
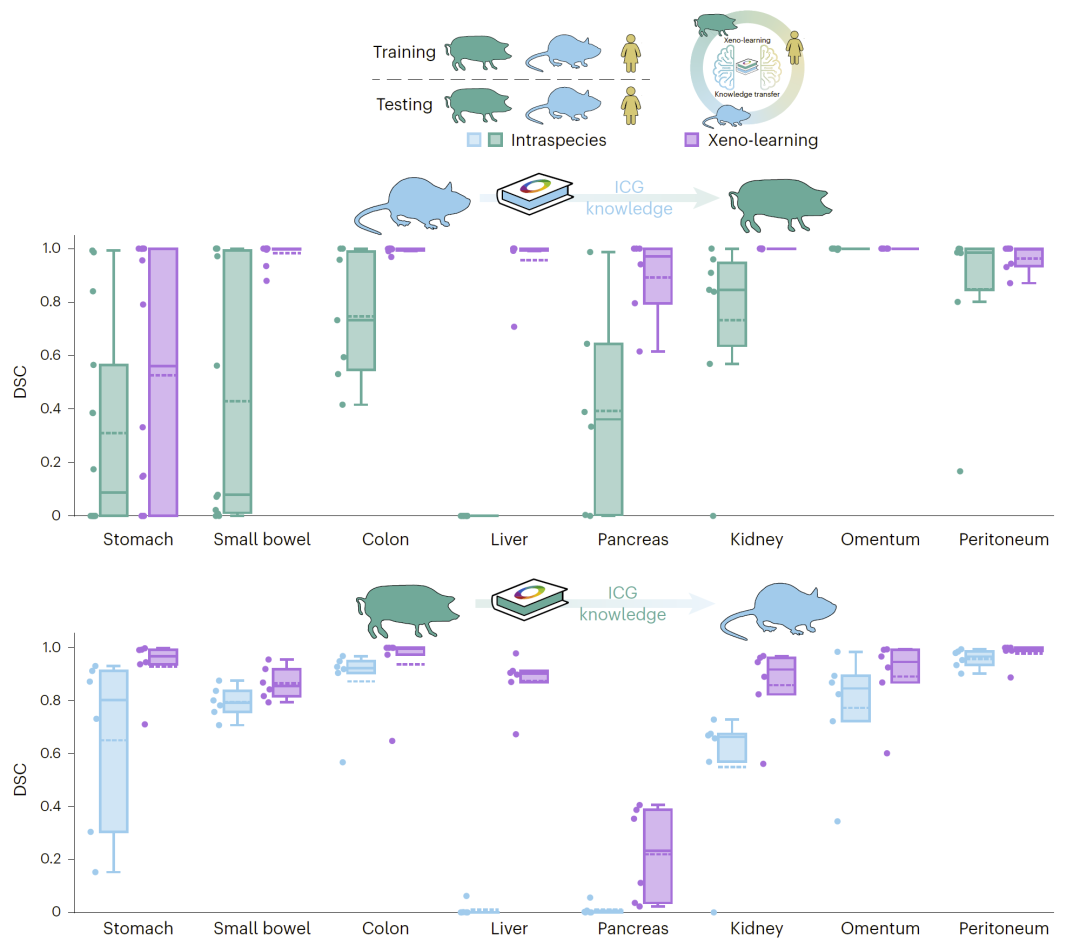
图8|Xeno-learning 在造影剂(ICG)荧光注射后恢复多器官分割性能。
与传统域适应方法相比更稳健
与直接基于光谱值的域适应方法相比,Xeno-learning 仅迁移相对变化规律,避免引入跨物种固有差异,表现更稳定。
大规模动物数据可显著增强临床模型
综合实验显示,通过 Xeno-learning,动物实验数据可作为高价值补充资源,大幅缓解临床数据稀缺问题。
讨论
本研究首次系统性验证了跨物种光谱知识迁移的可行性,并提出 Xeno-learning 作为新型跨域学习范式。
核心发现包括:
- 不同物种器官的绝对光谱特征差异巨大;
- 但病理状态引起的相对变化具有普适生理一致性;
- 基于相对变化迁移可绕开物种差异瓶颈。
该策略不仅显著提升组织分割鲁棒性,也为动物实验数据的大规模再利用提供了新路径。
在临床层面,该方法可加速 AI 成像模型落地,减少对大规模人体标注数据的依赖,同时降低伦理负担与研究成本。
研究人员也指出当前局限,如目前主要使用线性变化模型,尚未涵盖复杂非线性纹理变化,未来可引入更强大的图像到图像转换网络进一步扩展能力。
整理 | DrugOne团队
参考资料
Sellner, J., Studier-Fischer, A., Qasim, A.B. et al. Xeno-learning: knowledge transfer across species in deep learning-based spectral image analysis. Nat. Biomed. Eng (2026).
https://doi.org/10.1038/s41551-025-01585-4
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-01-27,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

