meta分析整合多次差异分析结果
今天是生信星球陪你的第1065天
公众号里的文章大多数需要编程基础,如果因为代码看不懂,而跟不上正文的节奏,可以来找我学习,相当于给自己一个新手保护期。我的课程都是循环开课,点进去咨询微信,随时可以报名↓ 生信分析直播课程(每月初开一期) 生信新手保护学习小组长期报名中(每月一期) 单细胞陪伴学习小组(每月一期)
背景知识
在数据挖掘中,多个数据差异分析之后的联合,有多种方法:
- 简单取交集 (Venn Diagram)
这是最直观的方法。分别对两个数据集做差异分析,然后画 Venn 图取重叠部分。
优点:逻辑简单,读者一看就懂。 缺点:存在严重的**“漏斗效应”**。很多基因可能在一个数据集中显著(P<0.05),在另一个数据集中处于边缘显著(比如 P=0.06),直接取交集会无情地丢弃这些其实很重要的基因。
- 效应量 Meta 分析 (Effect Size Meta-analysis) 这是目前的“黄金标准”。它不是简单的数值平均,而是根据每个研究的标准误 (SE) 进行加权。数据越准、样本量越大的研究,话语权越重。
优点:能综合考虑变化方向、幅度和数据质量,结果最稳健可信,且支持跨平台(芯片+测序)整合。 缺点:需要完整的 logFC 和 SE 数据,门槛稍高。
- 秩聚合算法 (RRA) 这是一种基于“排名”的整合方法。它不看具体的表达量数值,而是看基因在各个列表中是否都排在前列。
优点:容错率极高,能整合量纲完全不同的数据(如转录组+蛋白质组+甲基化)。 缺点:丢失了具体的“倍数变化”信息,无法量化差异幅度。
- 直接合并去批次 (ComBat/SVA) 将两个表达矩阵强行拼合,并使用算法去除批次效应。
适用场景:通常仅限于同平台的数据(如都是 Affymetrix 芯片)。 风险:如果强行合并芯片和测序数据,极易引入非线性偏差;且容易“过度校正”,误把生物学差异当成批次效应抹除。
- Fisher's Method (P值合并) 这是 Meta 分析的简易版,仅针对 P 值进行合并(将多个 P 值融合成一个统计量)。
适用场景:当你只有 Gene Symbol 和 P-value,没有 logFC 时的救命稻草。 硬伤:它分不清方向。如果某基因在一个数据集中上调,在另一个中下调,Fisher 法可能会误判为“显著”,导致假阳性。
- 共识加权基因共表达网络 (Consensus WGCNA) 这是一种进阶策略。它不局限于寻找单个差异基因,而是挖掘在两个数据集中“共存的基因模块”。
价值:如果 TCGA 和 GEO 都能构建出同一个共表达模块,说明该通路在生物学上非常保守且核心,适合讲述更高维度的调控网络故事。
今天介绍这里面的方法2(效应量 Meta 分析)的代码。
1.载入数据
rm(list = ls())
library(dplyr)
library(metafor)
library(ggplot2)
load("degs.Rdata")
head(deg1)
## logFC AveExpr t P.Value adj.P.Val
## Mug2 -3.836029 6.883903 -27.90973 2.676041e-12 2.764409e-08
## Orm2 3.054059 6.040447 24.29455 1.380244e-11 6.244226e-08
## H2-K1 -3.346620 8.882681 -23.16197 2.422945e-11 8.221052e-08
## Gm10260 5.463509 4.118297 26.93697 4.073695e-12 2.764409e-08
## Rps18 -2.921302 7.197548 -21.07808 7.337186e-11 1.492161e-07
## Cd36 4.472500 6.481416 20.99240 7.696087e-11 1.492161e-07
## B change Symbol
## Mug2 18.54363 DOWN Mug2
## Orm2 17.01484 UP Orm2
## H2-K1 16.56112 DOWN H2-K1
## Gm10260 16.45028 UP Gm10260
## Rps18 15.48881 DOWN Rps18
## Cd36 15.39094 UP Cd36
head(deg2)
## logFC AveExpr t P.Value
## 1600002H07Rik -2.520145 6.292221 -18.32099 5.872667e-10
## Cyp3a11 2.321189 11.282366 14.21200 1.008935e-08
## Slc37a4 -1.857103 6.303268 -12.39953 4.520266e-08
## Cdip1 -1.658108 6.411937 -12.35854 4.686372e-08
## Pfkfb1 -1.851370 5.545345 -12.36736 4.650084e-08
## Mgll -1.495570 6.969573 -12.01666 6.358669e-08
## adj.P.Val B change Symbol
## 1600002H07Rik 8.027349e-06 12.798728 DOWN 1600002H07Rik
## Cyp3a11 6.895568e-05 10.406196 UP Cyp3a11
## Slc37a4 9.446013e-05 9.069660 DOWN Slc37a4
## Cdip1 9.446013e-05 9.042104 DOWN Cdip1
## Pfkfb1 9.446013e-05 8.997119 DOWN Pfkfb1
## Mgll 1.045003e-04 8.765187 DOWN Mgll
我的两个数据实验设计相同,物种相同,都用了limma包做差异分析,deg1和deg2是两个数据各自差异分析的结果表格。如果是多次差异分析,也同样支持,准备多次差异分析的结果,然后后续代码rma的method参数从FE改为REML即可。
2.数据清洗
1.两个差异分析结果都需要有Symbol、logFC和SE(标准误)列。
差异分析常用的三大R包中,deseq2直接提供了SE值,即lfcSE 列。
limma的差异分析结果中没有提供SE值,可以使用SE = |logFC| / t计算。edgeR或者t-test也没有提供SE值,但提供了p值和logFC,也可以计算SE。
edgeR的SE计算示例代码(不运行):
DEG2 <- DEG2 %>%
mutate(Symbol = rownames(.)) %>%
mutate(
# 1. 计算 Z 分数
Z_score = qnorm(1 - (PValue / 2)),
# 2. 反推 SE
SE = abs(logFC) / Z_score
)
2.列名修改,避免多个数据相同的信息列名混乱。
3.剔除基因名NA、重复以及无穷值,防止因异常数据而报错。
4.两个差异分析结果数据取交集。
deg1 <- deg1 %>%
transmute(
Symbol,
logFC_dat1 = logFC,
SE_dat1 = abs(logFC / t),
P_dat1 = P.Value
) %>%
filter(!is.na(Symbol)) %>%
distinct(Symbol, .keep_all = TRUE) %>%
filter(is.finite(logFC_dat1), is.finite(SE_dat1), SE_dat1 > 0)
deg2 <- deg2 %>%
transmute(
Symbol,
logFC_dat2 = logFC,
SE_dat2 = abs(logFC / t),
P_dat2 = P.Value
) %>%
filter(!is.na(Symbol)) %>%
distinct(Symbol, .keep_all = TRUE) %>%
filter(is.finite(logFC_dat2), is.finite(SE_dat2), SE_dat2 > 0)
dat <- inner_join(deg1, deg2, by = "Symbol")
head(dat)
## Symbol logFC_dat1 SE_dat1 P_dat1 logFC_dat2 SE_dat2
## 1 Mug2 -3.836029 0.1374442 2.676041e-12 0.49740075 0.2591405
## 2 Orm2 3.054059 0.1257096 1.380244e-11 1.17220273 0.4348370
## 3 H2-K1 -3.346620 0.1444877 2.422945e-11 -0.09312900 0.1379991
## 4 Gm10260 5.463509 0.2028257 4.073695e-12 -0.02046381 0.4529364
## 5 Rps18 -2.921302 0.1385943 7.337186e-11 0.31219117 0.1859874
## 6 Cd36 4.472500 0.2130533 7.696087e-11 0.40889796 0.3730486
## P_dat2
## 1 0.07971635
## 2 0.01988533
## 3 0.51292278
## 4 0.96472774
## 5 0.11979833
## 6 0.29514775
3.执行meta分析
在 Meta 分析中,通常有固定效应(FE)和随机效应(REML)两种模型。两研究使用固定效应 FE,三个及以上研究选择随机效应(REML)。因为只有两个数据时,异质性估计极不稳定,固定效应(FE)模型反而是更稳健、更敏感的选择。
针对上述数据的每一行,定义计算函数。
run_meta_per_gene <- function(row_data) {
yi <- c(as.numeric(row_data["logFC_dat1"]), as.numeric(row_data["logFC_dat2"]))
sei <- c(as.numeric(row_data["SE_dat1"]), as.numeric(row_data["SE_dat2"]))
# 排除异常值
if (any(!is.finite(yi)) || any(!is.finite(sei)) || any(sei <= 0)) {
return(c(NA_real_, NA_real_))
}
vi <- sei^2
res <- tryCatch(
rma(yi = yi, vi = vi, method = "FE"), # 固定效应
error = function(e) NULL
)
if (is.null(res)) return(c(NA_real_, NA_real_))
c(as.numeric(res$beta), as.numeric(res$pval))
}
# 批量运行
res <- apply(dat, 1, run_meta_per_gene)
res <- as.data.frame(t(res))
colnames(res) <- c("Pooled_ES", "Meta_Pval")
head(res)
## Pooled_ES Meta_Pval
## 1 -2.884635 9.304021e-125
## 2 2.908911 3.380353e-128
## 3 -1.645183 4.656462e-61
## 4 4.547510 2.909540e-133
## 5 -1.766831 6.490362e-57
## 6 3.473059 1.266056e-78
Pooled_ES即Pooled Effect Size,合并效应值,是加权后的共识 logFC,它是两个数据集中 logFC 的综合结论。
Pooled Effect Size不是简单的 (dat1 + dat2) / 2。 它是基于数据质量的“加权平均值”。
Meta 分析算法会根据每个研究的标准误 (SE) 自动分配话语权: SE 越小,说明该研究数据越稳、精度越高,它在合并时的权重(Weight)就越大。 SE 越大,说明数据波动大、噪音多,它的权重就越小。
举个例子: dat1 (SE极小) 显示:某基因下调 4倍。 dat2 (SE较大) 显示:该基因下调 2倍。 最终结果:Pooled ES 可能是 3.5倍。 (结果会强烈向更靠谱的 dat1 倾斜,而不是简单的中间值 3)。
4.meta分析结果整理
res <- bind_cols(dat, res) %>%
mutate(
FDR = p.adjust(Meta_Pval, method = "BH")
) %>%
filter(is.finite(Pooled_ES), is.finite(Meta_Pval), is.finite(FDR)) %>%
# 防止FDR极小被数值舍入到0,导致 -log10(FDR) = Inf
mutate(FDR_plot = pmax(FDR, 1e-300))
head(res)
## Symbol logFC_dat1 SE_dat1 P_dat1 logFC_dat2 SE_dat2
## 1 Mug2 -3.836029 0.1374442 2.676041e-12 0.49740075 0.2591405
## 2 Orm2 3.054059 0.1257096 1.380244e-11 1.17220273 0.4348370
## 3 H2-K1 -3.346620 0.1444877 2.422945e-11 -0.09312900 0.1379991
## 4 Gm10260 5.463509 0.2028257 4.073695e-12 -0.02046381 0.4529364
## 5 Rps18 -2.921302 0.1385943 7.337186e-11 0.31219117 0.1859874
## 6 Cd36 4.472500 0.2130533 7.696087e-11 0.40889796 0.3730486
## P_dat2 Pooled_ES Meta_Pval FDR FDR_plot
## 1 0.07971635 -2.884635 9.304021e-125 2.998918e-121 2.998918e-121
## 2 0.01988533 2.908911 3.380353e-128 1.452763e-124 1.452763e-124
## 3 0.51292278 -1.645183 4.656462e-61 6.670641e-58 6.670641e-58
## 4 0.96472774 4.547510 2.909540e-133 1.875635e-129 1.875635e-129
## 5 0.11979833 -1.766831 6.490362e-57 7.607294e-54 7.607294e-54
## 6 0.29514775 3.473059 1.266056e-78 2.720544e-75 2.720544e-75
5.绘制火山图
cutoff_fdr <- 0.05
cutoff_es <- 0.585 # 约等于1.5倍
res <- res %>%
mutate(
group = case_when(
FDR < cutoff_fdr & Pooled_ES > cutoff_es ~ "Up",
FDR < cutoff_fdr & Pooled_ES < -cutoff_es ~ "Down",
TRUE ~ "Stable"
)
)
table(res$group)
##
## Down Stable Up
## 1043 10737 1113
my_colors <- c("Up" = "#D53E4F", "Down" = "#3288BD", "Stable" = "grey80")
p <- ggplot(res, aes(x = Pooled_ES, y = -log10(FDR_plot))) +
geom_point(
data = subset(res, group == "Stable"),
color = "grey80", size = 1, alpha = 0.5
) +
geom_point(
data = subset(res, group != "Stable"),
aes(color = group, size = -log10(FDR_plot)),
alpha = 0.8
) +
scale_color_manual(values = my_colors) +
scale_size_continuous(range = c(1, 4), guide = "none") +
geom_vline(xintercept = c(-cutoff_es, cutoff_es), linetype = "dashed") +
geom_hline(yintercept = -log10(cutoff_fdr), linetype = "dashed") +
labs(
x = "Pooled Effect Size",
y = "-log10(FDR)",
title = "Meta-analysis Volcano Plot"
) +
theme_bw() +
theme(
panel.grid = element_blank(),
legend.position = "none",
axis.title = element_text(size = 14),
axis.text = element_text(size = 12),
plot.title = element_text(hjust = 0.5)
)
p
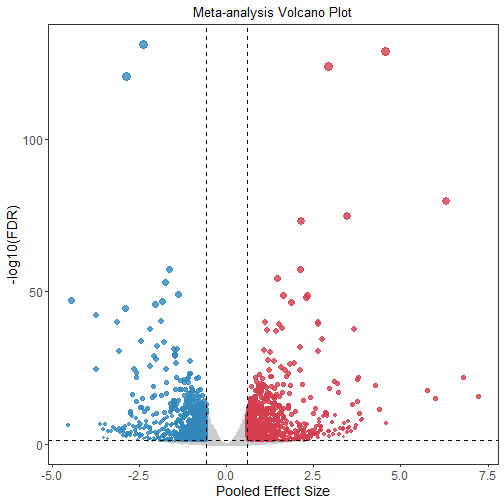
在 Meta 分析的火山图中,横坐标不是单一研究的 logFC,而是综合计算出的 Pooled ES:
Pooled ES > 0 (右侧): 综合所有证据后,判定该基因在处理组整体上调。例如 Pooled ES = 2,意味着综合来看表达量约升高了 2^2=4 倍。 Pooled ES < 0 (左侧): 综合判定该基因整体下调。 Pooled ES ≈ 0 (中间): 基因无明显变化,或者两个数据集结论严重冲突(一个极高、一个极低,导致互相抵消)。
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2026-01-26,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录


