基于表型的药物发现(PDD):重回视野的创新之路
基于表型的药物发现(PDD):重回视野的创新之路

MindDance
发布于 2026-01-08 12:50:17
发布于 2026-01-08 12:50:17
引言
1928年,微生物学家弗莱明偶然发现培养皿中的青霉菌使邻近细菌死亡,由此诞生了抗生素青霉素。上世纪60年代末,在抗疟战争陷入僵局时,中国科学家屠呦呦从几千种中草药中筛选出黄花蒿提取物,最终分离出高效抗疟的新药青蒿素。这些经典故事都源自同一种策略:基于表型的药物发现(Phenotypic Drug Discovery, PDD)。简单来说,就是先观察药物对生物表型的影响,再找到其中潜藏的疗效,而无需一开始就瞄准具体的分子靶点。令人意想不到的是,这种带有“经验主义”色彩的老方法在现代医药研发中正焕发新生——许多制药人士惊奇地发现,1999年至2008年FDA批准的大多数“头创”(first-in-class)新药,竟是在没有预设明确靶点的情况下凭借表型筛选发现的!PDD仿佛一位隐退的老前辈,在基因组时代又重新走上前台,引发业界的极大关注。

表型药物发现谱 <ins><a href='https://doi.org/10.1038/s41573-022-00472-w'>图片来源</a></ins>
表型药物发现谱 图片来源
从“靶向”回归“表型”
什么是表型药物发现?简而言之,PDD是一种“靶点不可知”的药物研发途径:研究者让成千上万的候选化合物作用于细胞、组织甚至整动物模型,直接观察是否能产生预期的表型变化(例如杀死癌细胞、让病变细胞恢复功能等),以此筛选出有疗效的候选药物。这一过程不需要预先知道药物作用于哪个具体蛋白,完全以生物效果为导向。这与过去几十年主导药物研发的基于靶点的药物发现(Target-Based Drug Discovery, TDD)形成鲜明对比:TDD要求先确定一个与疾病相关的分子靶点,然后设计并筛选能够与该靶点结合的化合物。简而言之,TDD像是靶向狙击,而PDD更像海底捞针——前者有明确的瞄准目标,后者则在复杂生物体系中寻找能够带来有益效应的“意外之喜”。
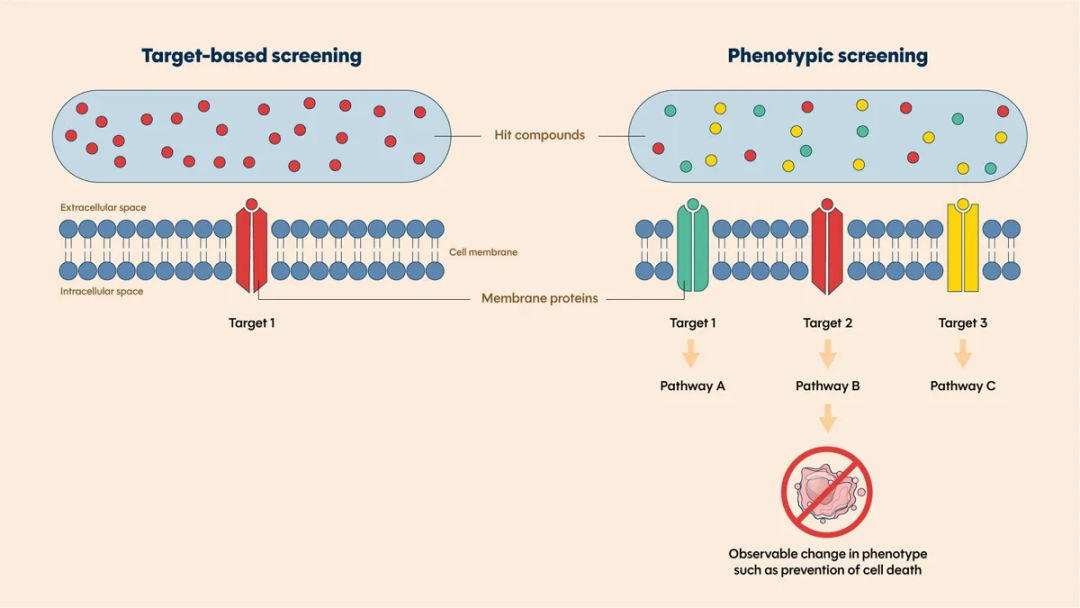
表型筛选可识别出能够诱导细胞或生理表型变化的活性化合物。通过采用更广泛的靶点空间,研究人员可以在不预先了解这些靶点的情况下,研究药物对复杂生物系统的影响。 <ins>图片来源: https://www.technologynetworks.com/drug-discovery/articles/phenotypic-screening-a-powerful-tool-for-drug-discovery-398572</ins>
表型筛选可识别出能够诱导细胞或生理表型变化的活性化合物。通过采用更广泛的靶点空间,研究人员可以在不预先了解这些靶点的情况下,研究药物对复杂生物系统的影响。 图片来源: https://www.technologynetworks.com/drug-discovery/articles/phenotypic-screening-a-powerful-tool-for-drug-discovery-398572
表型筛选可识别出能够诱导细胞或生理表型变化的活性化合物。通过采用更广泛的靶点空间,研究人员可以在不预先了解这些靶点的情况下,研究药物对复杂生物系统的影响。 图片来源: https://www.technologynetworks.com/drug-discovery/articles/phenotypic-screening-a-powerful-tool-for-drug-discovery-398572
这种“表型先行”的思路并不新鲜。事实上,在分子生物学兴起之前的漫长时期,药物发现主要都是依赖表型筛选和经验积累。许多经典药物,例如抗生素、抗癌药、免疫抑制剂等,都是通过对生物模型的实证筛选获得的。进入20世纪后期,随着分子生物学革命和人类基因组计划的推进,制药行业一度全面转向TDD路径:科研人员醉心于基因和蛋白,致力于“按图索骥”地研发针对特定靶标的药物。这种方法论曾造就了许多靶向药物的成功,比如针对EGFR突变的抗癌药、针对特定受体的降压药等等。然而,TDD的局限也逐渐显露:精确命中靶点并不保证治愈疾病,因为疾病生理过程远比单一靶点复杂。不少设计完美的靶向药在临床试验中折戟,就是因为抑制了某个机制却无法改善整体病情。
在这种背景下,PDD近十年来重新进入人们的视野。业界开始反思:也许绕开那些我们自以为了解的通路,转而直接向生物系统发问,让细胞或模型动物自己“告诉”我们什么化合物有效,反而能发现一些意料之外的疗法。2011年的一项分析引起轰动:1999–2008年间FDA批准的新药中,多数头创药源自表型筛选,而非预先设定靶点。这相当于给沉寂多年的PDD打了一剂强心针。随之而来的,是大型药企和科研机构对PDD的重新投入:从建立大型表型筛选平台,到资助相关基础研究,PDD正迎来自己的“二次崛起”。
表型筛选如何进行?
PDD的流程可以概括为三个阶段:表型筛选、先导化合物优化、机制研究。首先,研究者需要设计或选取合适的疾病模型和表型读数。这可能是在体外培养的细胞(例如疾病相关细胞系、干细胞分化的特定细胞等),也可能是模式生物(如秀丽线虫、斑马鱼、小鼠的疾病模型)甚至是患者来源的类器官。关键是要找到能够体现疾病状态的“表型指标”,比如细胞存活率、形态变化、某种生理功能的恢复等。接下来,将一个大型化合物库(动辄几十万种化合物)作用于模型进行高通量筛选,凭直觉看疗效:哪些处理能够纠正模型的异常表型?通过自动成像、机器学习分析等技术,科研人员从海量实验中挑选出能“改命”的化合物。这些命中化合物(hits)就是潜在的先导药物。
筛选出的先导化合物往往需要进一步优化其结构以提高活性、降低毒性,转变为可成药的分子。在此过程中,PDD的一大挑战也随之出现:靶点鉴定(Target Deconvolution)。与TDD从靶点出发正好相反,PDD拿到的是“有效但机理不详”的化合物——我们必须倒过来弄清它到底作用于生物体的哪个环节。靶点鉴定的方法很多,包括化学蛋白质组学(用改造过的化合物捕获结合蛋白)、基因组学筛选(比如利用CRISPR敲除库寻找影响药物作用的基因)、转录组分析(观察药物引起的基因表达改变来推测作用途径)等。这一过程好比给神秘钥匙匹配锁孔,虽然困难,却至关重要:了解靶点和作用机制(MoA)有助于优化药物和预判安全性。值得庆幸的是,现代技术提供了许多利器,如蛋白质相互作用图谱、机器学习预测等,使靶点鉴定的效率大大提高。当然,也有观点认为,即使不明确靶点,只要药有效也未尝不可先推进临床,但长远来看机制研究仍是新药开发不可或缺的一环。
PDD与传统TDD的区别
研发思维上的差异决定了PDD和TDD各自的优劣势。TDD就像精确制导:从病理机制中选定一个“看上去很关键”的靶点,例如某致病蛋白或受体,然后围绕它量身定制药物。这种方法机制清晰,药物作用靶点明确,可以通过结构生物学设计高选择性的分子。然而,TDD过于依赖现有的生物学知识——所见即所得,所不见即所失。换言之,TDD倾向于在熟悉的轨道上创新,对于未知的机制或非经典靶点可能束手无策。如果科研人员对疾病机理的认识有偏差,TDD就可能南辕北辙:精确击中靶标却无法解决疾病,因为也许选错了“靶”。
相比之下,PDD更像黑箱探索:不预设假说,直接观察药物能否带来有益的表型结果。它避免了研究者的偏见,因此有潜力发现全新机制的治疗策略。特别是针对那些发病机制复杂或未知的疾病,PDD提供了一条从表观现象入手的捷径——只要能改善患者细胞或动物模型的状态,就可能找到突破口。这也是为何PDD被认为有利于发现“头创”新药,即作用机制全新的一类疗法。从统计上看,PDD产出的新药中首创机制者居多,因为它不受限于传统靶点的框框。
二者的区别还体现在实验手段上。TDD通常依赖生物化学/生物物理方法(例如高通量筛选一个蛋白-配体结合的活性),指标单一且可量化,筛选体系相对简单。而PDD往往需要复杂的生物学模型,比如活细胞成像、多参数读出等,数据更加复杂。以往PDD常被诟病筛选过程费时费力,但时代在改变:高内容筛选(High-Content Screening)技术结合自动显微成像与图像分析,已经可以在细胞水平上同时观测数十种表型特征;再配合AI对海量影像数据的解析,“不借助靶点的药物筛选”正变得前所未有的高效。可以说,新科技正帮助PDD缩小与TDD在效率上的差距,让两种方法有机会在更公平的条件下各展所长。
优势与挑战
PDD的主要优势在于它的生物学相关性和创新潜力。因为直接在细胞或疾病模型上看疗效,PDD筛选出来的化合物更有可能在真实生物体内奏效,减少了“纸上谈兵”的成分。这种方法尤其擅长捕捉意外之喜:许多PDD发现的药物作用机制在一开始完全出人意料。例如,强力抗癌药来那度胺(Lenalidomide)是从反常的免疫抑制剂沙利度胺入手,通过表型优化得到的,它被FDA批准多年后其真正靶点——E3泛素连接酶复合物的一种蛋白Cereblon——才被揭示。又比如,针对囊性纤维化的突破疗法,科学家采用携带基因缺陷的细胞进行表型筛选,找到了一系列改善离子通道功能的分子(如Ivacaftor、Lumacaftor等),填补了传统方法未能解决的空白。这些案例证明,PDD能够打开“可药靶点空间”的天花板:不局限于教科书上的那些经典靶点,它能捕获全新的生物过程和通路,发掘“暗生物质”中的治疗机会。对于病因未明的疑难疾病而言,PDD提供了宝贵的新思路。
当然,PDD并非完美无缺。首先,正如前文所述的靶点鉴定难题,这是PDD最大的技术门槛之一。找到药有效容易,搞清为何有效却很难——这在一定程度上延缓了药物优化和机制研究的进程。不过随着各种组学和数据驱动方法的发展,这一困境正在缓解。其次,表型筛选对模型的依赖性很大:筛选结果能否转化成临床疗效,取决于所选模型是否真正反映了人类疾病。设计一个可靠的表型模型本身需要深厚的生物学知识和巧思。如果模型失准,可能筛出“假阳性”甚至南辕北辙的化合物。而且高等级的模型(例如动物模型、类器官)往往筛选 throughput 较低、成本高昂,这对资源也是不小的考验。再次,数据复杂性和解析难度也是挑战:PDD产生的是多维度生物数据,如何从中提炼出有意义的信号、区分真正有效的化合物,对于数据分析和统计方法提出了更高要求。此外,PDD筛出的药物常常作用于多个靶点(多重药理),这把“双刃剑”一方面可能带来协同疗效,另一方面也增加了潜在副作用的风险,需要在药理和安全性上权衡取舍。
总的来说,PDD的优势在于“拓宽可能性”,挑战在于“驾驭复杂性”。正因如此,现代新药研发中,PDD和TDD的融合逐渐成为趋势:先用PDD在生物模型中掘金,找到意想不到的新机制苗头,再用TDD和化学优化手段精雕细琢,将其打造成性能优良的药物。这种取长补短的策略有望大幅提高研发效率。毕竟,无论路径如何,目标都是找到真正有疗效的新药,而科学的魅力恰在于不拘一格。
经典案例与最新进展
回顾药物研发史,基于表型筛选的成功案例不胜枚举,从古老的民间草药到现代高科技平台都留下了PDD的印记。在历史长河中,除了前面提到的青霉素和青蒿素,胰岛素的发现(班廷通过动物实验验证胰腺提取物降糖)、肾上腺素的发现(早期科学家通过生理实验提取副肾髓质物质)等,也都带有明显的表型筛选色彩。进入现代,PDD依然战功赫赫。例如,利司扑兰(Risdiplam)和布那PLA姆(Branaplam)这两款治疗脊髓性肌萎缩症(SMA)的口服小分子,就是通过表型筛选发现的RNA剪接调节剂,能够提高缺陷基因的功能蛋白产量,从而改变疾病进程。它们填补了这一致命遗传病长期无药可医的空白,于近年来相继获批上市,造福患者。再比如,抗疟新药KAF156(Ganaplacide)是诺华等机构通过大规模表型筛选发现的全新抗疟化合物。它作用机制独特,对耐药疟原虫依然有效,目前已进入临床试验后期,有望成为青蒿素之后抗疟领域的又一利器。
值得一提的是,一些新兴技术和创业公司正推动PDD进入崭新的阶段。例如,美国初创公司Recursion Pharmaceuticals开创了将高通量成像技术“Cell Painting”与深度学习相结合的药物筛选模式。他们让细胞在显微镜下接受不同化合物处理,拍摄下数以千万计的细胞图像,用AI提取细胞形态学特征,从中发现潜在药物线索。这一策略已经使Recursion发现了多种在研药物,并与多家制药巨头达成合作。又如一些企业利用类器官(Organoids)和3D细胞培养构建更逼真的人体疾病模型,用来进行表型筛选,提高命中化合物的有效性。同时,多组学数据和大规模患者数据库也被引入PDD:研究者通过分析真实世界患者的基因、转录、代谢等数据,提炼出新的疾病表型指标,从而设计出更有预测力的筛选模型。这些前沿进展表明,PDD正在融合人工智能、生物工程等多学科成果,不断升级迭代。
在学术研究方面,权威期刊也频频发声,为PDD站台背书。《自然·评论药物发现》 在2022年发表长文总结PDD的成功经验和未来方向,指出 PDD策略已经成为提供首创药物的重要途径,并详细讨论了如何克服PDD面临的种种挑战。另一篇发表于 《Drug Discovery Today》 的综述则强调了PDD与机器学习结合的前景,预言智能技术将大幅提高表型筛选的数据处理能力,帮助发现过去被忽视的药物作用模式。可以预见,PDD的研究热点将越来越多地集中在新技术驱动下的效率提升、以及在更复杂疾病模型上的应用拓展。从业者也需要不断更新技能树,在生物学与数据科学的交叉地带游刃有余。
结语:发人深思的观点
当今的药物发现领域,有人比喻PDD是“返璞归真”——回到观察生物本身的疗效这一直觉起点;也有人称PDD是“曲径通幽”——绕过了我们对分子机制的成见,走一条发现新颖疗法的幽径。无论哪种比喻,事实是PDD正在为药物创新注入活力,让我们得以触及过去未曾涉足的“暗生物学”领域。这并不意味着靶向药物时代的终结,恰恰相反,未来最理想的模式或许是表型与靶点导向的融合:先通过表型筛选找到潜在突破口,再用分子生物学手段解析和优化。正如Nature文章所言,当疾病机理不明时,PDD提供了一条新路径;而要将这条路径走通并大规模应用,还需解决工业化的挑战,比如建立更高效的表型筛选平台。令人欣慰的是,人工智能等新技术正在为此赋能,将两种方法论巧妙地衔接起来,为更加高效的药物发现铺平道路。
回望历史,很多重大医学突破源自科学家敏锐的观察和大胆的尝试——这是PDD精神的最佳写照。当下,我们有前所未有的工具和知识,能够以更加系统和理性的方式实践这种精神。对于科研人员来说,基于表型的药物发现并非倒退,恰恰是一种前进:它提醒我们始终以患者的生命表现为中心,去发现和创造治愈疾病的新方法。在靶点理性与表型经验的交汇点上,也许正孕育着下一代“重磅药物”的诞生。让我们拭目以待,这场表型驱动的创新之旅将把人类医药带向何方。
参考资料:
[1] Vincent, F., Nueda, A., Lee, J. et al. Phenotypic drug discovery: recent successes, lessons learned and new directions. Nat Rev Drug Discov 21, 899–914 (2022). https://doi.org/10.1038/s41573-022-00472-w [2] https://www.technologynetworks.com/drug-discovery/articles/phenotypic-screening-a-powerful-tool-for-drug-discovery-398572 [3] https://www.cn-healthcare.com/articlewm/20220910/content-1433410.html [4] https://www.criver.com/insights/phenotypic-screening-and-target-deconvolution-perfect-match [5] https://blog.csdn.net/weixin_44585583/article/details/142392727
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-06-05,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

