Nat. Methods | TIRTL-seq: 深度、定量、低成本的配对 TCR 受体测序新方案
Nat. Methods | TIRTL-seq: 深度、定量、低成本的配对 TCR 受体测序新方案

DrugAI
发布于 2026-01-06 13:56:48
发布于 2026-01-06 13:56:48
DRUGONE
T 细胞的特异性由 TCR α链和 β链的组合决定。传统的批量 TCR 测序方法能够以较低成本生成大规模克隆信息,但无法获得 α–β 链的配对关系;而单细胞 TCR 测序虽能提供配对数据,却成本高昂且通量有限。研究人员提出了 TIRTL-seq,这是一种结合实验与计算的新型配对 TCR 测序方案,能够在 384 孔板中并行构建数百个 TCR 文库,每板成本低于 200 美元,为队列规模的 αβ TCR 配对研究提供了切实可行的方案。TIRTL-seq 不仅可以从上百万 T 细胞中同时获得高深度、定量且准确的配对 TCR 信息,还可用于纵向监测病毒感染过程中的克隆扩增,表现优于现有的传统和商业化单细胞 TCR 测序技术。

人体适应性免疫系统依赖 αβ T 细胞通过 TCR 识别抗原。TCR 的多样性由随机的 V(D)J 重排产生,使其能够识别广泛的病原体。然而,大多数抗原特异性克隆在 PBMC 中的频率极低,通常只有万分之一甚至更低,这使得高通量、深覆盖的 TCR 测序技术成为研究免疫反应动态的关键工具。
现有两类技术存在明显局限:
1)批量 TCR-seq(bulk)
- 能同时测到数十万克隆
- 成本低
- 但几乎所有公开数据都只测 TCRβ
- 缺乏 α–β 组合导致无法确认 TCR 特异性
2)单细胞 TCR-seq(scTCR-seq)
- 能获得 α–β 配对
- 但:通量有限、成本高、操作复杂
因此,研究人员希望开发一种技术:低成本 + 高通量 + 准确配对 + 可定量分析, 最终形成 TIRTL-seq。
方法
TIRTL-seq 的核心理念是:将数万到上千万 T 细胞分布在 384 孔板中,每孔进行细胞裂解、逆转录、第一轮 TCR 扩增、加样稀释、第二轮加索引 PCR。每个孔对应特定的条形码,可在一次测序中区分上百至数千个 TCR 文库。研究人员利用优化的 V–C 引物集和液滴式分液技术,使整个流程仅需约 7 小时、成本约 185 美元/板。然后,利用两种计算方法(MAD-HYPE 和新开发的 T-SHELL)从这些孔的 α、β 序列出现模式中重建 αβ TCR 链的配对关系。
结果
TIRTL-seq 流程开发与性能优化
TIRTL-seq 采用液滴式无接触分液,在 384 孔板中实现反应微型化,大幅降低成本与耗时。实验显示:
- 该流程可在单个 T 细胞中稳定检测 α 与 β 链;
- 在每孔 12,500 到 100,000 个 PBMC 的范围内均表现稳定;
- 在 25,000 PBMC/孔时检测到的克隆数达到饱和;
- 单板最高可处理约 1,000 万 PBMC。
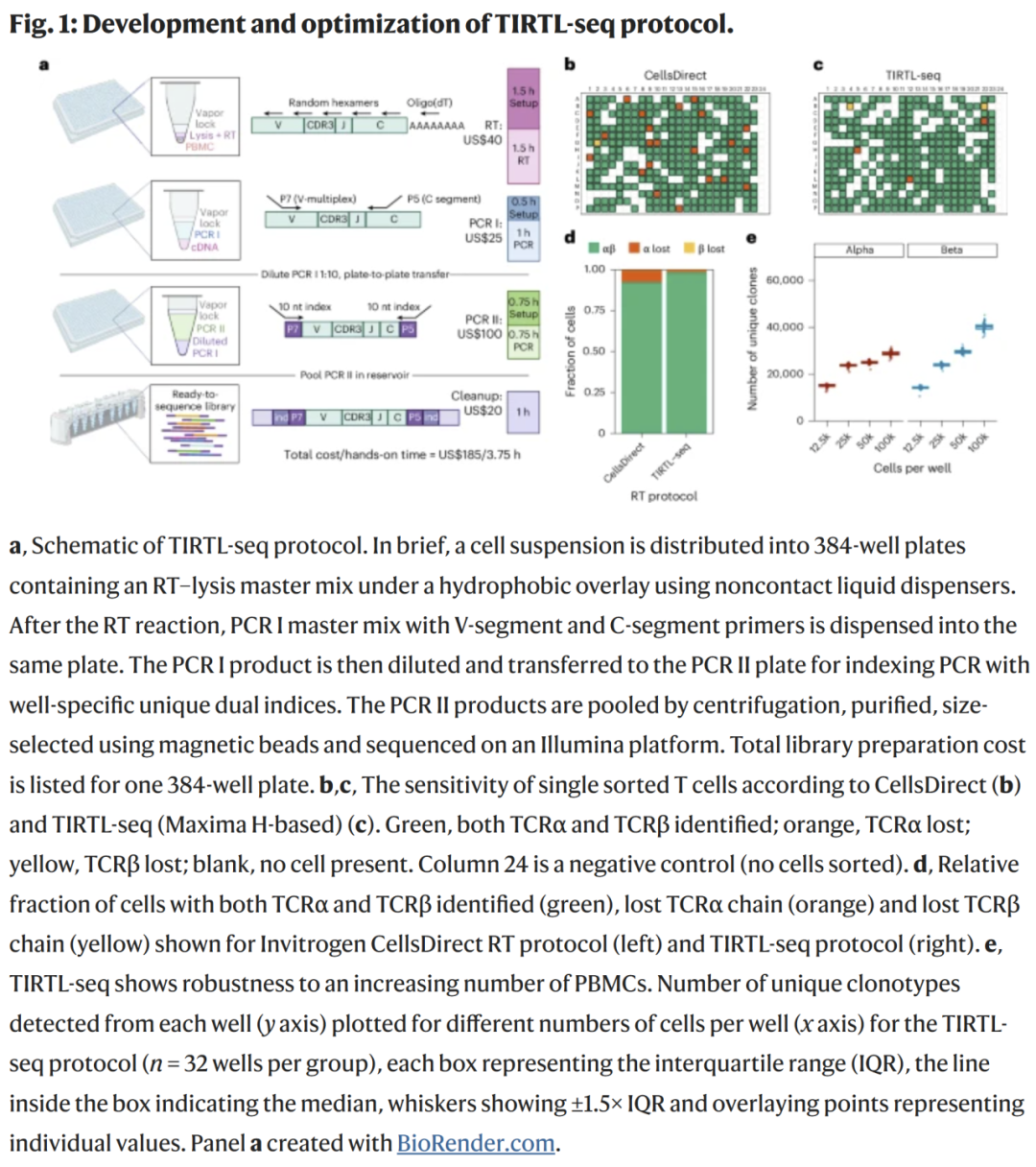
TIRTL-seq 可大规模获得 αβ 配对
利用 MAD-HYPE 算法,研究人员在一个装载 1000 万 PBMC 的 384 孔板中获得了 169,423 对 αβ 配对。
但传统 combinatorial pairing 方法难以配对“高频克隆”(因其出现在几乎所有孔中)。为此,研究人员开发了 T-SHELL 算法,利用 α 链和 β 链的“相对读数频率相关性”进行配对。T-SHELL 能准确识别所有高频克隆的正确 αβ 配对,解决 combinatorial pairing 的核心难题。
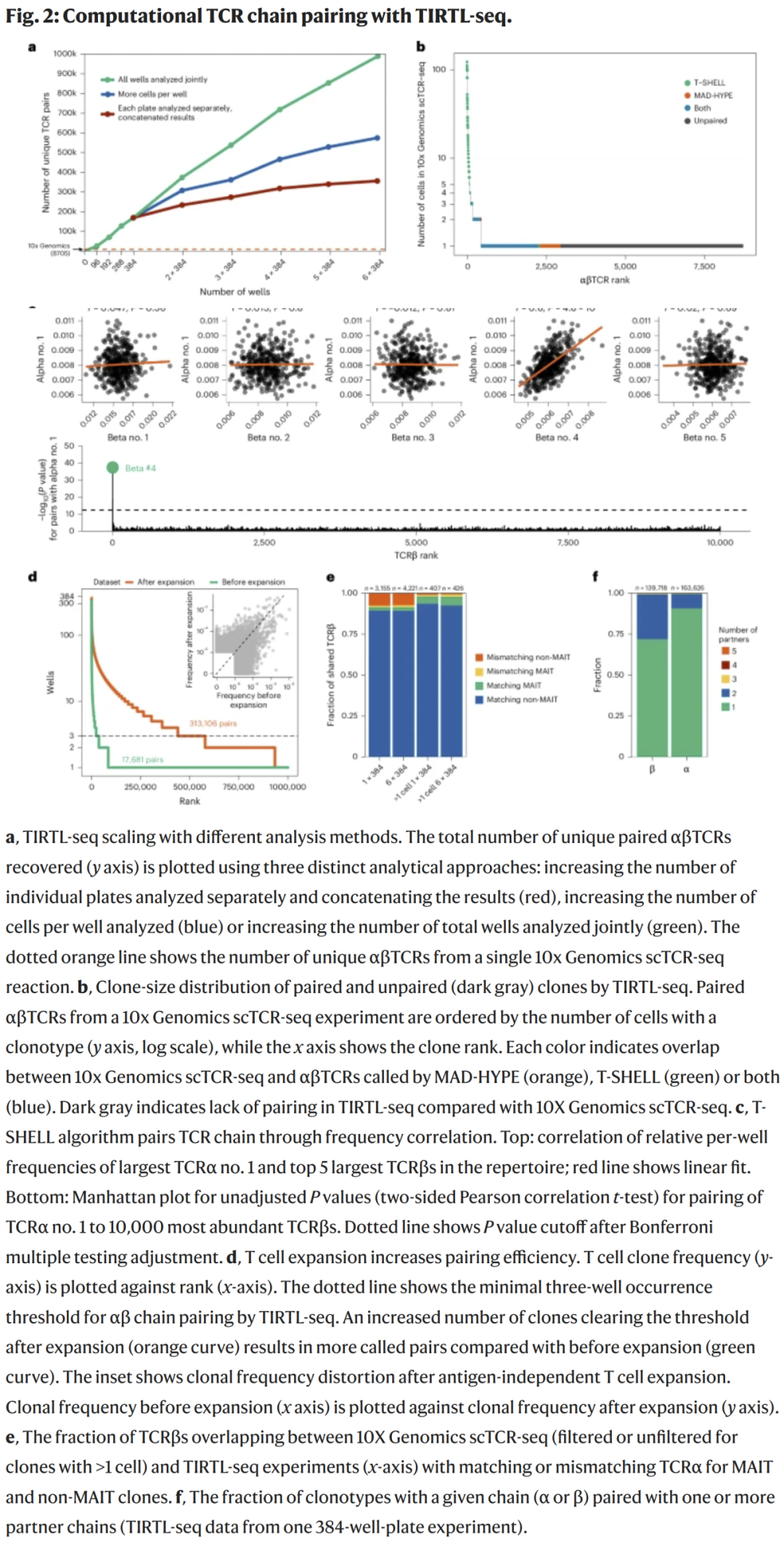
同时精准处理高频与低频克隆
- 高频克隆 → 使用 T-SHELL,配对成功率极高,且与 10x Genomics 技术一致
- 中等频率克隆 → MAD-HYPE 能稳定配对
- 极低频克隆 → 需至少出现在 384 孔中的 3 孔才能配对
研究人员通过体外扩增 T 细胞,使克隆数增加 10 倍,从而显著提高低频克隆的配对数量,但会改变原始频率分布。
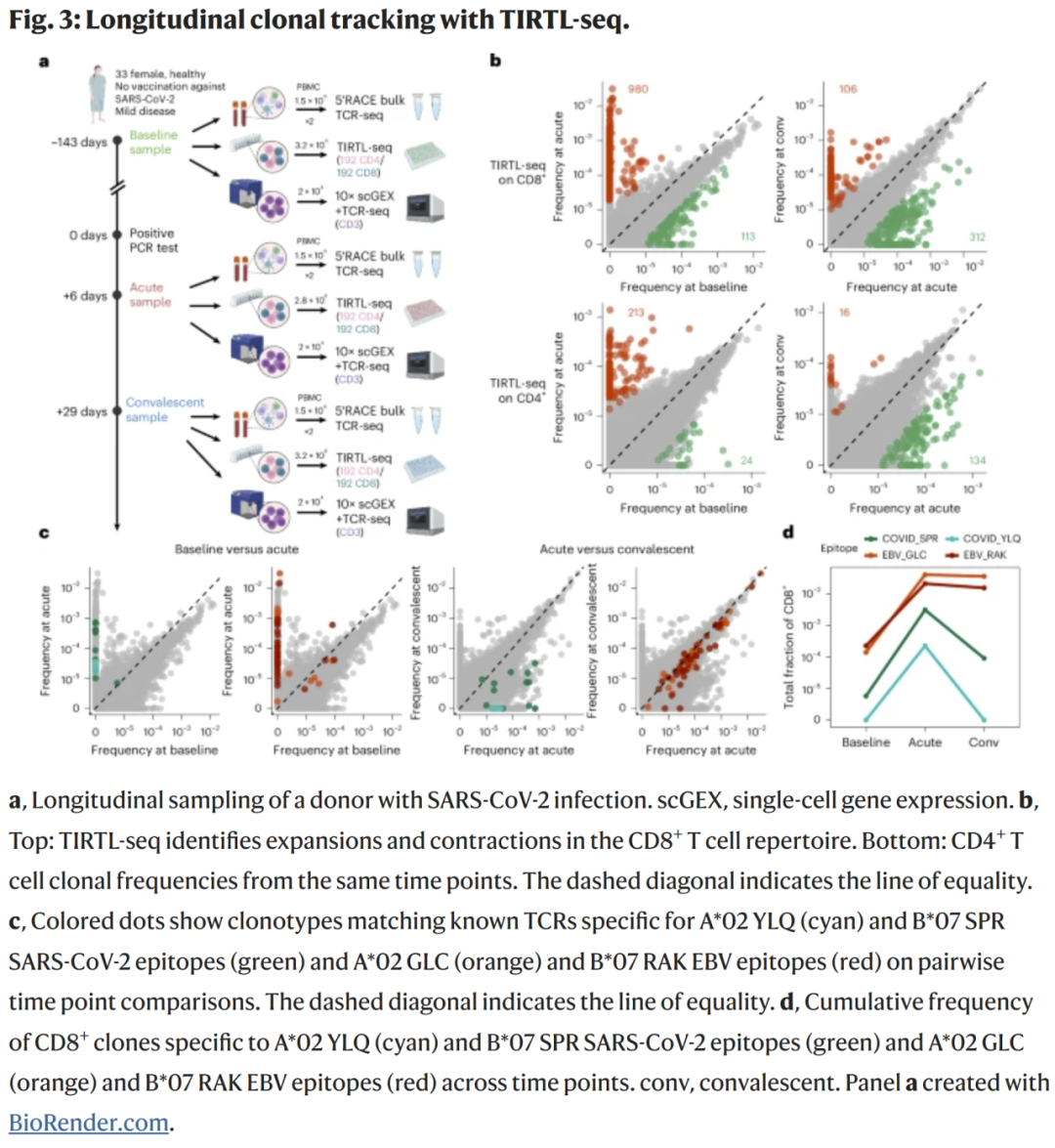
TIRTL-seq 在纵向感染研究中的表现
研究人员分析了一名 SARS-CoV-2 感染者在:
- 感染前(-143 天)
- 急性期(+6 天)
- 恢复期(+29 天)
三次采样中的 TCR 动态变化。
TIRTL-seq 能可靠识别:
- 急性期显著扩增的 CD8+ 与 CD4+ 克隆
- 恢复期显著收缩的克隆
- SARS-CoV-2 特异性克隆的扩增–收缩轨迹
- EBV 特异性克隆的大幅扩增与持续存在
这一结果揭示了急性感染与慢性感染在克隆动力学上的明显差异。
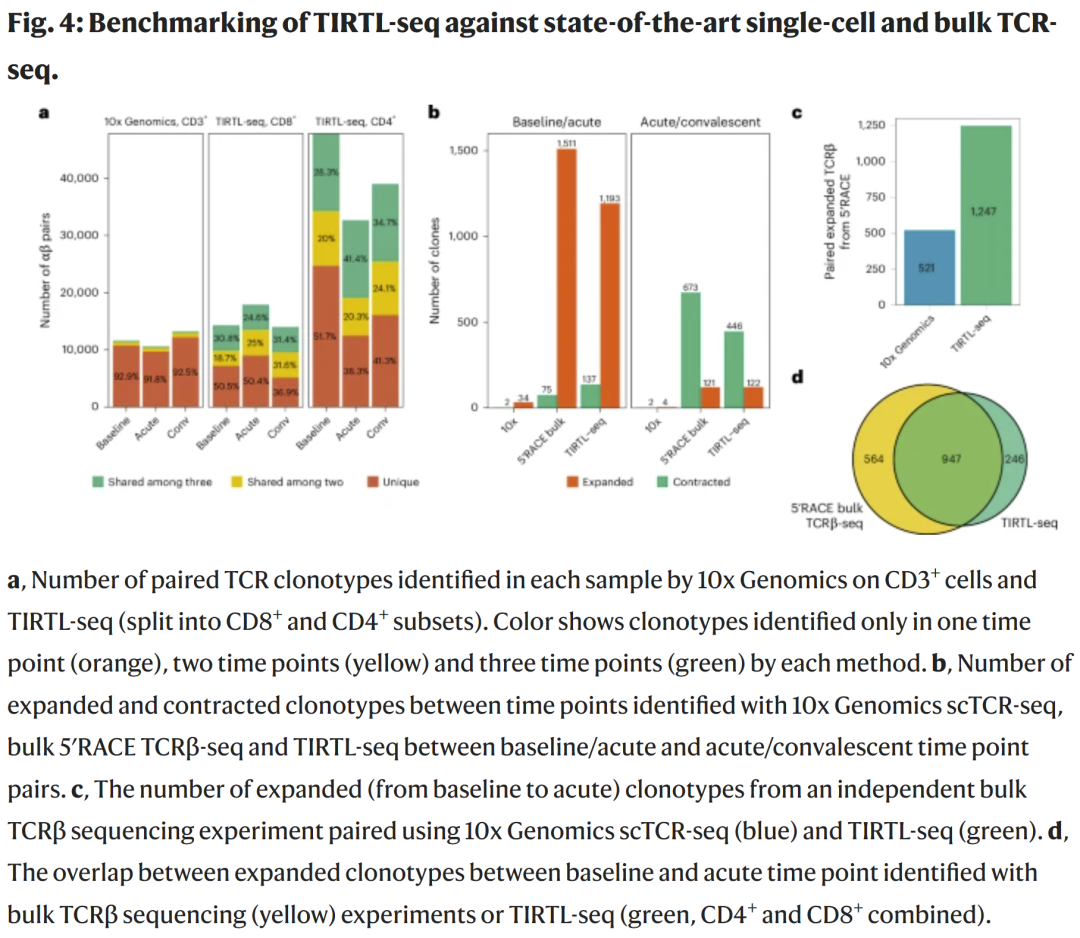
对比 TIRTL-seq、10x scTCR-seq 与 bulk RACE TCR-seq
研究发现:
- 在可获得的克隆量上:
TIRTL-seq(每板 16 万对以上) >> 10x Genomics(~8,700 对)
- 在配对准确性上:
TIRTL-seq ≈ 10x Genomics
- 在纵向识别扩增/收缩克隆方面:
TIRTL-seq 与 bulk 测序中提取的扩增克隆高度一致(约 80% 重叠)
更重要的是:
- TIRTL-seq 的配对成功率远高于 10x,尤其是在真实队列研究中
- 成本却仅为 10x 的约 1/10
讨论
研究人员总结,TIRTL-seq 的优势来自三个方面:
1)低成本且高通量
- 384 孔板微型化
- 每板仅约 185 美元
- 可扩展到上千万 PBMC
2)准确的 αβ TCR 配对
- MAD-HYPE 结合 T-SHELL
- 能处理低频与高频克隆
- 配对准确度媲美单细胞测序
3)可用于纵向免疫监测
- 适用于病毒感染、疫苗应答、自身免疫疾病等
- 能捕获扩增、收缩、持续存在的克隆动态
- 能识别抗原特异性克隆
研究人员指出的不足包括:
- 低频克隆(<3 个细胞)无法获得 αβ 配对
- 无法直接获得 T 细胞表型、基因表达信息
- 扩增前处理会改变克隆频率
- 扩充分辨率依赖 V 区域扩增引物
尽管如此,TIRTL-seq 显著提升了 TCR 配对测序的可及性,为高通量免疫监测和个性化免疫治疗研究提供了关键工具。
整理 | DrugOne团队
参考资料
Pogorelyy, M.V., Kirk, A.M., Adhikari, S. et al. TIRTL-seq: deep, quantitative and affordable paired TCR repertoire sequencing. Nat Methods (2025).
https://doi.org/10.1038/s41592-025-02907-9
内容为【DrugOne】公众号原创|转载请注明来源
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-11-26,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读

