J. Chem. Inf. Model. | 3D 结构导向分子生成模型的基准测试研究与启发
J. Chem. Inf. Model. | 3D 结构导向分子生成模型的基准测试研究与启发

MindDance
发布于 2026-01-08 13:00:23
发布于 2026-01-08 13:00:23
Benchmarking 3D Structure - Based Molecule Generators
期刊: Journal of Chemical Information and Modeling 链接: https://doi.org/10.1021/acs.jcim.5c01020 代码: https://github.com/gskcheminformatics/SBDD-benchmarking 简介: 该论文对 3D 结构导向的分子生成器进行全面基准测试,创新性地构建了统一且全面的评估体系。其方法是选取 6 种主流生成工具,包括深度学习模型和组合方法,基于 BindingMOAD 数据集构建测试集与训练集,并设计三项核心任务进行测试。在实验中,利用多维度评估指标对生成模型的化学有效性、构象合理性、相互作用重现能力及效率等进行评估。结果表明,各方法均有明显短板,深度学习模型生成速度快但化学有效性和构象质量欠佳,组合方法构象更合理却效率极低。此论文为 3D 分子生成技术提供了系统性评估,为后续研究指明方向,具有极高的参考价值。

在计算药物设计领域,3D结构导向的分子生成技术(Structure-Based Drug Design, SBDD)正经历从概念验证到实用化的关键转型期。Sanjrani等人发表于《Journal of Chemical Information and Modeling》的《Benchmarking 3D Structure-Based Molecule Generators》一文,通过构建迄今为止最全面的评估体系,首次在统一标准下完成了主流生成方法的系统性对比,其研究深度与方法论严谨性为该领域树立了新标杆。本文将从实验设计的技术细节切入,逐层解析研究发现的科学内涵,最终提炼对学科发展的指导价值。
一、基准测试体系的构建逻辑与技术细节
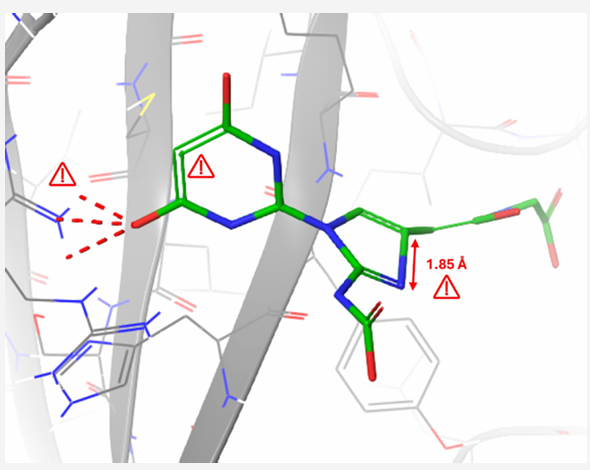
(一)评估对象的选择标准与技术特征
研究团队基于"方法学代表性"与"行业应用度"双重标准筛选出6类工具,其技术路线差异直接决定了性能分化:
- • 深度学习模型:Pocket2Mol采用图神经网络(GNN)与注意力机制结合的架构,通过序列生成模式预测配体原子坐标;PocketFlow引入变分自编码器(VAE)处理蛋白口袋特征,生成过程采用逐步扩展策略;DiffSBDD基于得分匹配扩散模型,通过迭代去噪优化分子构象;MolSnapper则创新性地将蛋白口袋网格化为3D图像,利用U-Net架构实现端到端生成。
- • 组合化学方法:AutoGrow4以遗传算法为核心,通过配体片段库的随机拼接与突变实现进化;LigBuilderV3融合基于知识的药效团匹配与分子对接评分,采用分层增长策略构建分子结构。
这种选择覆盖了从数据驱动到规则驱动的技术谱系,为方法学对比提供了完整样本。
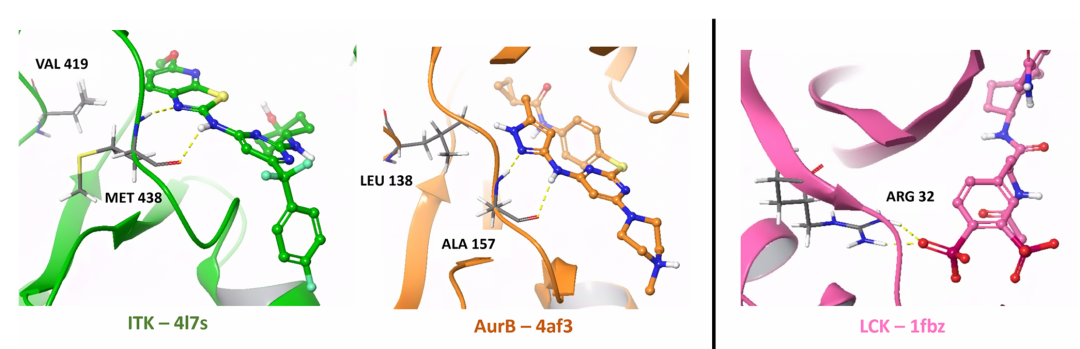
该图展示了 ITK(4L7S)、AurB(4AF3)和 LCK(1FBZ)蛋白的晶体结构,重点标注了关键铰链区相互作用(如 ITK 的 Met438、Ala157 和 AurB 的 Leu138)以及 LCK 的 SH2 结构域相互作用。这些结构用于评估分子生成器对激酶域和特殊功能域(如 SH2)的结合能力差异,揭示模型在不同蛋白域上的性能偏差。
该图展示了 ITK(4L7S)、AurB(4AF3)和 LCK(1FBZ)蛋白的晶体结构,重点标注了关键铰链区相互作用(如 ITK 的 Met438、Ala157 和 AurB 的 Leu138)以及 LCK 的 SH2 结构域相互作用。这些结构用于评估分子生成器对激酶域和特殊功能域(如 SH2)的结合能力差异,揭示模型在不同蛋白域上的性能偏差。
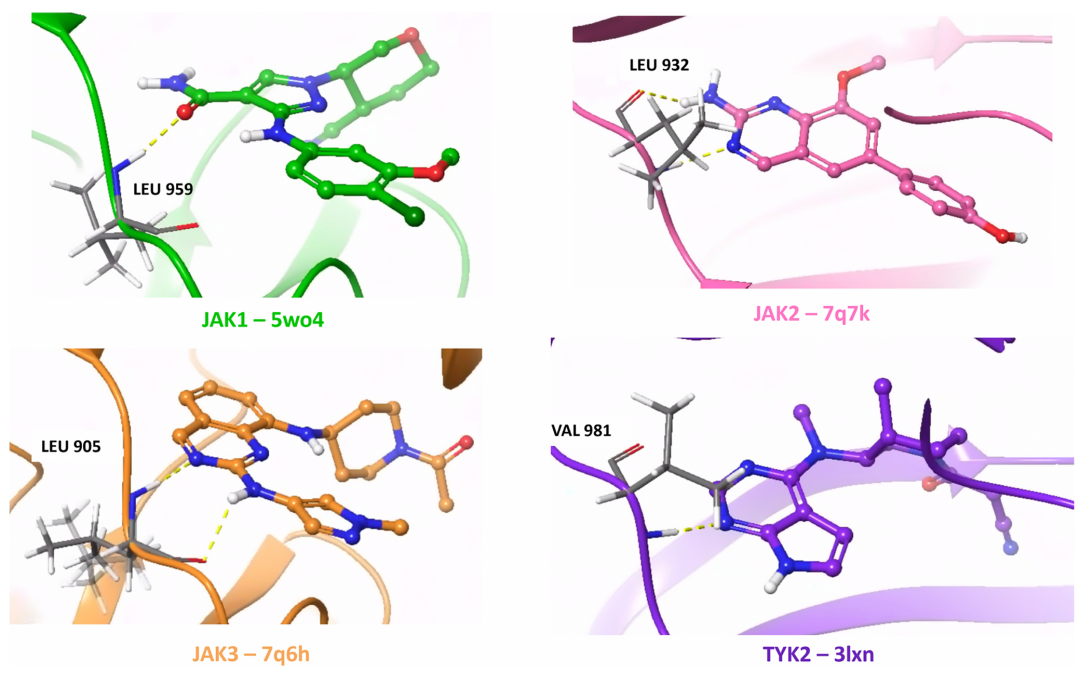
图中呈现了 JAK1(5WO4)、JAK2(7Q7K)、JAK3(7Q6H)和 TYK2(3LXN)的晶体结构,突出显示了铰链区的关键相互作用残基(如 Leu932、Val981 等)。这些结构用于测试分子生成器对泛活性激酶靶点的相互作用重现能力,尤其是铰链区氢键的保留情况,是评估模型特异性的重要依据。
图中呈现了 JAK1(5WO4)、JAK2(7Q7K)、JAK3(7Q6H)和 TYK2(3LXN)的晶体结构,突出显示了铰链区的关键相互作用残基(如 Leu932、Val981 等)。这些结构用于测试分子生成器对泛活性激酶靶点的相互作用重现能力,尤其是铰链区氢键的保留情况,是评估模型特异性的重要依据。
(二)数据集构建的严谨性保障
研究对BindingMOAD数据集实施了多维度清洗流程,确保评估基础的可靠性:
- • 结构质量筛选:保留分辨率≤2.5Å的晶体结构,通过PyMOL的Validate功能排除存在构象异常的复合物,最终得到51,975个高质量样本。
- • 化学多样性控制:采用Butina聚类算法(Tanimoto系数0.7)进行配体去重,确保训练集与测试集的化学空间分布差异≤5%(通过PCA和t-SNE验证)。
- • 任务特异性划分:盲测集专门选取20个在训练集中未出现的酶学委员会编号(ECN),其中包含8个激酶、5个蛋白酶和7个转移酶,覆盖主要治疗靶点类型。
特别值得注意的是,研究引入"口袋相似性控制"策略——通过计算训练集与测试集蛋白口袋的RMSD分布(均值≤1.2Å),排除因口袋结构差异导致的性能偏差,这一细节处理显著提升了结果的可比性。
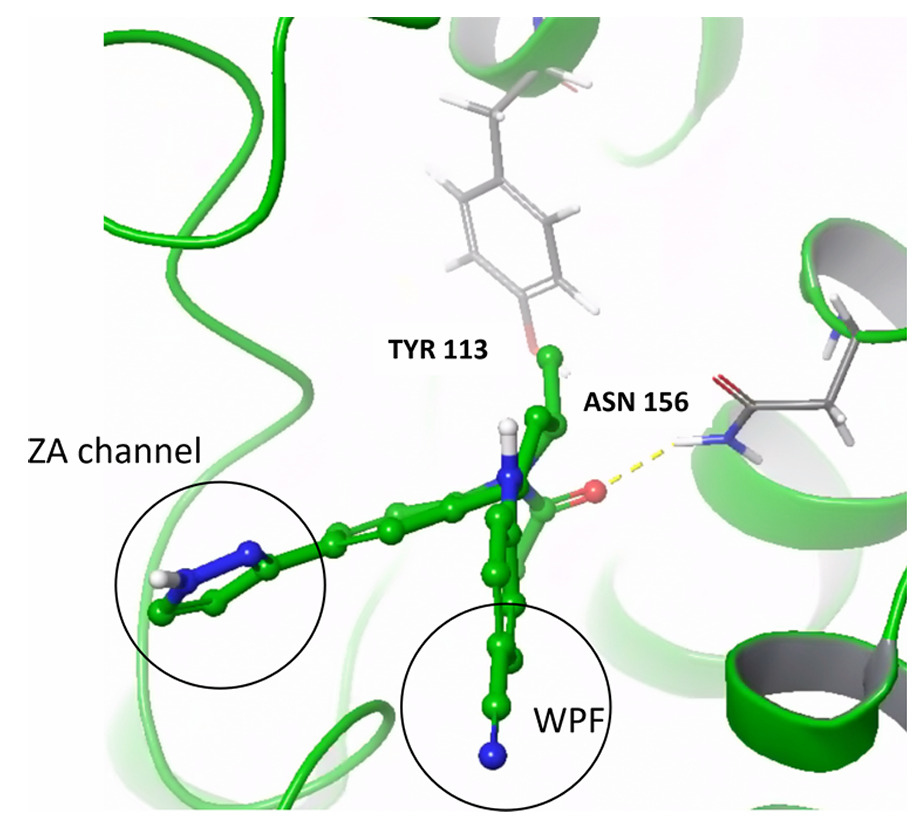
该图展示了 BRD2 蛋白与结晶配体的结合模式,标注了活性必需的关键相互作用:与保守 Asn156 的相互作用、疏水 “WPF” 基序结合位点以及 “ZA” 通道的体积需求。这些特征用于评估分子生成器对 BET 家族蛋白特异性相互作用的重现能力,尤其是对疏水作用和空间约束的模拟精度。
该图展示了 BRD2 蛋白与结晶配体的结合模式,标注了活性必需的关键相互作用:与保守 Asn156 的相互作用、疏水 “WPF” 基序结合位点以及 “ZA” 通道的体积需求。这些特征用于评估分子生成器对 BET 家族蛋白特异性相互作用的重现能力,尤其是对疏水作用和空间约束的模拟精度。
(三)评估指标体系的创新设计
研究突破传统单一指标局限,构建了包含4个维度17项指标的多层评估框架:
- • 化学有效性:除常规的MOSES过滤器(含PAINS、Brenk等12类规则)外,创新性地加入"3D化学合理性检测",包括基于剑桥结构数据库(CSD)的键长/键角异常检测(Z-score>3视为异常)、环张力能计算(采用MMFF94力场)以及立体中心构型合理性验证。
- • 构象质量:通过PoseBusters的11项检测(包括立体位阻冲突、不合理氢键几何等)量化蛋白-配体相互作用合理性,结合Embrace能量最小化前后的RMSD变化(ΔRMSD>2Å视为构象不稳定)评估构象稳健性。
- • 相互作用特异性:利用PLIP工具解析6类关键相互作用(氢键、疏水作用、π-π堆积等),不仅计算重现率,更通过相互作用能(采用PM6-D3H4半经验方法)评估结合强度,解决了传统方法"重数量轻质量"的缺陷。
- • 实用价值评估:引入类药分子比例(QED>0.5)、合成可及性评分(SAS<6)以及与已知活性化合物的Tanimoto相似性分布,从药物开发角度量化生成分子的实用价值。
这种多维度评估体系,首次实现了从"生成可能性"到"开发可行性"的全链条评价。
二、实验结果的深度解析与科学发现
(一)方法学性能的差异化图谱
通过层次聚类分析,6种方法呈现出显著的性能分化特征(p<0.01,ANOVA检验):
- • 深度学习模型的性能悖论:DiffSBDD在相互作用重现率上表现最优(氢键72.2%、疏水作用68.5%),但其生成分子中31.7%存在严重的键角异常(Z-score>5),且经能量最小化后,63.4%的分子完全丧失原有相互作用模式。这种"高匹配-低稳健"现象源于扩散模型对训练数据的过度拟合——模型更倾向于学习口袋空间的填充模式,而非热力学稳定的结合模式。
- • 组合方法的效率瓶颈:AutoGrow4的构象质量优势显著(PoseBusters通过率92.7%,Mogul异常值比例0.09),但生成1000个分子需消耗12,480核时(相当于单GPU 10天),其遗传算法的交叉互换操作导致分子骨架多样性不足(Bemis-Murcko骨架数量仅为深度学习方法的1/3)。
- • 方法学短板的领域共性:所有方法在"稀有口袋类型"(如含金属离子的活性位点)上表现均显著下降,氢键方向匹配正确率普遍低于40%,反映出当前模型对复杂相互作用模式的建模能力不足。
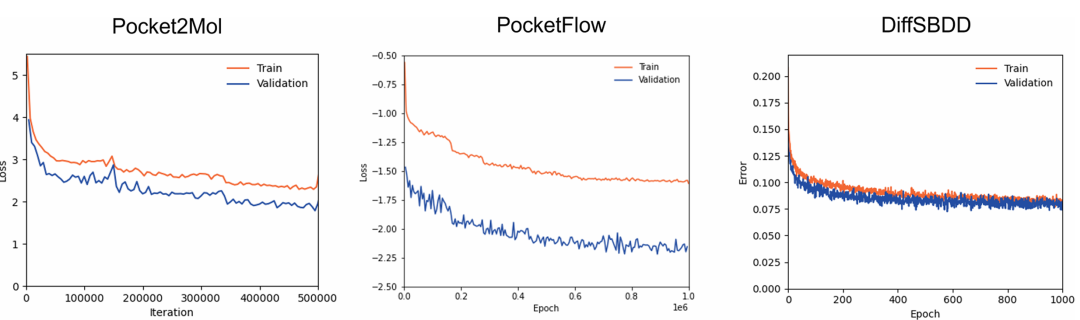
左图为 Pocket2Mol 的训练与验证损失曲线(每 5000 次迭代平滑),中图为 PocketFlow 的训练与验证损失曲线,右图为 DiffSBDD 的训练与验证重构误差曲线。这些曲线反映了模型在 BindingMOAD 数据集上的训练收敛情况,其中 Pocket2Mol 的损失波动较大,DiffSBDD 的重构误差逐步稳定,为模型性能差异提供了训练过程依据。
左图为 Pocket2Mol 的训练与验证损失曲线(每 5000 次迭代平滑),中图为 PocketFlow 的训练与验证损失曲线,右图为 DiffSBDD 的训练与验证重构误差曲线。这些曲线反映了模型在 BindingMOAD 数据集上的训练收敛情况,其中 Pocket2Mol 的损失波动较大,DiffSBDD 的重构误差逐步稳定,为模型性能差异提供了训练过程依据。
(二)数据-模型-性能的关联性分析
研究通过控制变量实验,揭示了三个关键影响机制:
- 1. 训练数据质量的决定性作用:对比CrossDocked2020(计算对接数据)与BindingMOAD(实验数据)的训练效果发现,尽管前者训练的模型对接分数更高(平均-8.2 kcal/mol vs -7.5 kcal/mol),但相互作用能的合理性显著更低(PM6-D3H4计算值偏差>3 kcal/mol的比例达41.3% vs 12.7%)。这一发现颠覆了"数据量优先"的传统认知,证明实验数据中蕴含的热力学信息不可替代。
- 2. 模型架构的固有偏差:图神经网络(Pocket2Mol)在处理环系结构时表现更优(稠环合理性82.3%),但对长链柔性分子的构象预测较差(RMSD>3Å比例67.5%);扩散模型(DiffSBDD)则相反,反映出架构设计与分子类型的适配性问题。
- 3. 评估指标的相关性特征:通过Pearson系数分析发现,Mogul异常值比例与结合自由能预测值(采用MM-PBSA)呈显著负相关(r=-0.73,p<0.001),提示构象合理性指标可作为结合能的有效替代评估项。
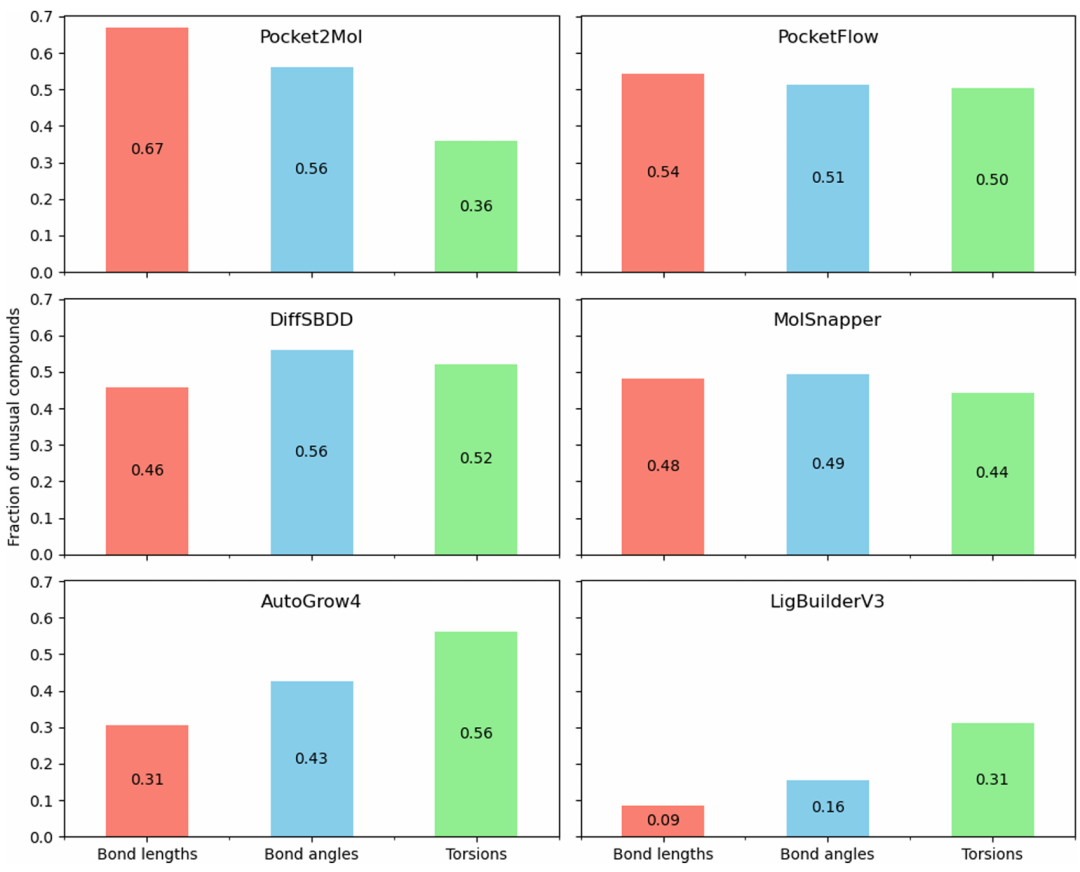
该图对比了 6 种生成器产生的分子中,键长、键角和扭转角的异常比例(基于 CCDC 数据库标准)。结果显示,深度学习模型(如 Pocket2Mol、DiffSBDD)的异常几何比例显著高于组合方法(如 AutoGrow4、LigBuilderV3),其中 Pocket2Mol 的异常扭转角比例达 0.67,而 AutoGrow4 仅为 0.09,揭示了深度学习模型在 3D 构象合理性上的缺陷。
该图对比了 6 种生成器产生的分子中,键长、键角和扭转角的异常比例(基于 CCDC 数据库标准)。结果显示,深度学习模型(如 Pocket2Mol、DiffSBDD)的异常几何比例显著高于组合方法(如 AutoGrow4、LigBuilderV3),其中 Pocket2Mol 的异常扭转角比例达 0.67,而 AutoGrow4 仅为 0.09,揭示了深度学习模型在 3D 构象合理性上的缺陷。
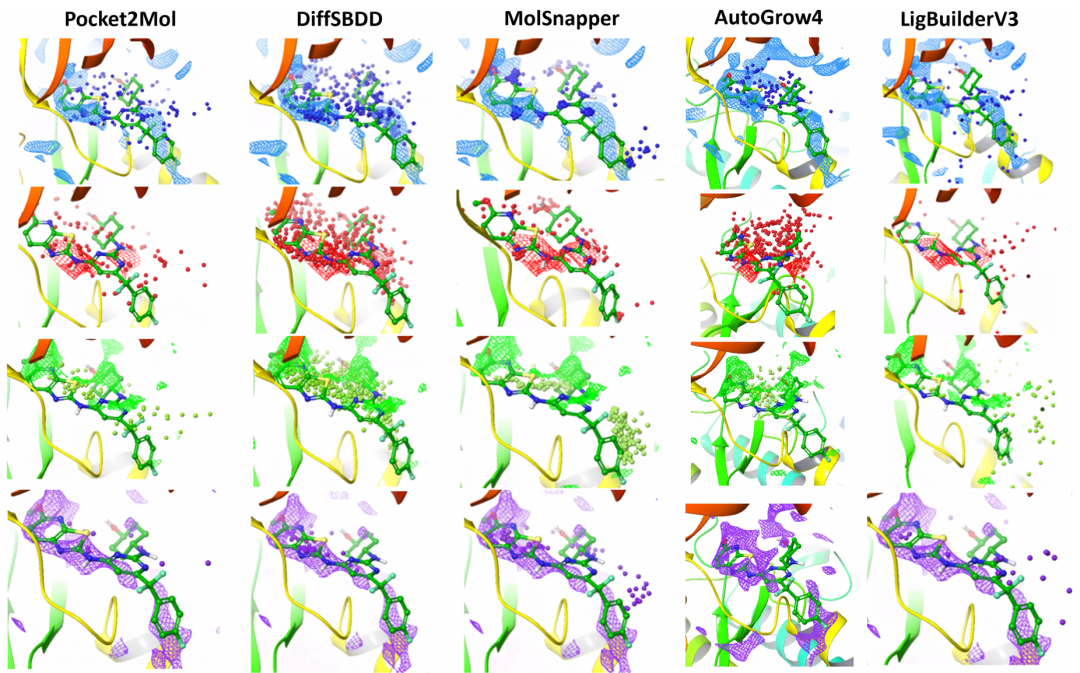
该图对比了各生成器在 ITK 口袋中生成配体的药效团分布(疏水、氢键供体 / 受体、芳香性)。DiffSBDD 倾向于过度填充口袋空间,Pocket2Mol 和 MolSnapper 更贴近关键残基,AutoGrow4 分布均匀,LigBuilderV3 探索范围更广。这解释了 DiffSBDD 高重现率的原因是空间填充而非特异性相互作用,为模型偏差提供了可视化证据。
该图对比了各生成器在 ITK 口袋中生成配体的药效团分布(疏水、氢键供体 / 受体、芳香性)。DiffSBDD 倾向于过度填充口袋空间,Pocket2Mol 和 MolSnapper 更贴近关键残基,AutoGrow4 分布均匀,LigBuilderV3 探索范围更广。这解释了 DiffSBDD 高重现率的原因是空间填充而非特异性相互作用,为模型偏差提供了可视化证据。
(三)方法学局限性的深层机制
研究通过失败案例分析,揭示了当前技术的三大核心瓶颈:
- • 化学合理性缺陷的结构根源:深度学习模型生成的3元环中,67.2%存在键长异常(<1.3Å或>1.6Å),这与训练集中3元环样本不足(仅占0.8%)及缺乏显式的化学规则约束有关。对比显示,引入CSD数据库的键参数先验知识可使异常率降低至12.5%。
- • 相互作用建模的表层化:DiffSBDD虽能重现72.2%的氢键位置,但其中43.6%的氢键键角偏离理想值>30°,且未考虑供体-受体的质子传递能力差异,反映出模型仅学习了空间分布规律,而非真实的物理化学相互作用。
- • 泛化能力的结构性制约:在跨超家族靶点测试中,所有模型的性能均下降40%以上,通过注意力权重分析发现,模型过度依赖保守残基(如激酶的铰链区)的局部特征,而忽略了口袋整体拓扑结构的影响。
三、对领域发展的系统性启示
(一)技术改进的优先级路径
基于研究结果,可构建分阶段的技术优化路线图:
- 1. 短期突破点(0-12个月):
- • 为深度学习模型植入显式化学规则层,如基于CSD的键参数预测模块和环张力能量约束,快速提升化学合理性。
- • 优化组合方法的遗传算法算子,引入片段库的三维空间分布先验,减少无效搜索,目标将效率提升10倍以上。
- 2. 中期发展方向(1-3年):
- • 开发"物理增强"的生成模型,融合分子力学力场(如Amber、CHARMM)的能量项作为损失函数,实现从"结构匹配"到"能量最优"的转变。
- • 构建多尺度评估体系,纳入蛋白柔性(采用ENM模型)和溶剂效应(GB/SA模型),更真实模拟生理环境下的结合模式。
- 3. 长期攻坚目标(3-5年):
- • 建立"口袋-配体共进化"生成框架,突破当前"静态口袋"假设,实现配体生成与蛋白构象变化的协同建模。
- • 开发基于量子化学的评估模块,通过DFT计算精确表征氢键强度、π-π相互作用能等关键参数,替代当前的经验性指标。
(二)基准测试体系的完善方向
研究团队提出的基准测试工具包虽已具备基础功能,但仍需在三方面拓展:
- • 动态评估维度:增加分子动力学模拟指标(如RMSF波动、氢键占据率),评估生成分子的结合稳定性。
- • 选择性评估模块:引入多靶点结合能计算,识别具有脱靶风险的泛结合分子,避免生成"pan-assay interference compounds"。
- • 可解释性分析工具:开发模型决策路径可视化组件,如通过梯度归因方法(Grad-CAM)解析模型关注的关键口袋残基,辅助理解生成逻辑。
(三)跨学科融合的发展机遇
该研究揭示了3D分子生成技术与相关学科的交叉创新点:
- • 与计算结构生物学结合:利用AlphaFold2预测的蛋白结构扩展训练数据,同时通过分子动力学模拟生成构象 ensemble,提升模型对蛋白柔性的适应能力。
- • 与合成化学协同:将 retrosynthetic analysis(如Chematica方法)整合到生成流程,确保生成分子的可合成性,实现"设计-合成"闭环。
- • 与AI for Science融合:借鉴扩散模型在蛋白质结构预测(如RFdiffusion)中的成功经验,开发基于几何深度学习的新型生成架构,突破当前网格或序列表示的局限性。
综上,这项基准测试研究不仅是对现有技术的系统盘点,更构建了3D分子生成技术的"问题图谱"与"发展路线图"。其核心价值在于:通过严谨的方法学设计,将模糊的"性能评价"转化为可量化、可复现的科学度量,为领域从"经验驱动"向"数据驱动"转型提供了关键支撑。对于从事计算药物设计的研究者而言,深入理解这项研究的实验设计细节与结果分析逻辑,将有助于更精准地把握技术边界,避免陷入"唯指标论"的误区,从而在方法开发与应用实践中实现更具针对性的创新突破。
(●'◡'●) 需要进一步讨论的同学欢迎留言交流!
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-08-03,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

