Science | AI 驱动的结构基础模型
Science | AI 驱动的结构基础模型

MindDance
发布于 2026-01-08 12:59:53
发布于 2026-01-08 12:59:53
AI to rewire life’s interactome: Structural foundation models help to elucidate and reprogram molecular biology
期刊: Science 链接: https://doi.org/10.1126/science.adx7802 https://zenodo.org/records/6568518 代码: https://github.com/zrqiao/NeuralPLexer 简介: 本文探讨了利用人工智能和加速计算构建 “计算显微镜”,以解析生物分子相互作用组,为分子设计和治疗开发提供新机会,其创新点在于将生成式机器学习方法应用于解决蛋白质 - 配体相互作用及构象景观等复杂问题。研究团队开发了 NeuralPLexer 生成式 AI 策略模拟蛋白质 - 配体结合景观,还开发了 OrbNet-Equi 几何深度学习方法研究分子相互作用的能量学,并通过多种实验验证了这些工具的有效性。在预测隐蔽口袋、解析蛋白质功能机制、发现新口袋和设计配体等方面,这些工具均表现出色,如 NeuralPLexer 在 KRAS-G12C 等目标上的设计成功率高于传统方法。该论文展示了结构基础模型在解析和重塑分子生物学中的潜力,为相关领域的研究和应用开辟了新路径。

在分子生物学领域,生物分子间的相互作用是生命活动的核心。从信号传递到能量转换,这些历经进化形成的精密调控网络,蕴藏着疾病治疗与分子设计的无限可能。近日,发表于《Science》的重磅论文《AI to rewire life’s interactome》,系统阐述了如何利用人工智能(AI)与加速计算技术构建"计算显微镜",为解析和重构生物分子相互作用组提供了革命性工具。
一、生物分子相互作用解析的困境与突破方向
生物分子(如蛋白质与小分子)的相互作用是构成复杂生物组织、协调生命基本过程的基础。要理解这些相互作用,需解析其三维原子结构,但传统实验手段存在显著局限:X射线晶体学、冷冻电镜等方法虽能获得高精度结构,却受限于实验室研究的低效率——从样本制备到结构解析往往需要数月时间,难以满足大规模研究需求。
半个世纪以来,突破这一瓶颈的关键在于构建"计算显微镜":直接从分子序列信息合成结构视图。近年来,AI驱动的蛋白质结构预测技术取得里程碑进展,AlphaFold2等模型通过学习进化约束(如多序列比对、蛋白质语言模型),借助神经网络实现了氨基酸三维结构的高精度预测,为这一目标提供了可能。
二、生成式AI在分子构象研究中的核心应用
1. NeuralPLexer:蛋白质-配体相互作用的动态解析工具
生物分子具有高度动态性,其功能依赖于多种构象状态的转换。传统"锁钥模型"假设蛋白质为刚性结构,无法解释配体结合引发的构象变化;分子动力学模拟虽能捕捉动态过程,但因需跨越能垒而计算成本极高。
针对这一挑战,研究团队开发了NeuralPLexer生成式AI策略,基于生成扩散模型模拟蛋白质-配体结合的热力学景观:
- • 从分子复合物的初始草图出发,逐步细化原子级结构细节;
- • 通过多初始猜测同步生成构象快照,覆盖完整的动态构象空间;
- • 采用模拟生物分子层级结构的神经网络,在保持物理对称性的同时,利用蛋白质-配体接触信息优化预测。
实验验证显示,NeuralPLexer在多场景中表现优异:
- • 准确预测"隐蔽口袋"(配体结合诱导产生的新型结合位点),构象分布与实验数据一致;
- • 对酶系统的构象采样通过TM-score、Q-factors等指标验证,精度超越静态模型;
- • 无需亲和力训练数据,即可通过构象预测的置信度区分强弱结合剂。
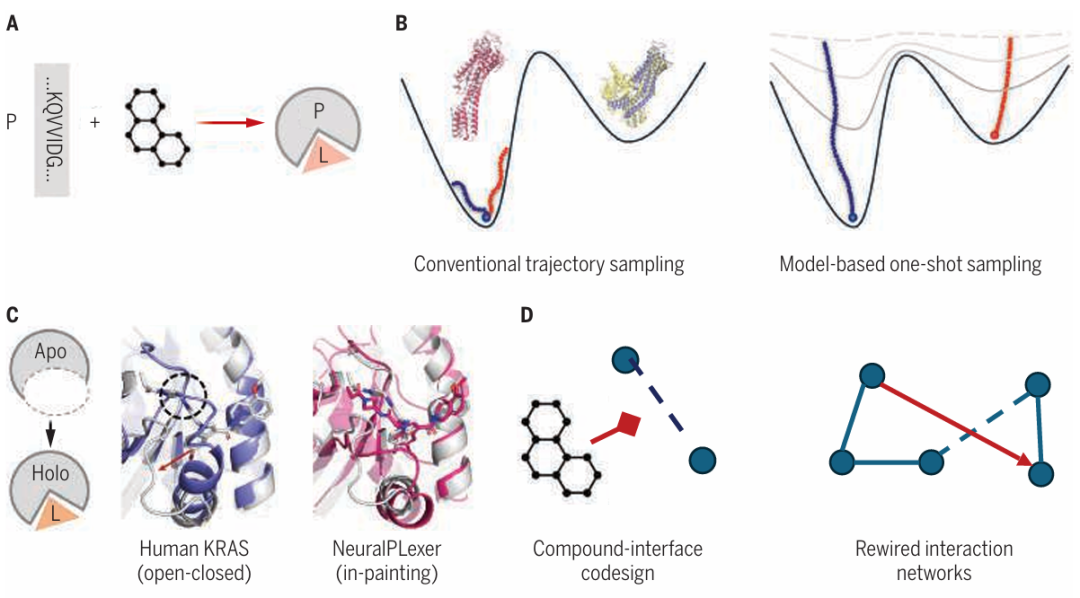
A. 展示了蛋白质 - 配体复合物的生成式结构预测示意图。B. 体现了生成式建模能够从分子构象景观中快速采样。C. 以人类 KRAS G12C 配体结合状态的预测为例,展示了 NeuralPLexer 预测所揭示的结构见解。D. 呈现了结构预测基础模型和从头分子设计方法的新机遇。
A. 展示了蛋白质 - 配体复合物的生成式结构预测示意图。B. 体现了生成式建模能够从分子构象景观中快速采样。C. 以人类 KRAS G12C 配体结合状态的预测为例,展示了 NeuralPLexer 预测所揭示的结构见解。D. 呈现了结构预测基础模型和从头分子设计方法的新机遇。
2. 从结构预测到机制解析:揭示分子功能的深层逻辑
NeuralPLexer的价值不仅在于结构预测,更在于其解析分子功能机制的能力:
- • 在酮醇酸还原异构酶研究中,模型捕捉到辅因子与抑制剂结合时N-亚结构域的闭合运动,为酶催化机制提供关键线索;
- • 对G蛋白偶联受体的构象预测,解释了其在无配体时的组成型活性,揭示了受体激活/失活的结构基础。
这些成果表明,AI模型可成为解析变构调节、酶催化等分子机制的核心工具,为理解生物功能的结构基础提供全新视角。
三、跨尺度分子研究的技术协同与创新
1. OrbNet-Equi:分子能量学的高效计算引擎
除结构预测外,分子相互作用的能量学特征是理解反应机制的关键。研究团队开发的OrbNet-Equi几何深度学习方法,实现了量子力学精度的能量计算:
- • 对主族化学体系的预测精度媲美全精度量子力学方法;
- • 计算速度提升约1000倍,可解析质子化状态、电子自旋构型等细节;
- • 为质子/电子转移路径设计提供了全面分析策略。
2. 基于"图像修复"原理的新型结合位点发现
突破已知相互作用的局限,研究团队为NeuralPLexer赋予口袋从头设计能力:借鉴AI图像编辑的"局部修复"逻辑,仅利用目标蛋白的骨架结构,即可同步预测配体结构、蛋白质序列及口袋形状变化。
在KRAS G12C(一种与癌症密切相关的突变蛋白)研究中,该方法的设计成功率显著高于传统对接算法,证明其在未表征结合位点的配体设计中具有独特优势。
四、结构基础模型的未来拓展与学科影响
随着结构预测模型精度的提升,其应用将向更复杂的生物组装体拓展,包括:
- • 化学调节剂稳定的蛋白质-蛋白质相互作用(诱导接近效应);
- • 任意 stoichiometry 的生物组装体解析。
这些进展将推动"理性设计配体"成为可能:通过重塑蛋白质相互作用网络,恢复细胞健康状态。统一的相互作用预测模型与从头设计框架,有望在以下领域产生变革:
- • 精准调控蛋白质寡聚状态,扩大治疗窗口;
- • 设计新型变构调节剂,靶向传统"不可成药"靶点;
- • 加速从分子机制到临床药物的转化周期。
结语
该研究通过AI与结构生物学的深度融合,构建了从静态结构到动态功能、从已知相互作用到从头设计的完整研究体系。正如"计算显微镜"的隐喻所示,这些工具不仅是实验手段的补充,更重塑了我们解析生命相互作用组的认知方式——为基础研究与药物研发提供了"看见"分子动态、"设计"相互作用的能力,标志着分子生物学进入AI驱动的理性设计时代。
(●'◡'●) 需要进一步讨论的同学欢迎留言交流!
本文参与 腾讯云自媒体同步曝光计划,分享自微信公众号。
原始发表:2025-07-28,如有侵权请联系 cloudcommunity@tencent.com 删除
评论
登录后参与评论
推荐阅读
目录

