顶刊分享--激活的ATF6α是限制免疫监视的肝脏肿瘤驱动因子
原创顶刊分享--激活的ATF6α是限制免疫监视的肝脏肿瘤驱动因子
原创
追风少年i
发布于 2026-02-21 15:27:25
发布于 2026-02-21 15:27:25
作者,Evil Genius
春节了, 越长大越孤单,玩的朋友都没几个了。
学员们也是非常辛苦,大年初一改本子,现在申请国自然等课题,真的是非常耗精力。
科研这条路非常不好走,除非特别有兴趣 + 家庭条件允许,正常的逻辑是努力读到博士,进课题组,有编制无后顾之忧,然后发挥自己的兴趣,在科研的路上慢慢探索,我这种没条件,农村出身是没办法的事,当初选择专业,没人引导,像生物、食品、还有农学、医学相关的专业,当初有人告诉我一声读到博士才有出路,那当时肯定不会选择的,如果当初也选择了自动化、车辆工程等硬核工学专业,估计生活现在应该好得多,不至于和高中同学差距如此的大了。
今天我们分享文献,应该是国人发的,不过是在德国留学。

一般这种正刊的文章都涉及到了生物学问题的机制,基本都是多组学。
知识积累
人肝细胞癌中ATF6α的活化与侵袭性肿瘤表型显著相关,表现为患者生存期缩短、肿瘤进展加速及局部免疫抑制。在小鼠肝细胞中特异性激活ATF6α可诱发进行性肝炎,伴随内质网应激、免疫抑制和肝细胞增殖。同时,激活的ATF6α通过结合基因调控元件直接抑制糖异生酶FBP1,并增强糖酵解。恢复FBP1表达可减轻ATF6α活化相关的病理改变。
肝细胞内ATF6α的持续激活会触发肝癌发生、瘤内T细胞浸润以及营养匮乏导致的免疫耗竭。
内质网应激和UPR激活是癌症中的负面预后因素,并与肝脏疾病相关。UPR包含三种具有下游信号级联的内质网跨膜蛋白:(1)PKR样内质网激酶(PERK);(2)肌醇需求酶1α(IRE1α);(3)活化转录因子6α(ATF6α),其被切割产生N末端p50片段(nATF6α)进入细胞核,激活内质网伴侣蛋白和脂质合成基因。虽然PERK和IRE1α可能促进癌症特征,但对ATF6α的了解较少,其在肠上皮细胞中的慢性激活会诱导微生物群依赖性结肠腺瘤.
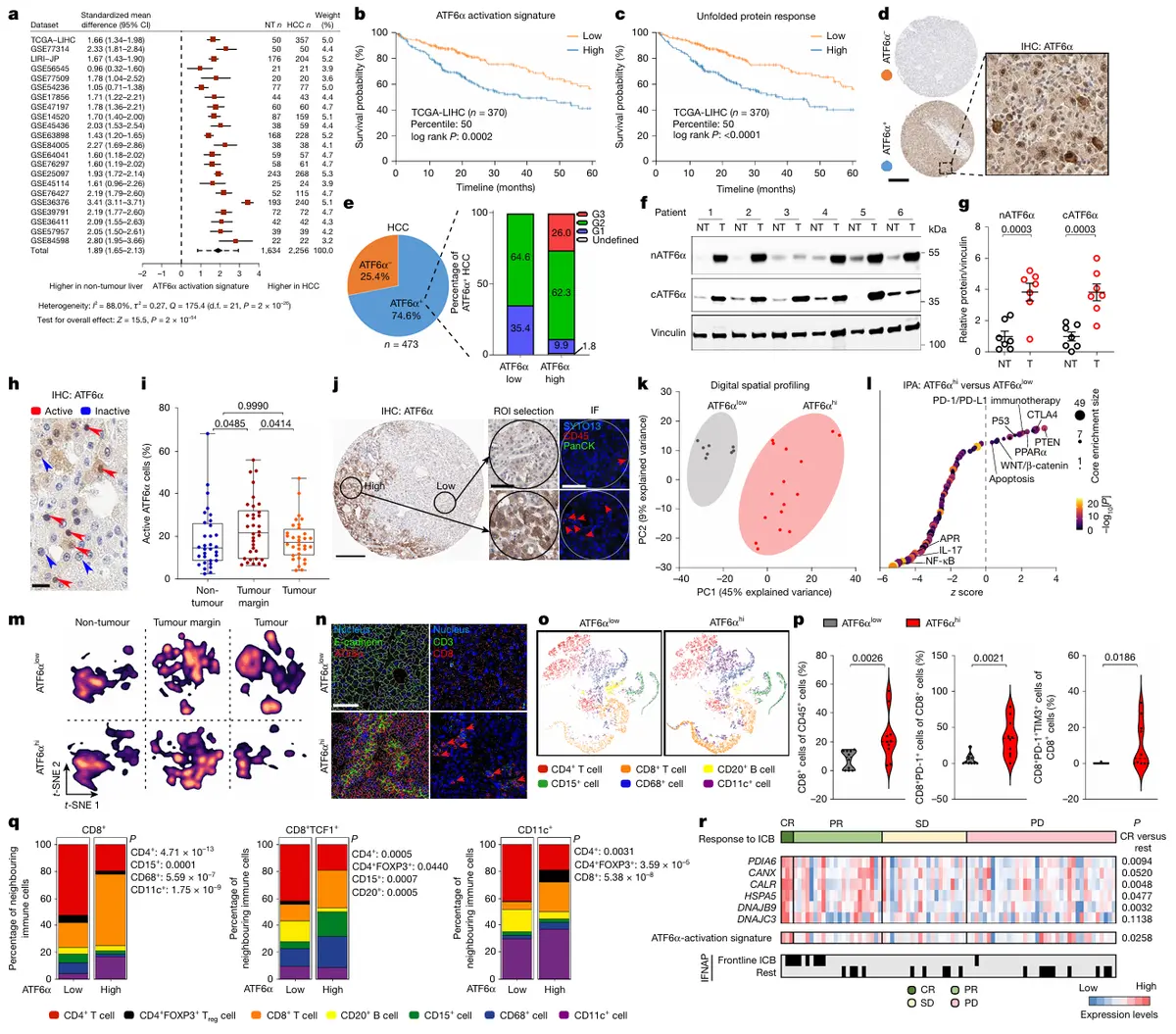
结果1、ATF6α活化标志着侵袭性肝癌
患者来源的肝脏切片显示核ATF6α表达,表明慢性肝炎中存在内质网应激和ATF6α活化。
ATF6α的持续活化(尤其是其核转位)是驱动肝癌恶性进展的关键事件,与患者预后不良、肿瘤增殖及代谢重编程密切相关,是潜在的预后标志物。
ATF6α活化作为肿瘤驱动因子的多组学证据
空间转录组学揭示ATF6α高表达区域的分子特征
通过对人类肝癌连续切片中ATF6α高表达(ATF6αhi)与低表达(ATF6αlow)区域进行空间转录组测序,发现:
伴侣蛋白与癌基因:ATF6α特异性伴侣蛋白HSP90B1及癌症相关基因在ATF6αhi区域显著上调。
通路富集:ATF6αhi区域富集了PD-1/PD-L1、CTLA-4信号、缺氧、细胞周期进展及糖酵解通路。
代谢开关:糖酵解增强与FBP1下调相关,而FBP1低表达与侵袭性肝癌亚型(T-SIII)及患者生存期缩短密切相关。FBP1减少作为代谢开关,在应激肝细胞和肝癌祖细胞中逆转衰老、支持增殖并促进DNA损伤诱导的突变。
成像质谱流式揭示ATF6αhi肿瘤的免疫微环境特征
免疫细胞浸润:ATF6αhi肿瘤区域CD8+ T细胞及CD11c+ 细胞浸润增加,但其中CD8+PD-1+ T细胞及CD8+PD-1+TIM3+终末耗竭T细胞比例显著升高。
细胞邻域分析:ATF6αhi肿瘤中形成以CD11c+树突状细胞(DC)和CD4+ T细胞为中心的CD8+ T细胞聚集灶,同时CD11c+ DC与FOXP3+CD4+调节性T细胞(Treg)共定位增强,提示局部免疫抑制;而ICB应答相关的CD8+TCF1+ T细胞亚群在ATF6αhi肿瘤中几乎不与Treg共定位。
ATF6α活化与ICB治疗反应的相关性
对接受抗PD-1单药治疗的晚期肝癌患者样本分析发现,获得完全缓解的患者肿瘤组织中ATF6α靶基因表达及ATF6α活化特征基因集显著高于疗效不佳者,提示ATF6α活化可能使肿瘤对免疫检查点阻断疗法敏感。
结论:ATF6α活化通过驱动代谢重编程(下调FBP1促进糖酵解)和重塑免疫微环境(促进T细胞耗竭及Treg共定位),在肝癌发生发展中发挥驱动作用;但ATF6αhi肿瘤的独特免疫微环境特征(如CD8+TCF1+ T细胞与Treg的分离)可能解释其对ICB治疗的良好响应性。
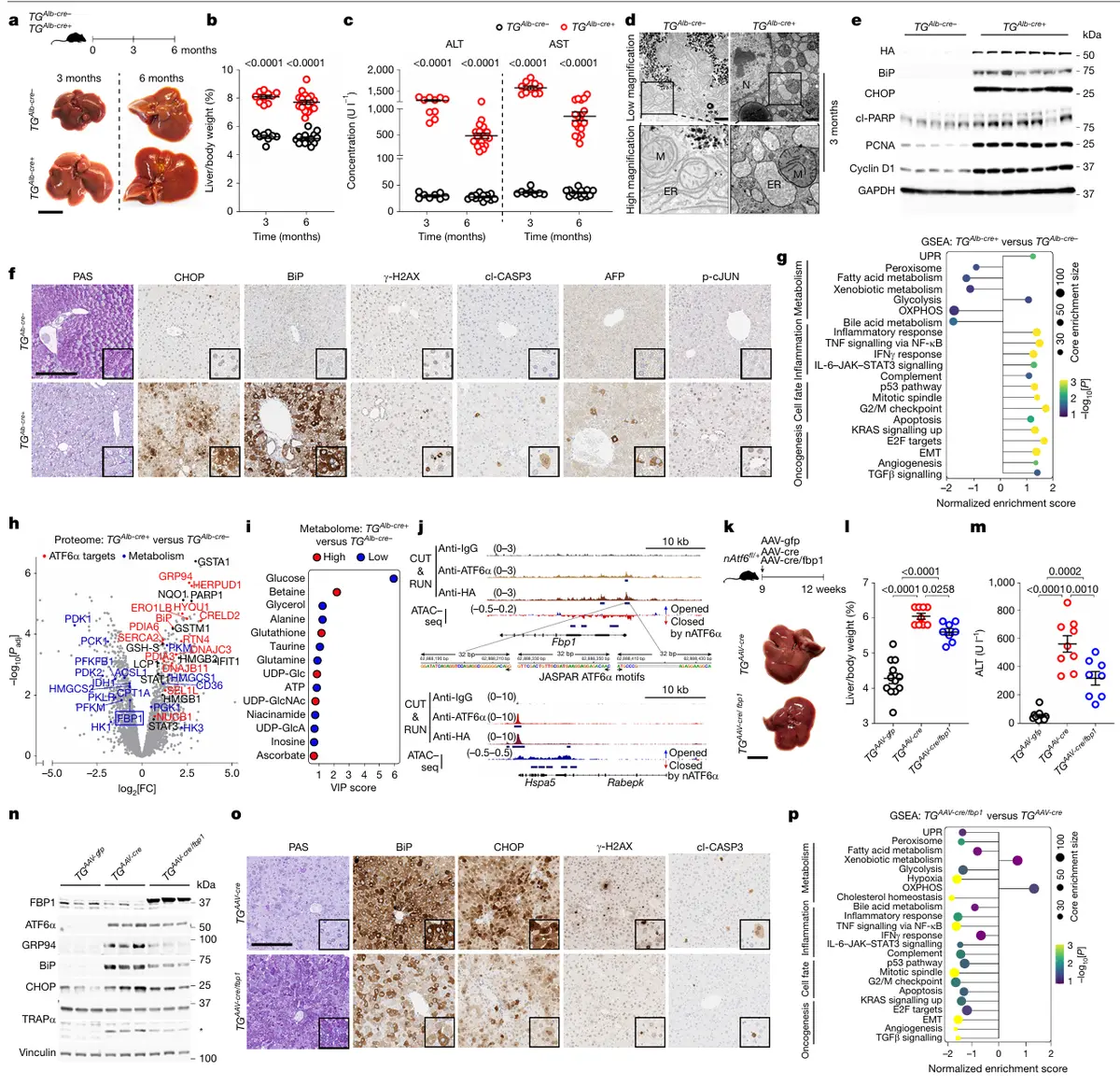
结果2、肝细胞ATF6α活化诱导损伤的机制及FBP1的保护作用
肝细胞特异性ATF6α活化小鼠模型的建立与表型
通过他莫昔芬诱导的肝细胞特异性nATF6α转基因小鼠(TGAlb-cre+)及AAV8-cre介导的ATF6α活化模型(TGAAV-cre),发现:
肝脏损伤:小鼠出现肝肿大、肝重比增加、血清转氨酶(ALT/AST)升高。
内质网应激:电镜显示内质网板层结构肿胀破裂;UPR靶基因(如Hspa5)及蛋白表达上调。
增殖与癌变相关指标:Ki-67、PCNA、cyclin D1等增殖标志物升高,DNA损伤标志γ-H2AX、凋亡标志cl-PARP/cl-CASP3增加,甲胎蛋白(AFP)、癌症干细胞标志物CD44v6、癌蛋白p62及p53结合蛋白1(53BP1)表达上调。
转录组改变:GSEA分析显示UPR、糖酵解、炎症、细胞周期及致癌信号通路上调,而解毒代谢和氧化磷酸化下调;胆固醇合成相关蛋白(HMGCS1、CD36)增加,脂肪酸代谢转录下调。
ATF6α直接调控糖代谢重编程
糖酵解增强:糖酵解酶(PKM、PGK1)表达增加。
糖异生抑制:FBP1等糖异生限速酶被显著抑制,导致肝糖原和葡萄糖耗竭。
直接结合证据:CUT&RUN实验证实nATF6α直接结合于FBP1启动子区域;ATAC-seq显示FBP1位点染色质可及性降低,提示表观遗传沉默。
生理功能影响:ATF6α活化小鼠表现出葡萄糖耐受性增强(提示糖利用改变),但胰岛素耐受性、运动、呼吸及摄食饮水无显著变化。
FBP1恢复对ATF6α活化损伤的保护作用
肝脏损伤缓解:AAV介导的肝细胞FBP1回输降低肝重比、血清转氨酶及葡萄糖敏感性。
内质网应激减轻:UPR诱导减弱、TRAPα低糖基化状态改善、DNA损伤及细胞凋亡/增殖减少。
代谢重塑逆转:糖酵解下调、氧化磷酸化(OXPHOS)恢复、牛磺酸(促肝癌糖酵解代谢物)水平降低、葡萄糖水平升高、13C标记乳酸摄取减少。
酶活性依赖:只有催化活性的FBP1(而非E98A突变体)能恢复糖原、限制ATF6α靶基因诱导并降低血清及肝脏脂质积累。
机制模型
ATF6α活化直接抑制FBP1→糖异生受阻→糖原/葡萄糖耗竭→蛋白质N-糖基化底物缺乏→内质网功能紊乱→内质网应激持续→ATF6α持续活化(恶性循环)。恢复FBP1可打断这一循环,通过恢复糖异生、提供糖基化底物、减轻内质网应激,从而缓解肝损伤及癌前病变。
结论:肝细胞ATF6α持续活化通过直接转录抑制FBP1,驱动糖代谢重编程(糖酵解增强、糖异生阻断),导致内质网应激恶性循环和肝损伤,而FBP1功能恢复可逆转这一过程,提示FBP1是ATF6α下游的关键代谢节点和潜在干预靶点。
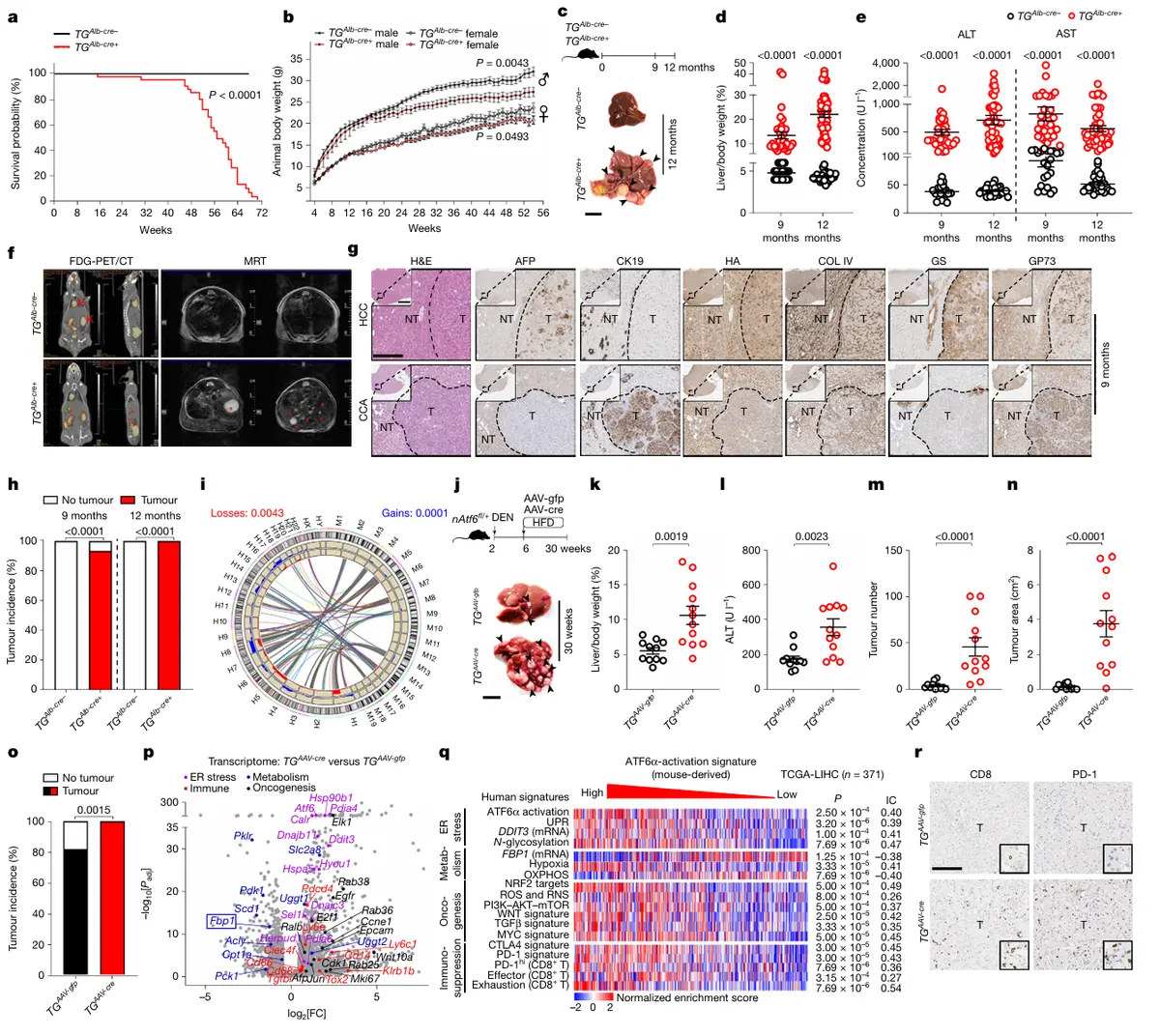
结果3、ATF6α活化驱动小鼠肝癌发生及FBP1的保护作用
肝细胞ATF6α持续活化通过抑制FBP1,驱动ER应激、代谢重编程及免疫耗竭微环境,最终导致肝癌发生;FBP1恢复可阻断这一进程并减轻T细胞耗竭,进一步证实FBP1是ATF6α下游关键效应分子及潜在治疗靶点。
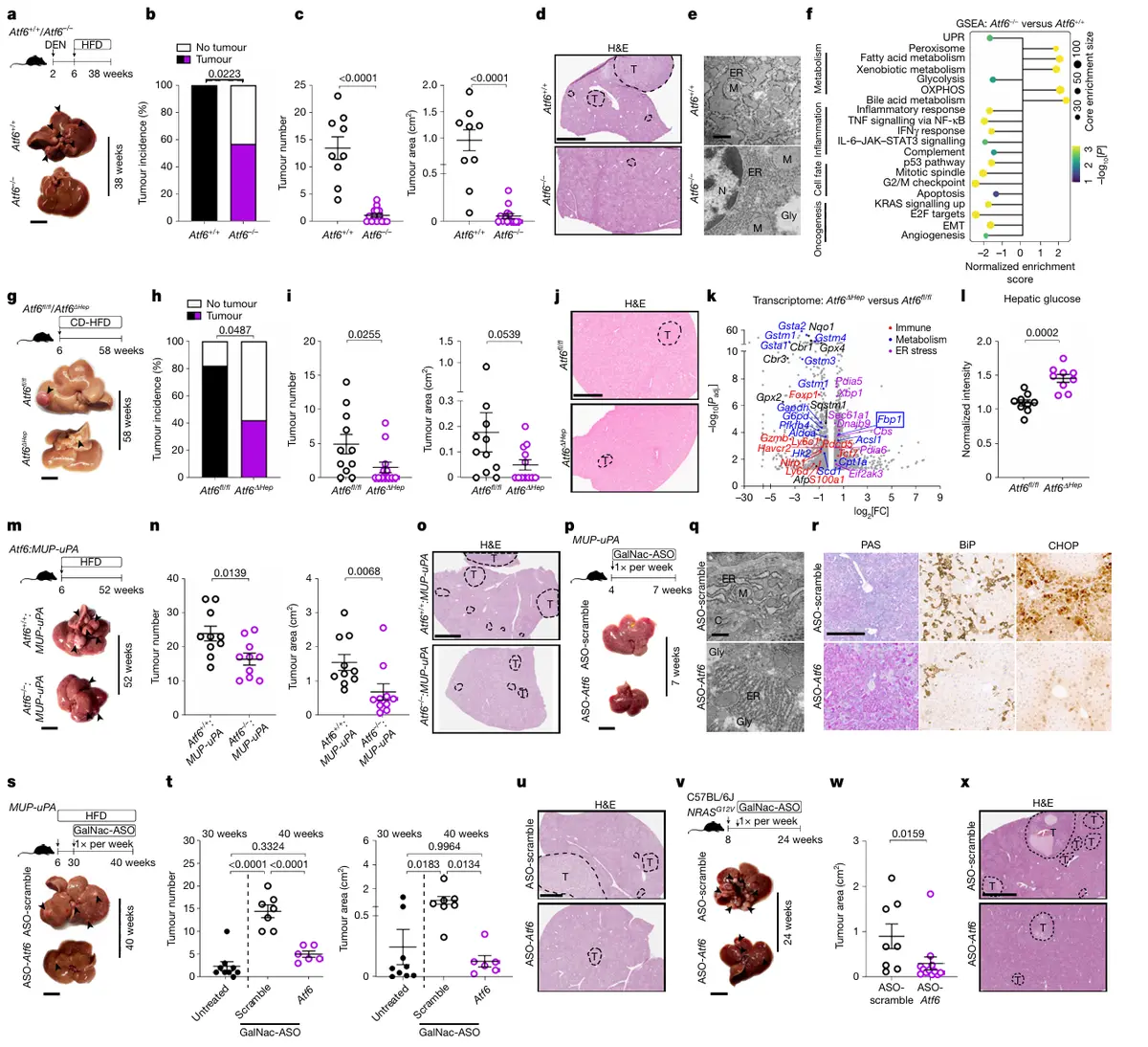
结果4、Atf6缺失及靶向治疗在小鼠肝癌模型中的保护作用
全局Atf6敲除(Atf6−/−)减轻DEN/HFD诱导的肝癌
肿瘤负荷:与Atf6+/+对照相比,Atf6−/−小鼠肝重比、ALT水平降低,肿瘤数量及体积显著减少,脂肪变性及内质网应激减轻。
分子改变:UPR激活受抑、TRAPα低糖基化改善、FBP1水平维持,糖酵解、炎症及致癌信号通路下调。
免疫浸润:CD8+ T细胞及PD-1+细胞浸润减少(与ATF6α活化小鼠中增殖及免疫浸润增加的现象相反)。
肝细胞特异性Atf6敲除(Atf6ΔHep)的多模型验证
CD-HFD模型:58周喂养后,Atf6ΔHep小鼠肝癌发生率、肿瘤数量显著降低,肝糖原恢复、Fbp1表达上调、糖酵解通路下调,CD8+及PD-1+细胞减少。
WD±DEN模型:DEN/WD或单独WD处理的Atf6ΔHep小鼠肿瘤结节数量及体积均小于对照,肝肿大减轻。
MUP-uPA模型:在内质网应激驱动的MASH-HCC模型中,Atf6缺失降低肝重比、肝损伤及肿瘤负荷,同时BiP/Hsp90b1表达下调,而其他UPR分支(Ddit3/Atf4/Xbp1)无代偿性激活。
治疗性靶向ATF6α:GalNac-ASO-Atf6
早期干预(MUP-uPA模型4-7周龄):ASO介导的Atf6敲低(85%)消除uPA过表达引起的急性内质网应激,防止肝糖原耗竭,降低BiP、脂质积累、细胞增殖及死亡。
治疗性干预(MUP-uPA模型30-40周龄荷瘤期):ASO处理使肝细胞及肿瘤细胞中Atf6 mRNA降低72%,下调内质网应激、UPR及糖酵解靶点,显著减少肿瘤负荷。
NRASG12V加速肝癌模型:ATF6α活化加速肿瘤生长并耗竭糖原;ASO-Atf6处理缩小肿瘤体积、防止糖原耗竭、降低PD-1+细胞丰度。
核心结论
Atf6缺失(全局或肝细胞特异性)通过维持FBP1水平、抑制糖酵解及UPR、减轻免疫耗竭,在多物种肝癌模型中发挥保护作用。
肝细胞靶向GalNac-ASO-Atf6治疗能有效减轻已建立的肿瘤负荷,恢复抗肿瘤免疫反应,提示ATF6α是肝癌的潜在治疗靶点。
结果5、肝细胞ATF6α驱动免疫抑制及对ICB的增敏作用
ATF6α活化与免疫抑制微环境
转录特征:3月龄TGAlb-cre+小鼠肝脏即富集免疫抑制相关基因集(ICF、TGFβ活化、Treg细胞特征),FBP1恢复可部分逆转;人类ATF6αhi HCC富集免疫耗竭亚类特征及ICB反应预测特征(如IFNAP)。
免疫细胞组成:TGAlb-cre+肝脏中M-MDSC、PD-1+ T细胞、CD206+/PD-L1+巨噬细胞显著增加,与人类HCC观察一致。
PD-L1上调:6月龄癌前阶段即检测到肝PD-L1水平升高。
ATF6α通过代谢竞争限制CD8+ T细胞功能
scRNA-seq揭示:TGAlb-cre+肝脏CD8+ T细胞效应/耗竭亚群增加,但糖酵解及OXPHOS通路活性降低,提示葡萄糖缺乏微环境选择性抑制CD8+ T细胞代谢。
肝细胞自主性效应:
ATF6α活化肝细胞(FL83BTG)葡萄糖消耗及乳酸产生增加;
与MART-1特异性T细胞共培养时,nATF6α表达肿瘤细胞(HLE/Colo800)对T细胞杀伤抵抗;
抑制乳酸脱氢酶( galloflavin)或乳酸外排(AZD3965)可恢复T细胞杀伤效率。
机制模型:ATF6α活化肝细胞通过增强糖酵解/乳酸产生,在细胞非自主层面上抑制CD8+ T细胞抗肿瘤免疫监视。
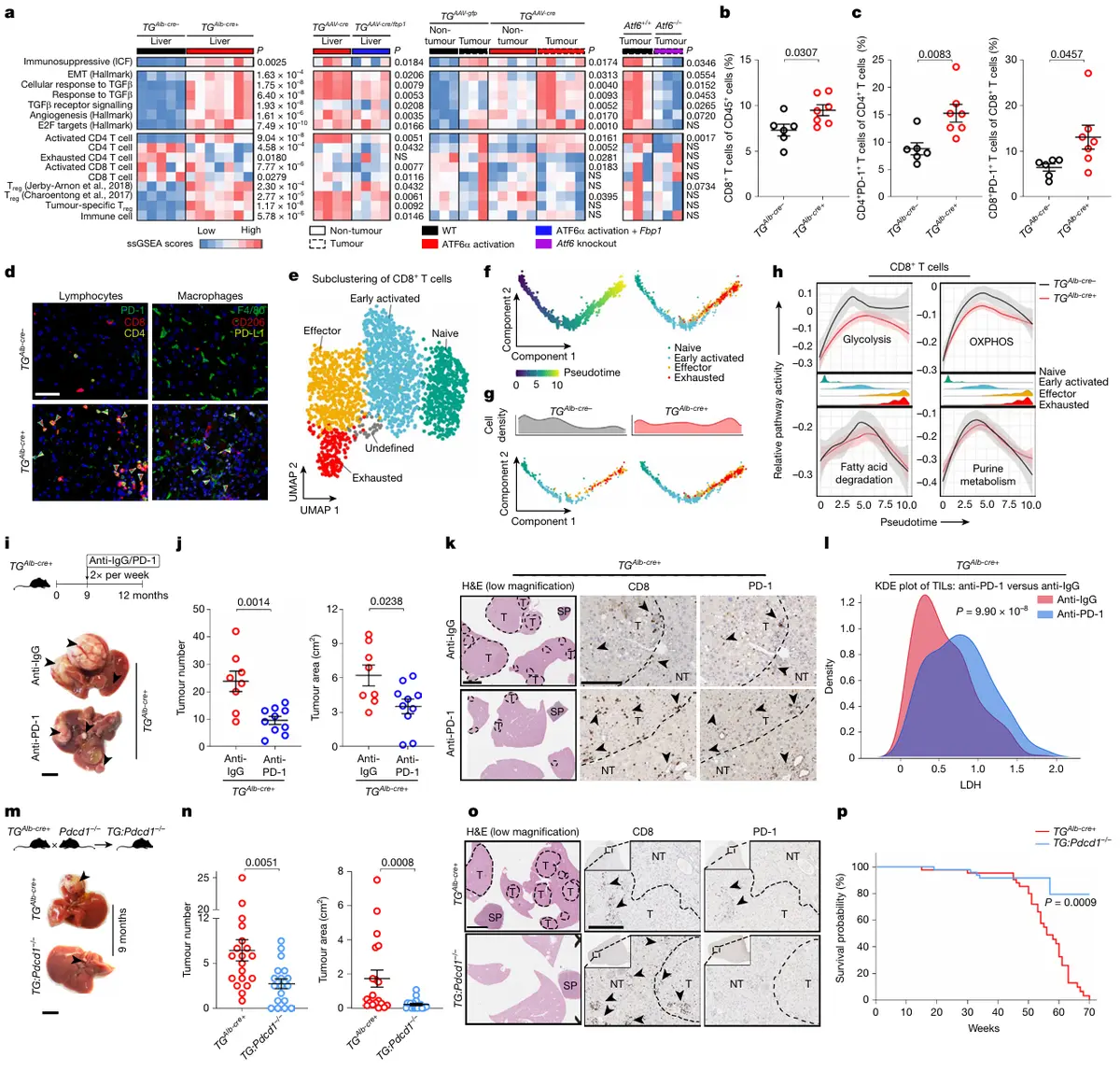
ATF6α活化使肝癌对ICB治疗敏感
自发肝癌模型(TGAlb-cre+):抗PD-1治疗减少肿瘤数量/体积,增加CD8+ T细胞浸润,MIBI显示TIL中LDH表达升高(提示代谢恢复)。
致癌基因诱导模型(MYC:TP53KO / KRASG12D:TP53KO):
单独抗PD-1无效,但联合AAV-ATF6α活化后,抗PD-1显著降低肿瘤负荷、延长生存;
响应ICB的肿瘤中CD8+ TIL糖酵解能力增强。
遗传性PD-1敲除(TG:Pdcd1−/−):
肿瘤数量/体积显著减少,CD8+ TIL浸润增加、效应表型比例升高、LDH表达增强;
生存期延长,而ATF6α活化水平及肝损伤无改变。
核心结论
肝细胞ATF6α活化通过代谢重编程(增强糖酵解/乳酸产生)塑造免疫抑制微环境,限制CD8+ T细胞功能。
然而,ATF6α活化同时赋予肿瘤对ICB治疗的敏感性,其机制可能包括:①形成ICB响应的免疫微环境结构(CD8+ T细胞与DC/CD4+ T细胞聚集、与Treg空间分离);②ICB解除T细胞代谢抑制(恢复糖酵解)。
ATF6α活化状态可作为预测肝癌ICB疗效的生物标志物,并为联合治疗策略(靶向ATF6α + ICB)提供理论依据。
最后来看看方法,当然有单细胞、ATAC、IMC、MIBI多组学。

生活很好,有你更好。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

