文献分享--口腔黏膜免疫受独特的空间结构调控
原创文献分享--口腔黏膜免疫受独特的空间结构调控
原创
追风少年i
发布于 2026-02-21 15:24:34
发布于 2026-02-21 15:24:34
作者,Evil Genius
今天我们分享文献

知识积累
屏障组织(如皮肤、胃肠道和呼吸道)持续暴露于外界环境中。它们既要提供与外部世界的物理隔离,又要整合复杂的环境信号,以执行监视功能并抵御外来侵害,同时忽略或主动耐受无害抗原与共生微生物。
口腔黏膜是一种尤为特殊的暴露屏障表面。作为宿主的第一道接触界面,食物、共生微生物及空气微粒均通过此门户进入人体。与皮肤不同,口腔黏膜表面大多角化程度极低且缺乏黏膜下淋巴组织,却承载着丰富多样的共生微生物群落。
剖析环境与宿主之间的平衡在口腔黏膜最脆弱部位——牙相关上皮处尤为重要。
结果1、人类牙龈整合多组学图谱构建
空间蛋白质组学分析:采用迭代漂白扩展多重染色技术,使用专为口腔组织优化的18参数抗体组合
空间转录组学分析:采用Xenium平台搭配450个基因的探针组合,其中包含基于前期单细胞测序数据定制的探针。
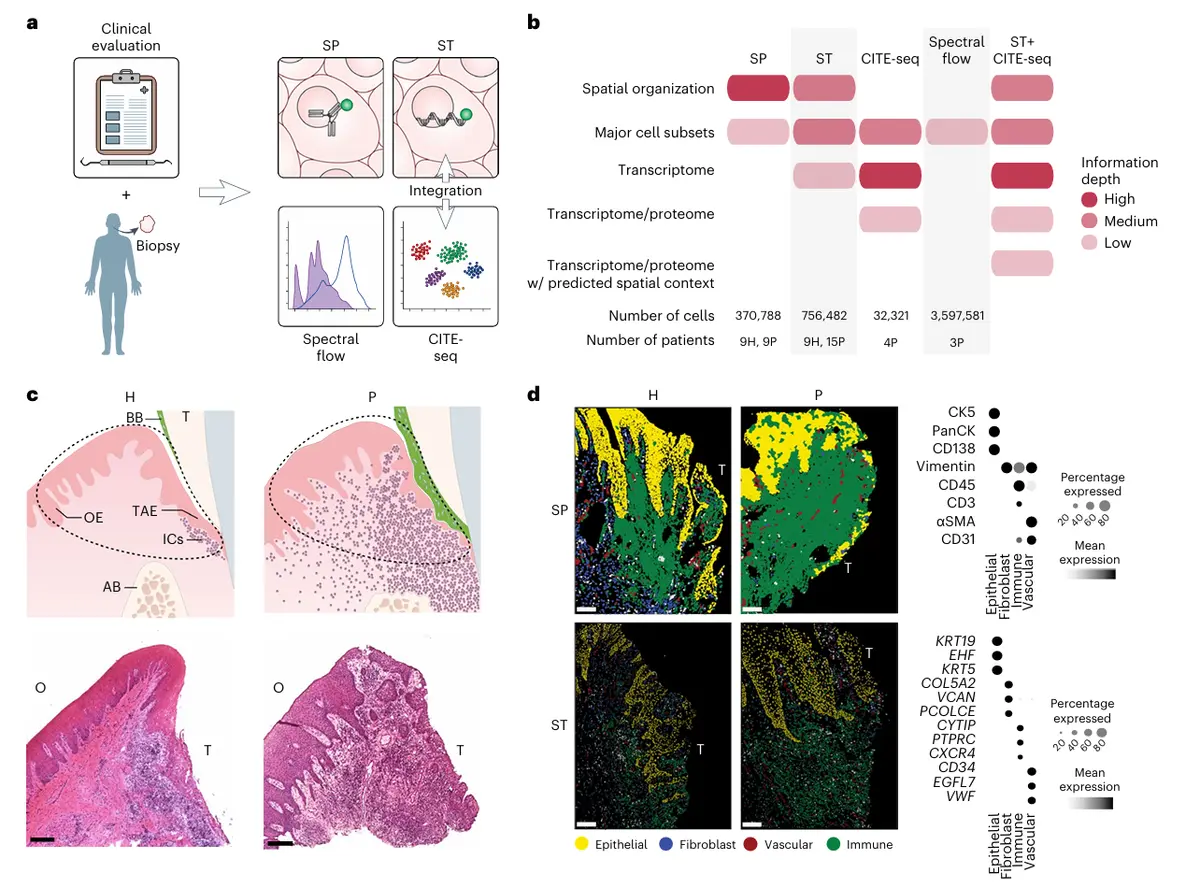
结果2、空间蛋白质组学与转录组学解析细胞分布格局
同时运用空间蛋白质组学与空间转录组学技术,以界定健康及病变牙龈中的细胞区室及其空间分布。
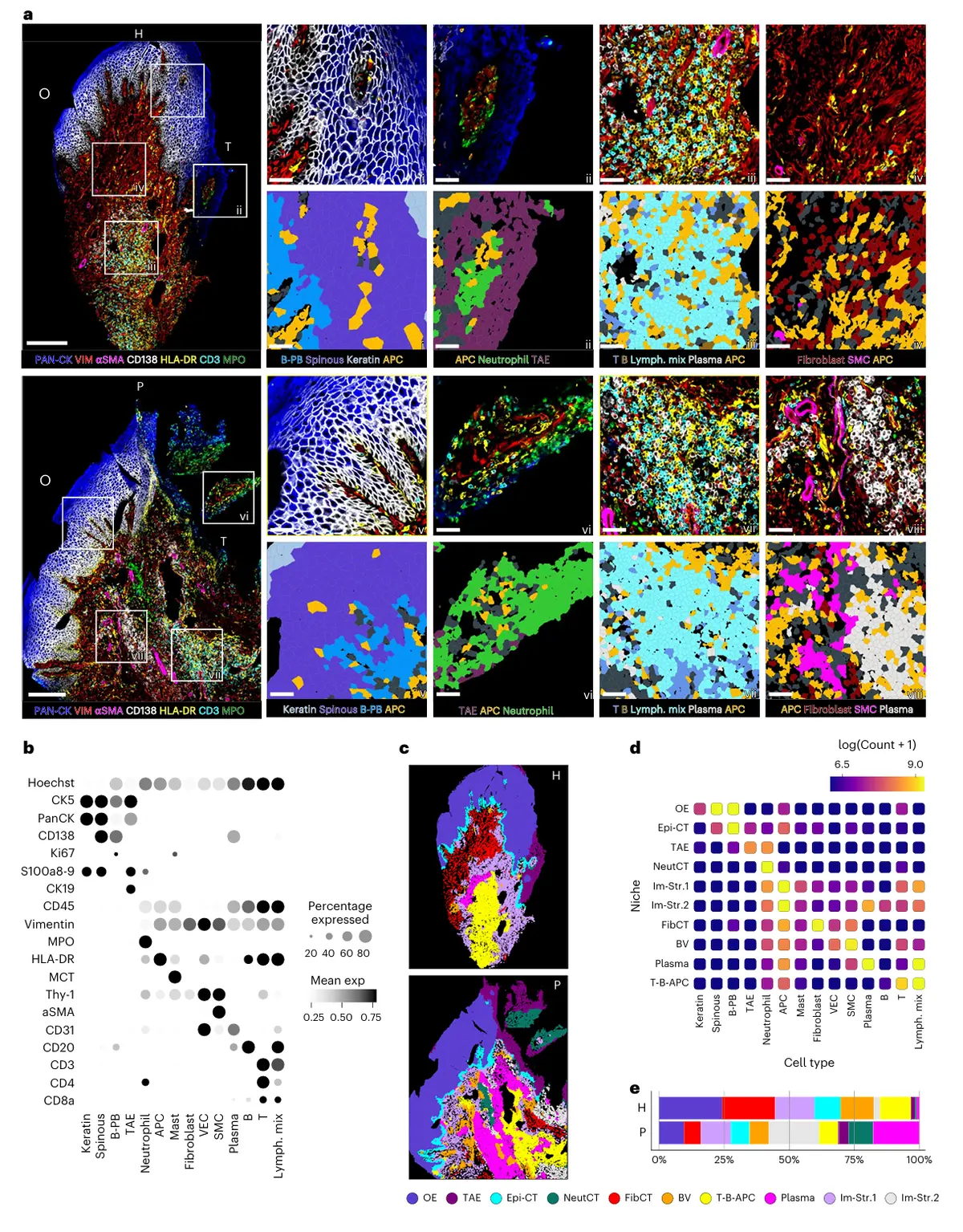
结果3、牙相关上皮区以中性粒细胞为主导的炎症反应
牙相关上皮的结构与功能特性
解剖特征
牙相关上皮(TAE)非角化、单层/薄层结构,缺乏口腔上皮(OE)的复层角化特征。
表达CK19但缺失CD138,提示细胞连接松散、屏障渗透性高。
微生物暴露
紧邻牙面生物膜,微生物可穿透上皮进入上皮下空间(健康与疾病状态下均存在)。
中性粒细胞为主导的免疫巡逻机制
中性粒细胞浸润
健康状态下TAE即存在中性粒细胞(MPO⁺)浸润,形成上皮下免疫哨兵层。
牙周炎期间中性粒细胞数量急剧增加,在上皮下形成密集分界带。
上皮主动调控
TAE组成性表达中性粒细胞趋化因子(CXCL1/2/6),主动招募中性粒细胞。
表层TAE特异性高表达IL1A、IL36G等促炎细胞因子。
TAE独特的转录组特征
免疫相关基因富集
高表达急性期反应蛋白(SAA1/2)、补体因子(CFH/CFHR3)及炎症调控因子(DNASE1L3)。
缺乏角化标志(如CNFN),但表达半桥粒附着蛋白(LAMC2)以维持牙面附着。
跨屏障比较
相较于皮肤、肺、肠道等其他屏障上皮,TAE呈现独特的炎症预备状态:
核心通路:“抗菌反应”“中性粒细胞趋化”“白细胞聚集”。
功能定位:处于持续低度炎症的免疫激活状态,以快速应对微生物挑战。
生物学意义
双重角色:TAE既是物理屏障,又是主动免疫调控界面。
健康与疾病平衡:
健康时:维持可控炎症,实现免疫监视与微生物共存。
病变时(如牙周炎):炎症扩大但罕见系统性感染,体现局部免疫的精准调控能力。
临床启示:TAE的“炎症预备状态”可能是口腔黏膜高效抗感染、快速愈合且不留瘢痕的分子基础。
牙相关上皮通过结构性渗透性、组成性表达趋化因子及中性粒细胞常驻巡逻,构建了一个独特的前线免疫微环境。这种“常备不懈”的免疫状态,使其能在暴露于高微生物负荷的同时,维持屏障稳态并快速响应损伤,揭示了口腔黏膜免疫适应性的组织特异性策略。
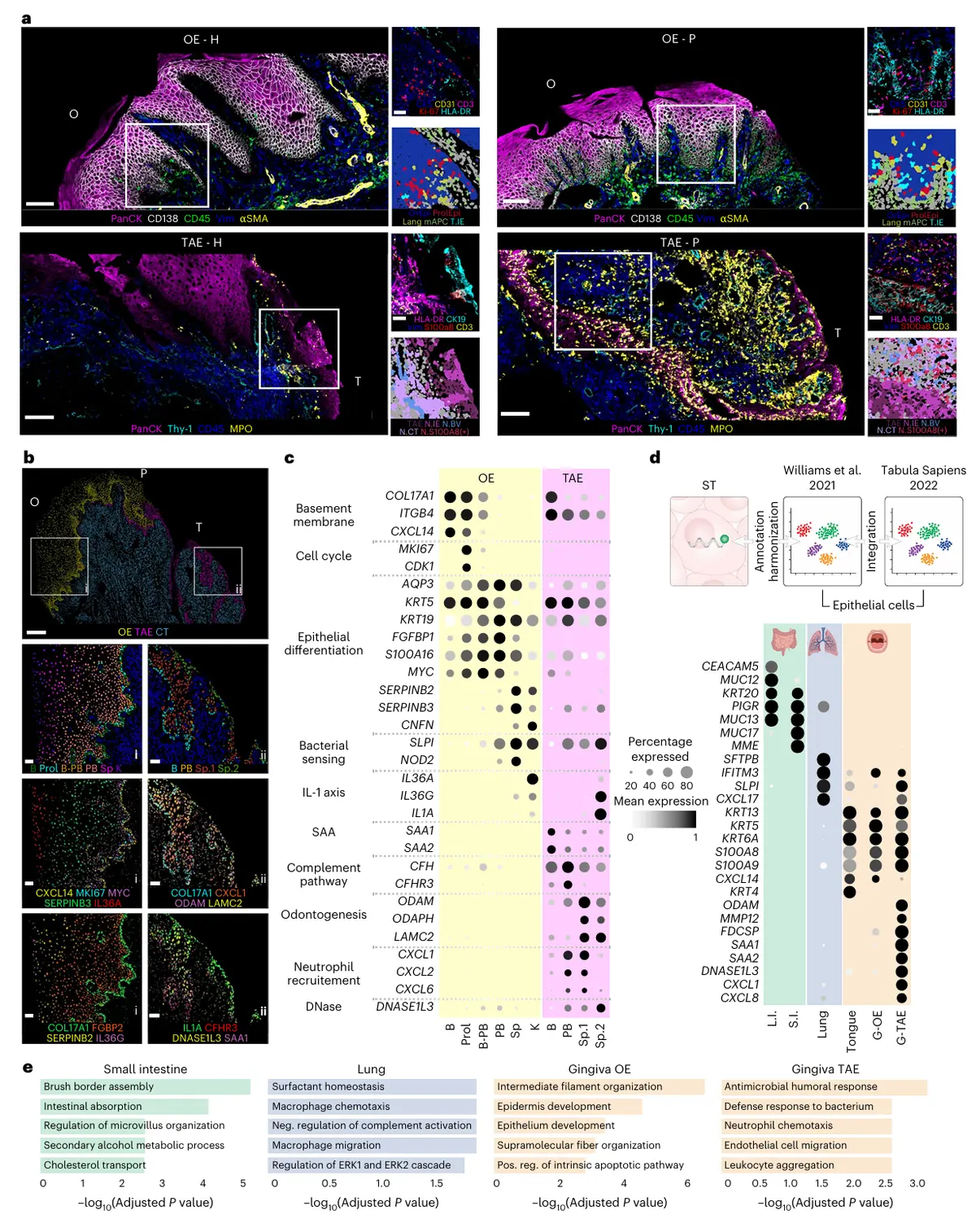
结果4、牙相关上皮区域的独特免疫分区结构
空间结构层次(由近及远)
第一层:中性粒细胞结缔组织区(NeutCT)
位置:最靠近牙相关上皮
特征:
健康与疾病状态下均存在,结构位置稳定
疾病期中性粒细胞数量剧增并向深层延伸
第二层:T-B-APC区
位置:位于中性粒细胞区外侧
细胞组成:
辅助性T细胞(CD4⁺)
B细胞(CD20⁺)
抗原呈递细胞(HLA-DR⁺)
疾病期扩展至更深区域,但细胞总量与健康期相近
第三层:浆细胞区
位置:上皮下组织最深层(T-B-APC区远端)
特征:
仅在疾病期明显形成
含CD138⁺浆细胞、浆母细胞(Ki67⁺)及T细胞
健康与疾病状态对比
特征 | 健康状态 | 疾病状态(如牙周炎) |
|---|---|---|
中性粒细胞区 | 存在,数量较少 | 细胞数量大幅增加,向深层浸润 |
T-B-APC区 | 存在,范围较浅 | 向深层延伸,细胞组成更复杂 |
浆细胞区 | 无明确聚集,细胞分散在结缔组织中 | 明显形成结构化聚集区 |
深层结缔组织 | 主要为纤维血管组织,免疫细胞稀少 | 出现免疫-基质混合微环境(Im-Str) |
空间转录组学的精细解析
T-B-APC区细胞亚群
B细胞(表达MS4A1/BANK1)
辅助性T细胞(表达CD4/TRAC)
成熟调节性树突状细胞(mregDCs,表达CD83/LAMP3)
邻近B细胞的T细胞亚群(TH.B)
浆细胞区细胞亚群
浆细胞亚群(Pl.1/Pl.2)
浆母细胞
特异性成纤维细胞亚群(Fib.2):
- 表达趋化因子(CXCL12、CCL19)
- 表达补体基因(C3、CFB)
核心发现
稳定的空间层级:
免疫细胞在TAE外侧呈现 “中性粒细胞区 → T-B-APC区 → 浆细胞区” 的同心圆式分层布局,且该基本框架在健康与疾病中保持稳定。
疾病的适应性改变:
量的扩张:中性粒细胞与浆细胞数量增加
质的重组:浆细胞区结构化、出现淋巴样聚集体、成纤维细胞获得免疫调节功能
基质细胞的主动参与:
疾病中成纤维细胞亚群(Fib.2) 通过表达趋化因子与补体基因,可能协助浆细胞区形成与维持。
生物学意义
屏障防御策略:分层布局实现 “前线吞噬(中性粒细胞)→ 适应性免疫启动(T/B/APC)→ 抗体生产(浆细胞)” 的阶梯式防御。
病理适应机制:疾病状态下通过扩增现有层级而非破坏基本结构,维持屏障功能的同时增强免疫应答。
治疗启示:靶向特定免疫层级的细胞动态(如浆细胞区的形成)可能为慢性炎症疾病提供新策略。
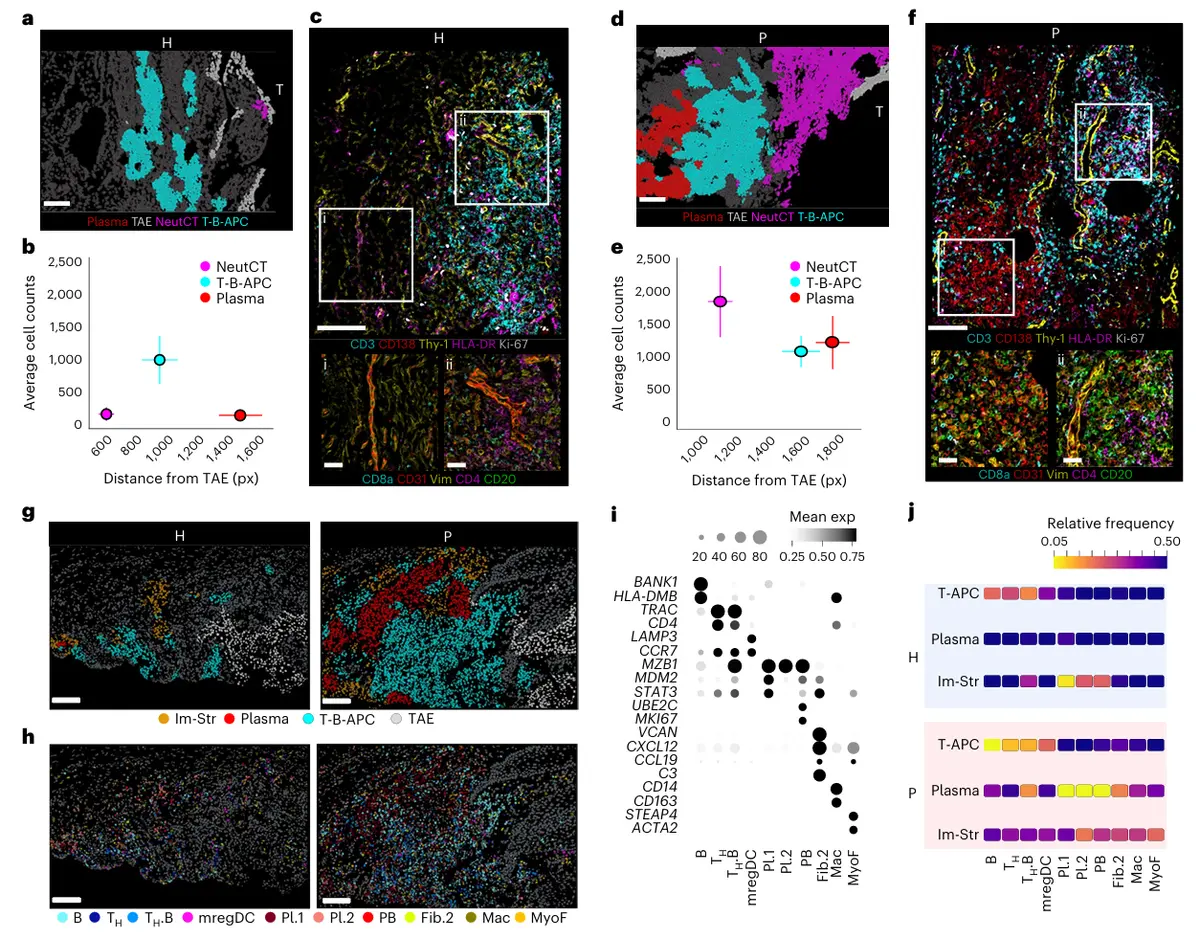
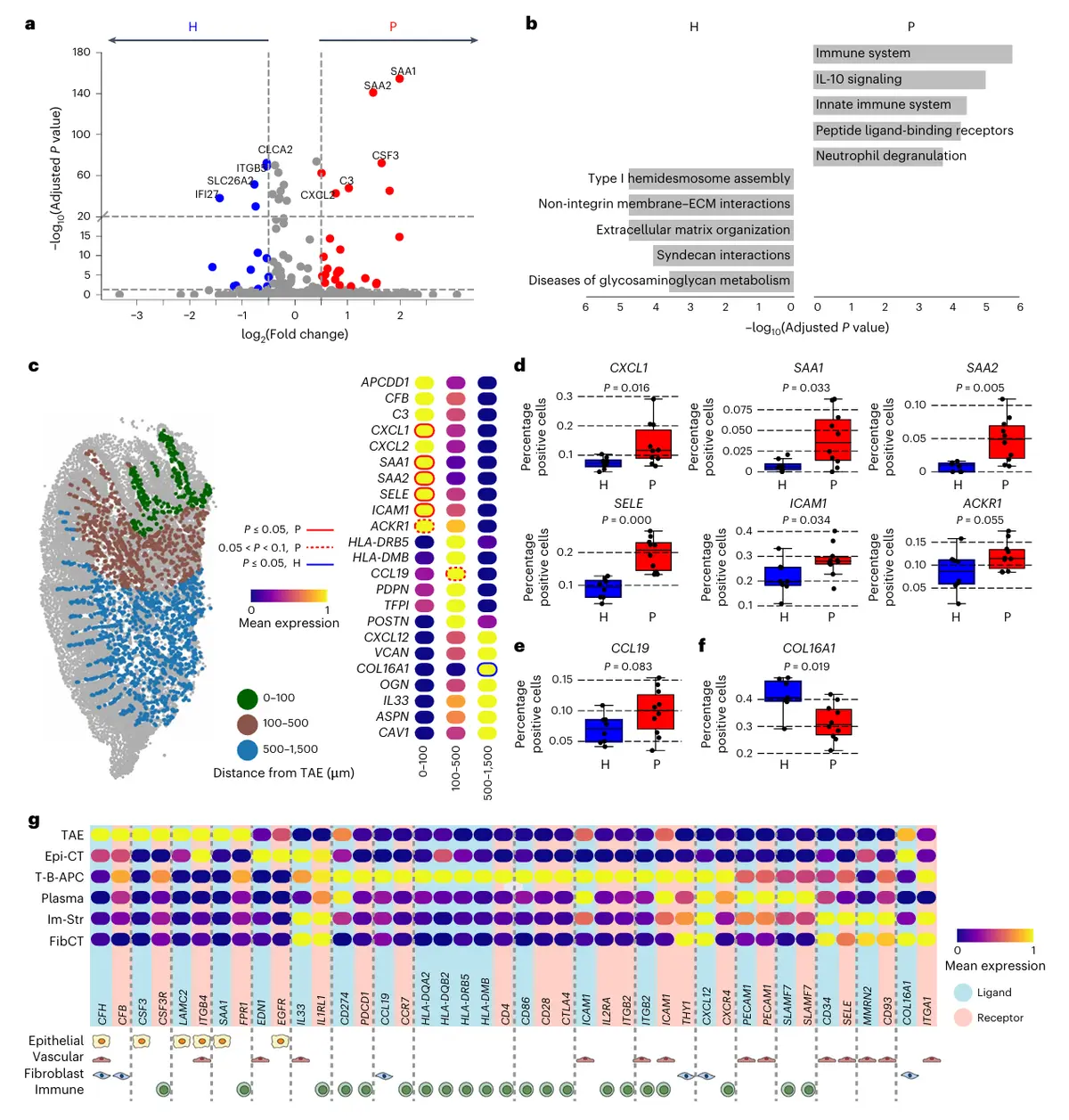
结果5、上皮与基质区室协同构建免疫分层结构
TAE上皮细胞的核心调控作用
基因表达特征
疾病状态下TAE显著上调:
先天免疫调节分子(SAA1/2、C3)
中性粒细胞趋化因子(CXCL2、CSF3)
通路富集分析:
疾病TAE富集 “先天免疫系统”、“中性粒细胞脱颗粒” 等通路
功能解读
TAE通过释放趋化信号 主动招募并活化中性粒细胞,形成 “第一道免疫防线”。
基质细胞的空间特异性贡献
距离分区 | 关键表达基因 | 推断功能 |
|---|---|---|
近端(0–100 μm) | SELE、ICAM1(黏附分子);CXCL1/2、SAA1/2(趋化/急性期蛋白) | 协同TAE强化先天免疫应答,促进中性粒细胞募集与黏附 |
中段(100–500 μm) | HLA-DRB5/DMB(抗原呈递);CCL19(三级淋巴结构形成) | 支持淋巴聚集区形成,参与适应性免疫启动 |
远端(500–1500 μm) | CXCL12(免疫细胞趋化因子) | 募集远端免疫细胞,维持免疫细胞稳态分布 |
疾病特异性变化:
近端区:先天免疫分子(SAA、CXCL1)及内皮黏附分子(SELE、ICAM1)上调
中段区:趋化因子CCL19上调
远端区:健康状态下结构基因(COL16A1)显著高表达
成纤维细胞与血管细胞的微环境特异性功能
Fib.2成纤维细胞亚群(主要位于浆细胞区):
表达 CXCL12、CCL19、补体基因,可能协助浆细胞区形成与维持。
血管细胞:
在近TAE区域表达黏附分子,促进免疫细胞外渗。
细胞间通讯网络的空间特异性
免疫分区 | 关键配体-受体对 | 功能意义 |
|---|---|---|
TAE区 | CSF3–CSF3R、SAA1–FPR1 | 驱动中性粒细胞募集与活化 |
T-B-APC区 | CD274–PDCD1、CCL19–CCR7、CXCL12–CXCR4; HLA-DR–CD4、CD28/CD80–CTLA4 | 促进三级淋巴结构形成、抗原呈递与共刺激信号 |
浆细胞区 | SLAMF7(自分泌/旁分泌信号) | 维持浆细胞存活与功能 |
整体机制模型
分层化免疫组织原则:
TAE上皮 → 释放先天免疫信号 → 近端基质细胞协同放大 → 形成中性粒细胞前线
↓
中段基质细胞 → 表达淋巴组织趋化因子 → 形成T/B/APC聚集区
↓
远端基质细胞 → 提供趋化维持信号 → 促进浆细胞区形成
疾病适应模式:
炎症状态下,上皮与基质细胞同步上调免疫调节基因,在不破坏基本分层结构的前提下,增强各层级的防御功能。
生物学与临床意义
揭示黏膜免疫的组织逻辑:
免疫分层并非仅由免疫细胞自主完成,而是 “上皮-基质-免疫细胞”三位一体的协同构建结果。
提供慢性炎症治疗新思路:
靶向上皮或基质细胞的位置特异性信号(如TAE区的CSF3、浆细胞区的CXCL12),可能精准调控特定免疫层级,避免全局免疫抑制。
阐释疾病耐受机制:
即使在重度炎症(如牙周炎)中,分层结构仍保持稳定,这可能是口腔黏膜能长期应对高微生物负荷而不发生系统性扩散的结构性基础。
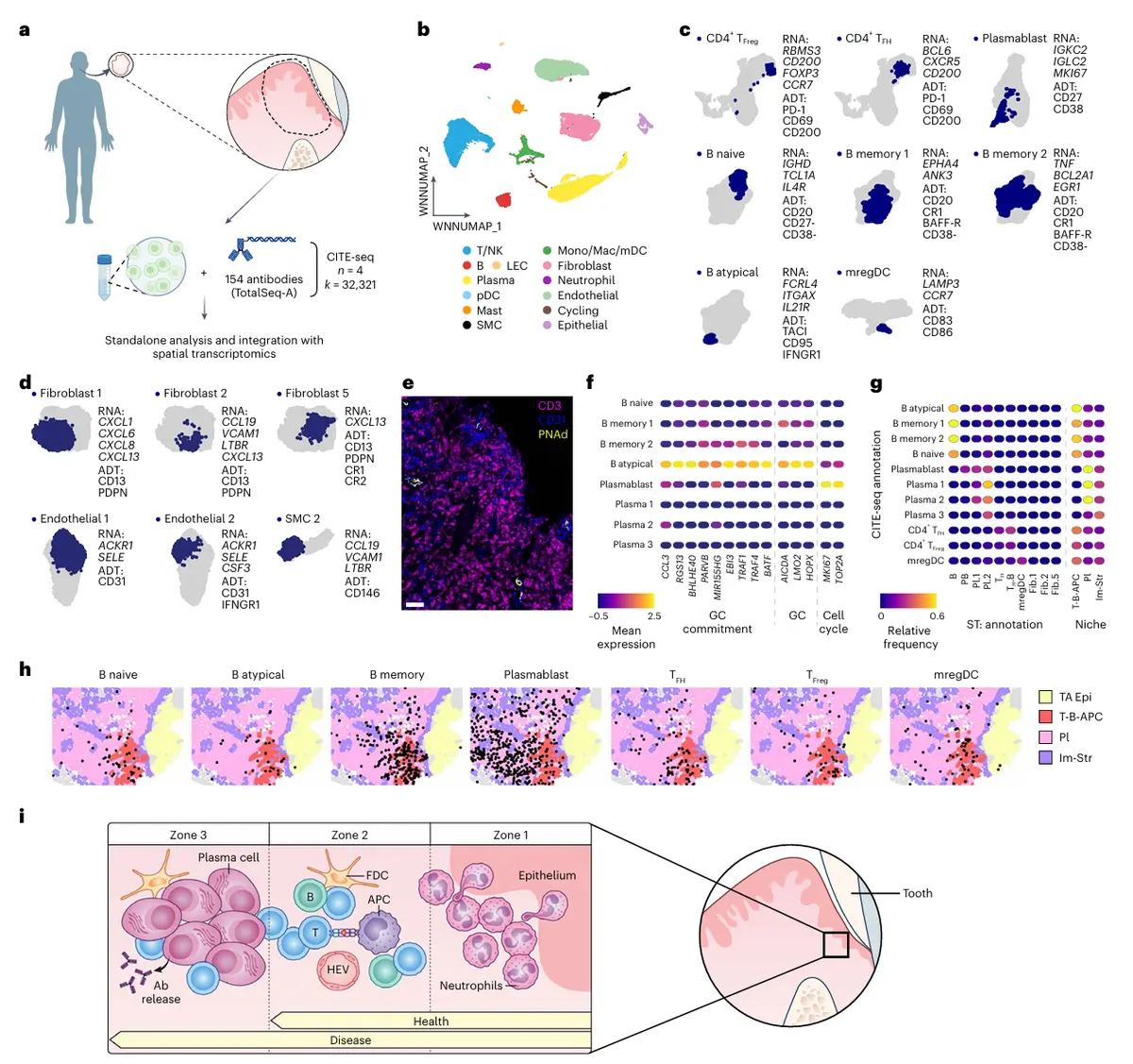
结果6、牙周炎中三级淋巴结构的形成
在牙周炎的T细胞区室中,我们鉴定出与三级淋巴结构相关的细胞类型,包括:
滤泡辅助性T细胞(CD4⁺ TFH;特征:PRDM1⁻、BCL6⁺、CXCR5⁺、CD200⁺)
滤泡调节性T细胞(CD4⁺ TFreg;特征:PRDM1⁻、RBMS3⁺、CD200⁺、FOXP3⁺)
这两种细胞均表达PD-1、CD69及CD200表位。B细胞成熟全过程也被完整注释,涵盖:
初始B细胞(IGHD⁺、TCL1A⁺、IL4R⁺、CD20⁺、CD27⁻、CD38⁻)
两类记忆B细胞(CD20⁺、CR1⁺、BAFF-R⁺、CD38⁻)
非典型B细胞(FCRL4⁺、ITGAX⁺、IL21R⁺、TACI⁺、CD95⁺、IFNGR1⁺)
通过整合多组学方法,我们揭示了牙相关上皮邻近区域在健康与疾病状态下均保持的独特免疫分层结构,并在炎症性疾病中发现了具有支持局部抗体产生潜能的不成熟三级淋巴结构的形成
最后来看看方法


生活很好,有你更好。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

