文献分享--通过多重免疫荧光技术对肿瘤免疫互作进行代谢表征揭示非小细胞肺癌免疫治疗反应的空间作用机制
原创文献分享--通过多重免疫荧光技术对肿瘤免疫互作进行代谢表征揭示非小细胞肺癌免疫治疗反应的空间作用机制
原创
追风少年i
发布于 2026-02-10 10:05:00
发布于 2026-02-10 10:05:00
作者,Evil Genius
小年了,怎么感觉现在一点年味都没有。
今天我们分享文献

知识积累
目前主流的免疫检查点抑制剂(如抗PD-1/PD-L1和抗CTLA-4疗法)旨在阻断T细胞抑制信号和肿瘤介导的自身免疫耐受。耐药机制复杂多样,主要包括:肿瘤新抗原生成不足、抗原呈递功能受抑制、抗原呈递细胞募集受阻、T细胞迁移障碍、T细胞耗竭、肿瘤微环境缺氧、T细胞活化受损以及PD-L1剪接变异体逃逸PD-1阻断等。
结果1、患者特征与队列选择
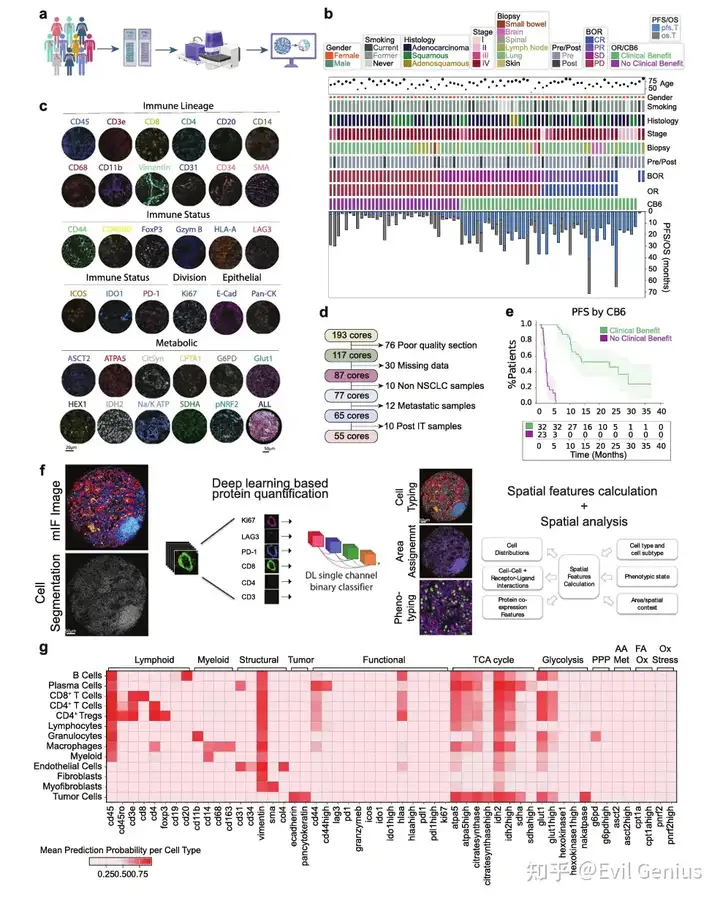
结果2、细胞类型比例分析
一、细胞组成特征
肿瘤微环境构成
肿瘤细胞占比为10%-90%,巨噬细胞与CD4⁺ T细胞是主要免疫成分
成纤维细胞与肌成纤维细胞显著参与组织结构形成
功能表达模式
肿瘤细胞表达IDO1、PD-L1、HLA-A等功能标记
巨噬细胞呈现最广泛的功能标记阳性表达(包括代谢与免疫调节标记)
代谢标记分析显示肿瘤与免疫细胞均存在活跃的氧化磷酸化(OXPHOS)代谢表型
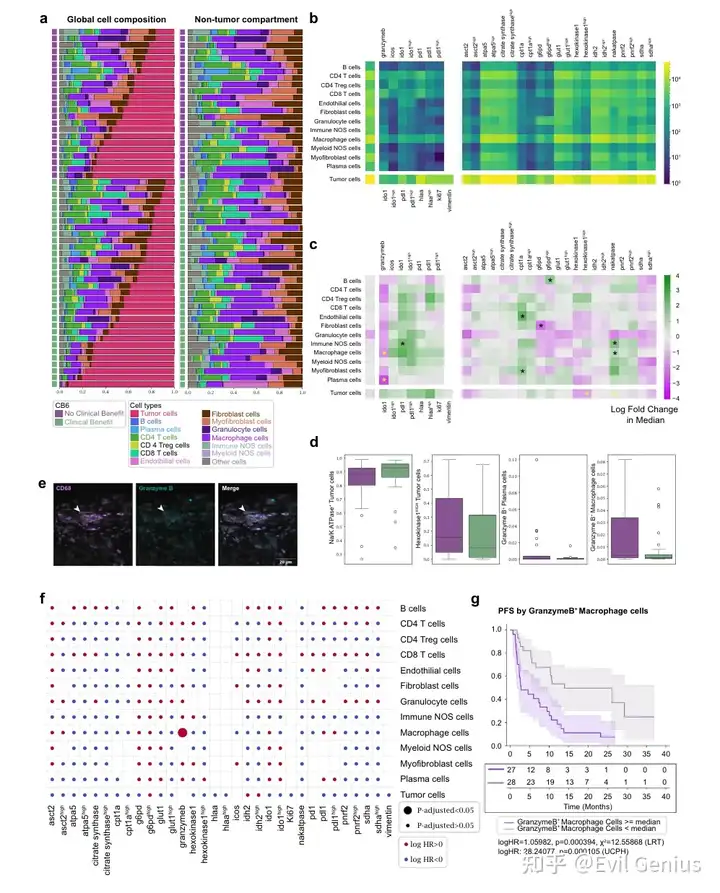
二、临床获益相关的细胞亚群
通过统计学比较临床获益(CB)与非临床获益(NCB)患者群体,发现:
CB患者富集特征
高能量需求型免疫细胞:Na⁺/K⁺ ATPase⁺/IDO1⁺ 免疫非特指细胞、CPT1a⁺ 内皮/肌成纤维细胞
代谢活跃的免疫细胞:G6PDᴴᴵᴳᴴ B细胞、Na⁺/K⁺ ATPase⁺ 巨噬细胞
NCB患者富集特征
细胞毒性相关细胞:颗粒酶B⁺ 浆细胞、颗粒酶B⁺ 巨噬细胞
促肿瘤代谢表型:G6PD⁺ 成纤维细胞、己糖激酶1ᴴᴵᴳᴴ 肿瘤细胞
不良预后相关代谢表型:ASCT2⁺(氨基酸代谢)与SDHA⁺(三羧酸循环)肿瘤细胞在早期复发(<6个月)患者中显著升高
三、关键预后预测因子
经多重检验校正后,颗粒酶B⁺ 巨噬细胞被确定为唯一与ICI治疗不良结局显著相关的独立预测因子:
其高表达与更短的无进展生存期(PFS)直接相关
提示该细胞亚群可能通过细胞毒性作用或免疫抑制微环境促进治疗抵抗
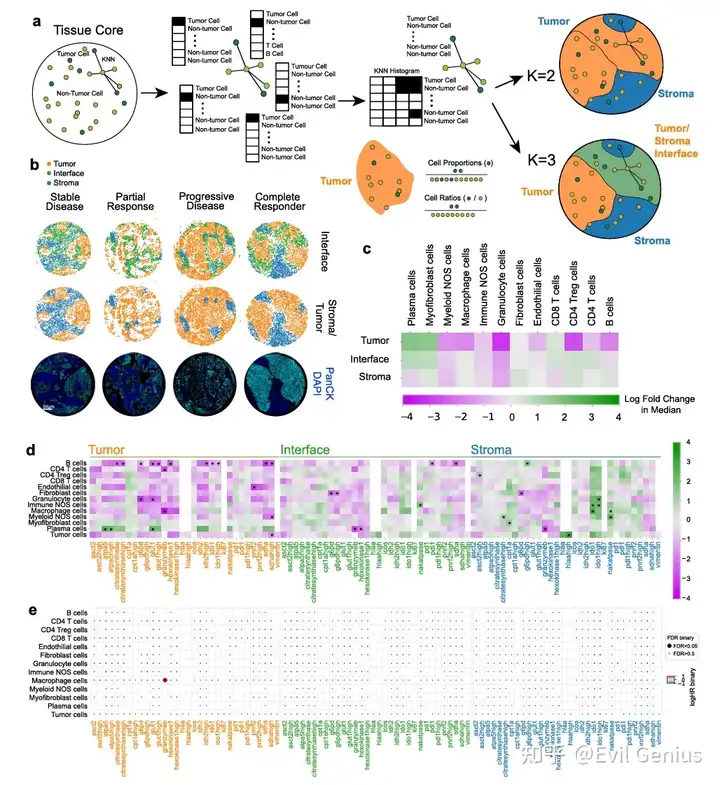
结果3、组织区域解析
采用细胞邻域(CNs)方法构建无偏倚的组织区域划分。
K=2模型:区分肿瘤区域与基质区域
K=3模型:额外解析肿瘤-基质界面区域,该区域被认为是功能性免疫细胞与代谢梯度影响治疗响应的关键区域
肿瘤区域内的细胞分布与临床关联
有益趋势
浆细胞浸润增加与临床获益趋势相关
不利趋势
粒细胞与CD4⁺调节性T细胞浸润增多与治疗响应呈负相关
代谢高度活跃的B细胞(同时高表达GLUT1、G6PD/己糖激酶1、Ki67)提示存在:
高糖酵解表型
磷酸戊糖途径激活
氧化磷酸化水平升高(通过柠檬酸合酶、IDH2、SDHA高表达反映)
此类细胞在肿瘤区域富集与ICI耐药相关
粒细胞表达G6PD与GLUT1同样提示不良预后
颗粒酶B⁺巨噬细胞被定位于肿瘤区域,其富集与早期复发显著相关(经FDR校正验证)
例外情况
肿瘤区域内浆细胞表达OXPHOS酶(ATPA5与GLUT1)显示有益作用,可能通过促进局部抗体分泌增强ICI响应
交界区域的独特发现
在肿瘤-基质界面区域:
不利特征
表达G6PDᴴᴵᴳᴴ的成纤维细胞富集于无响应患者
表达颗粒酶B与己糖激酶1的浆细胞、表达PD-1与SDHA的B细胞均与较差结局相关
有益特征
粒细胞、免疫非特指细胞及巨噬细胞中色氨酸途径酶IDO1的表达
肿瘤细胞HLA-A的表达
二者均与较好预后相关,提示低炎症基质微环境可能有利于治疗
免疫细胞比值分析
肿瘤区域内粒细胞/CD8⁺ T细胞高比值与复发相关
基质区域B细胞/肿瘤区域肌成纤维细胞(及免疫细胞)高比值同样提示不良预后
界面区域粒细胞/基质B细胞高比值与较差结局相关
结果4、代谢微区域分析
采用基于细胞邻域(CNs)的代谢密度聚类方法识别代谢微区域(MBNs)。共定义四种特征鲜明的聚类:代谢活性极低、低、中等(含调节性活性)及高代谢活性区域。这些微区域描述了具有不同代谢通路活性的组织区域:高MBN区域显示高SDHA表达,低MBN区域则呈现低CPT1a表达,分别对应高能量需求与低能量需求状态。
高活性MBN中肿瘤细胞增多与不良预后相关,而低活性MBN中粒细胞存在同样提示较差结局。
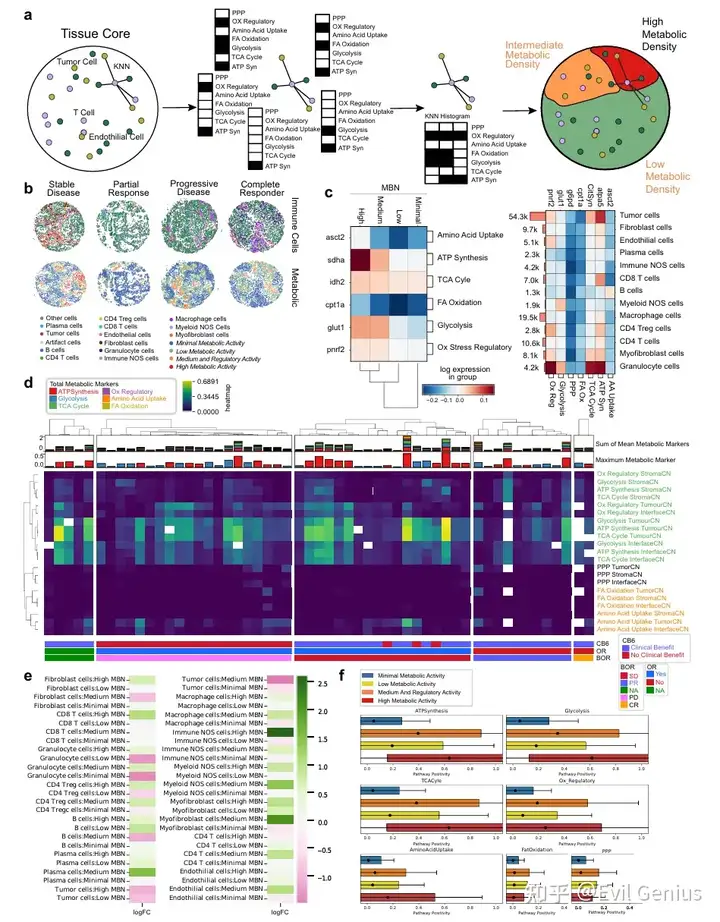
结果5、组织架构的高阶特征建模
基于肿瘤区域或代谢区域定义的细胞频率分析基础上,进一步通过构建综合性特征生成流程深化分析层次。该流程整合了区域属性与细胞间相互作用及空间邻近特征,系统刻画了组织微架构的多维度信息。
特征工程构建
多尺度空间特征
设计了描述基础细胞类型、功能表型及代谢表型在组织芯片核心内不同距离尺度下的密度、邻近度与相对聚类程度的特征体系。
多层次区域整合
特征计算涵盖:
K=2与K=3细胞邻域模型下的所有细胞类型(包括免疫与肿瘤功能亚型)比例及比例比值
四种代谢微区域(MBNs) 内的细胞分布特征
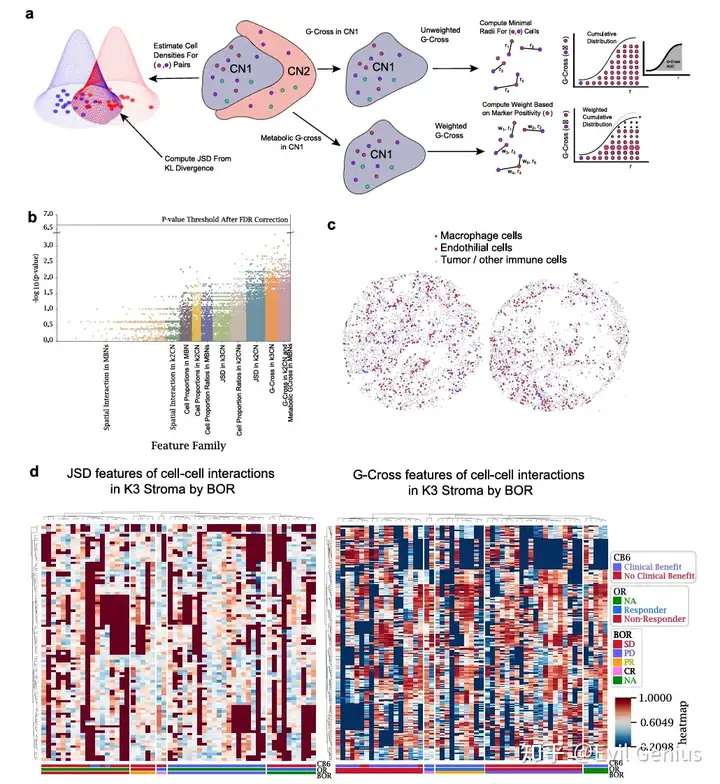
相互作用与邻近性量化
JSD Score特征:通过细胞类型概率分布重叠度的对称归一化度量,刻画大规模细胞相互作用与空间重叠模式
G-Cross特征:基于细胞/细胞或功能/代谢类型在150μm半径内的最近邻累积径向分布曲线下面积,捕捉局部细胞邻近性
边界细胞特征:通过构建各细胞邻域的凹包定义边缘细胞,计算跨邻域的边界细胞G-Cross值,以量化局部边界聚集效应
SCIMAP空间互作度量:在100μm半径内计算各细胞邻域内表型间的局部相互作用强度
特征筛选与统计验证
初步单变量分析
采用曼-惠特尼U检验评估所有工程化特征与患者治疗响应的关联,发现不同特征类型与特征家族间的单变量P值存在显著差异。
多重检验校正结果
经本杰明-霍奇伯格校正后,无一特征达到错误发现率阈值,表明需采用更先进的统计方法进行生物标志物挖掘与预后建模。
相互作用特征的变异性
与单纯的细胞/功能/代谢比例特征相比,JSD与G-Cross等相互作用相关特征在P值上表现出更高变异性。例如:
巨噬细胞与内皮细胞高度混合时呈现最大JSD值(概率分布重叠最高)
巨噬细胞远离内皮细胞自我聚集时呈现最小JSD值(重叠度最低)
关键发现与启示
对细胞间相互作用的JSD与G-Cross特征谱分析显示,仅基于基础细胞类型相互作用无法在患者响应维度形成明显特征趋势。这提示:
需要引入功能与代谢分层信息以增强特征空间的生物学判别力
高阶空间组织模式可能比简单细胞共存更具预后预测价值
必须采用多变量建模方法整合复杂空间特征以构建稳健预测模型
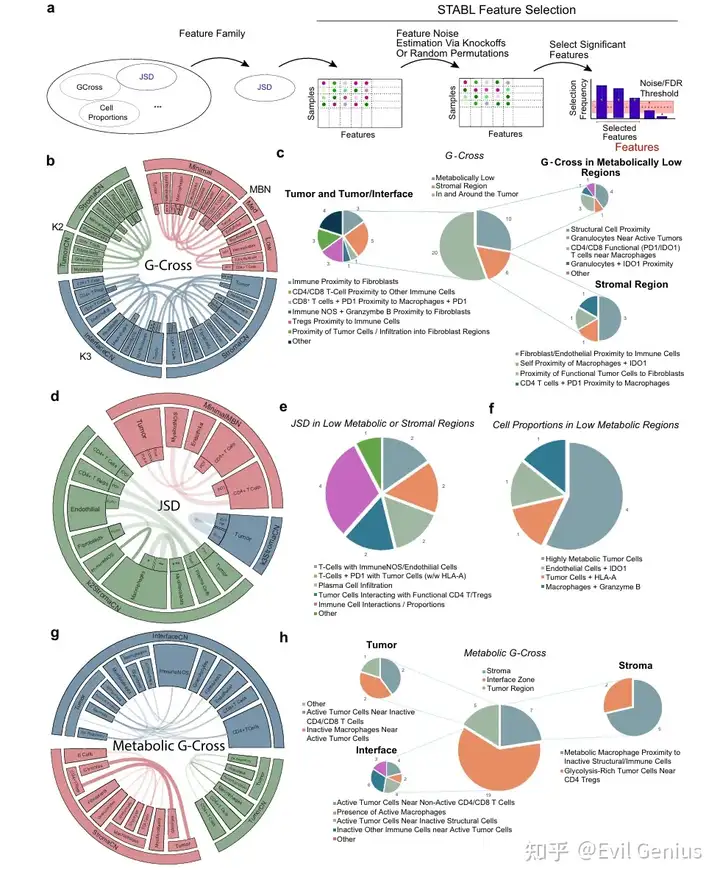
结果6、临床获益空间特征筛选
通过稳定特征选择方法,从复杂空间特征中识别出关键细胞空间相互作用模式,揭示了:
免疫-基质界面的可及性与免疫启动状态对治疗获益至关重要
代谢活性与细胞空间定位的耦合是影响ICI应答的核心因素之一
特定细胞邻接关系(如PD-1⁺ T细胞与肿瘤细胞邻近)可能促进免疫逃逸
这些空间特征为理解免疫治疗应答与抵抗的微环境动态提供了新视角,并为开发基于空间生物学的新型预测模型奠定基础。
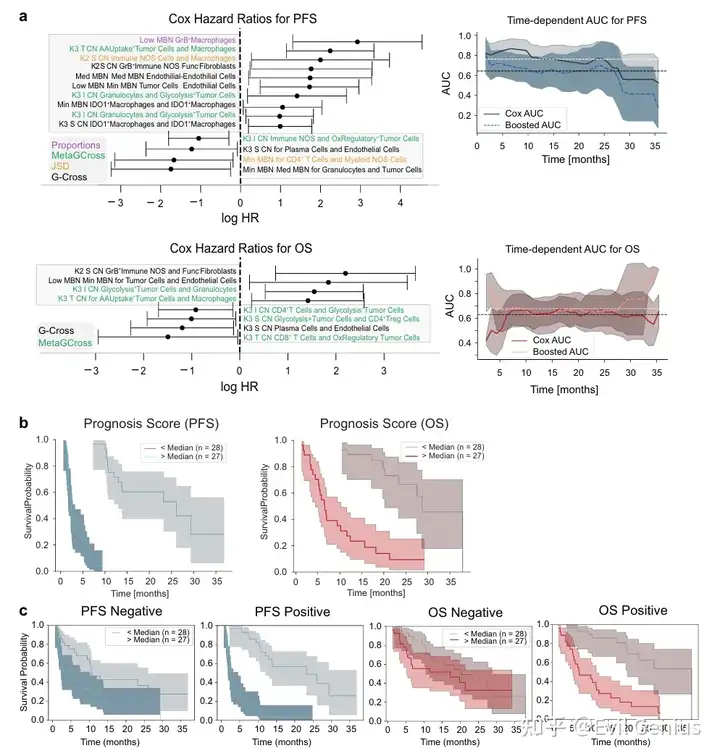
结果7、基于选定特征的生存预测
通过Cox比例风险回归分析,从筛选出的空间特征中构建了预测非小细胞肺癌患者免疫治疗预后的模型。结果显示,肿瘤细胞与巨噬细胞的G-Cross相互作用及低代谢区域内颗粒酶B⁺巨噬细胞频率是预测疾病进展的关键特征。该模型在预测24个月无进展生存期(PFS)时曲线下面积(AUC)达0.8,总体生存期(OS)预测AUC为0.7。跨队列验证表明,特征在不同独立队列中具有泛化性,其中ICOS⁺调节性T细胞与成纤维细胞在肿瘤界面区域的相互作用提示T细胞排斥,而CD4⁺调节性T细胞与基质区糖酵解型肿瘤细胞的互作则暗示免疫抑制微环境。同时,低代谢区域中IDO1⁺或颗粒酶B⁺巨噬细胞的自身聚集与不良预后相关。
最后来看看方法

生活很好,有你更好。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

