PSA重组兔单抗如何提升前列腺癌诊疗的精准度?
原创PSA重组兔单抗如何提升前列腺癌诊疗的精准度?
原创
STARTER
发布于 2026-02-10 09:30:41
发布于 2026-02-10 09:30:41
一、总前列腺特异性抗原为何是前列腺癌的核心标志物?
前列腺特异性抗原是由前列腺上皮细胞特异性合成与分泌的一种丝氨酸蛋白酶。其生理功能主要与精液液化相关,正常情况下仅有微量透过血-前列腺屏障进入血液循环。这种高度的器官特异性使其成为目前公认的前列腺相关疾病,尤其是前列腺癌的独特血清学标志物。当前列腺组织发生恶性转化时,肿瘤的生长会破坏正常组织结构屏障,同时癌细胞可能过度产生PSA,共同导致血清总前列腺特异性抗原水平的显著升高。临床上,通常将血清TPSA浓度大于10.0 ng/mL视为具有高度提示意义的阳性临界值,其诊断前列腺癌的特异性可达90%至97%。因此,TPSA检测构成了前列腺癌筛查、辅助诊断以及高危人群风险分层的关键基石。然而,其诊断价值受到一定范围的限制,亟需更精准的检测工具以优化其应用。
二、TPSA检测在疾病管理中扮演何种角色?
TPSA的临床应用贯穿于前列腺癌管理的多个阶段。在早期筛查与诊断环节,对于无症状的男性高危人群(如年龄大于50岁或有家族史者),定期进行血清TPSA检测有助于早期发现肿瘤。当患者被确诊并接受治疗后,TPSA的动态监测则成为评估疗效与监测复发的重要手段。例如,在接受根治性前列腺切除术后的患者中,成功的治疗应使血清TPSA水平在短期内降至无法检测的极低水平。若术后PSA水平再次出现可检测到的升高,通常提示存在残留病灶或疾病复发。同样,在接受放射治疗的患者中,治疗有效者多数可在数月内观察到PSA水平显著下降至正常范围。由此可见,准确、灵敏且可重复的TPSA定量检测,是临床进行有效决策的前提。这便对检测试剂的核心组分——抗体的质量提出了严苛要求。
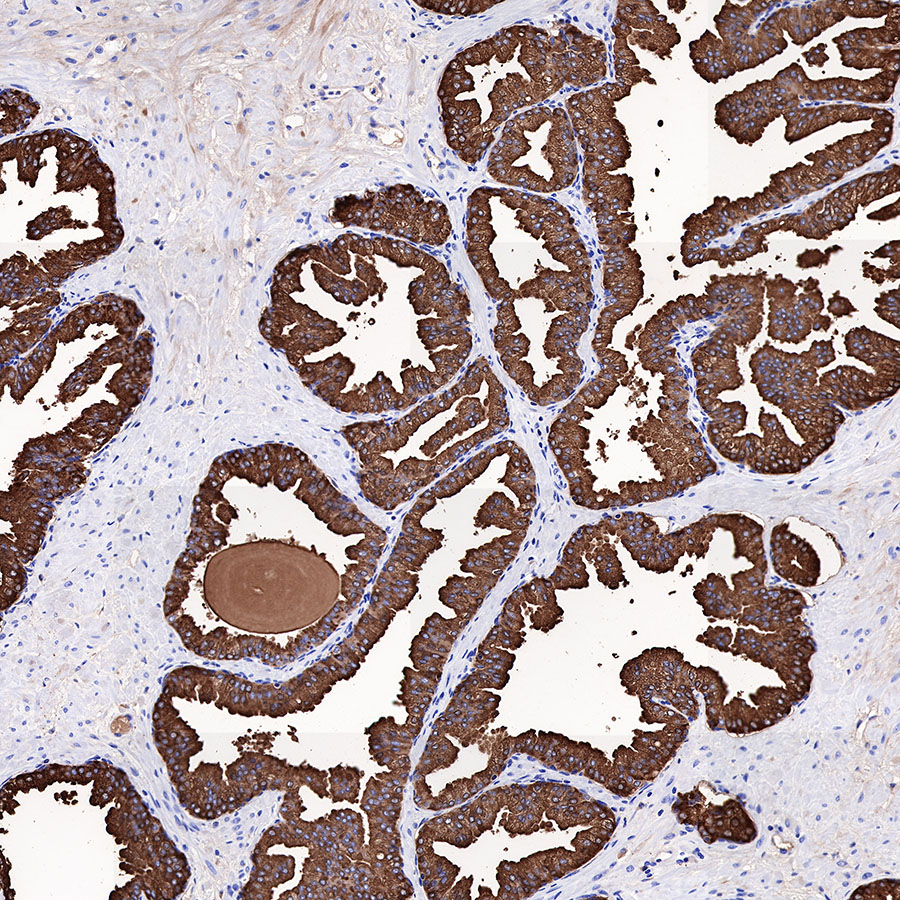
三、为何需要引入游离前列腺特异性抗原比值分析?
尽管TPSA是重要的标志物,但其单独使用存在显著局限性。主要原因在于,血清TPSA水平在4.0至10.0 ng/mL这一"诊断灰区"内时,良性的前列腺增生与早期前列腺癌患者的检测值存在大量重叠,导致基于单一TPSA值难以可靠区分良恶性病变。为克服这一挑战,临床引入了游离前列腺特异性抗原检测及FPSA/TPSA比值计算。FPSA是指未与血清中蛋白酶抑制剂结合的PSA形式。研究发现,前列腺癌患者血清中FPSA所占比例通常低于良性前列腺增生患者。当设定FPSA/TPSA比值的临界值为0.15时,该指标在鉴别诊断中展现出优越的性能:其诊断敏感性、特异性及准确性均明显超越单独使用TPSA,尤其适用于TPSA值处于2-20 ng/mL范围内的未治疗患者。这一进展凸显了同时精确测定不同PSA分子形式的重要性。
四、PSA重组兔单抗在精准检测中有何技术优势?
实现TPSA与FPSA的高精度定量检测,高度依赖于免疫分析方法的性能,而抗体的质量是决定方法优劣的核心。PSA重组兔单抗在此领域展现出多重技术优势。首先,其生产基于重组DNA技术,在哺乳动物细胞等系统中表达,确保了抗体批次间的高度均一性和稳定性,这是实现检测试剂标准化与结果可比性的基础。其次,兔源单克隆抗体通常具有比鼠源抗体更高的亲和力,这对于检测低浓度样本(如术后监测)至关重要,可有效提升检测灵敏度,降低假阴性风险。再者,通过基因工程手段,可以对抗体进行定向设计与筛选,获得针对PSA分子不同表位或不同存在形式(如特异性识别游离态而不识别结合态)的高特异性配对抗体,从而直接构建出能够准确区分并定量FPSA与总PSA的检测体系。此外,重组抗体易于进行多种标记(如酶、荧光、电化学标记),可灵活适配于化学发光、酶联免疫吸附测定、免疫层析等不同检测平台,满足从中心实验室到床旁快速检测的多样化需求。
五、如何解读PSA检测结果及注意事项?
临床医生在解读PSA检测报告时,需采取综合、审慎的态度。首先,必须认识到多种因素可影响血清PSA水平。前列腺炎、急性尿潴留、近期进行的直肠指诊、前列腺活检或膀胱镜检查等,均可能导致PSA一过性升高,造成假阳性。相反,某些治疗良性前列腺增生的药物(如5α-还原酶抑制剂)可能使PSA水平降低。因此,了解患者的近期病史与操作史对于正确判读结果至关重要。其次,应结合FPSA/TPSA比值进行综合判断,尤其是在TPSA值处于"灰区"时。但需注意,当TPSA值低于2.0 ng/mL或高于20.0 ng/mL时,该比值的鉴别诊断价值有限。最后,PSA检测不能替代病理诊断,其异常结果需结合影像学检查(如多参数磁共振成像)并最终通过前列腺穿刺活检来明确诊断。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读

