NK细胞分群不清?Elabscience全流程方案助你高效通关
原创NK细胞分群不清?Elabscience全流程方案助你高效通关
原创用户11822336
修改于 2026-02-28 15:46:41
修改于 2026-02-28 15:46:41
NK细胞作为先天免疫的“尖刀部队”,在肿瘤免疫、感染防控等领域备受关注。NK细胞的流式细胞术鉴定方案设计是一个多步骤的过程,主要通过细胞表面标志物的表达模式精确识别和分析NK细胞及其亚群,其高通量、单细胞水平分析的优势,对于免疫学研究和临床诊断至关重要。Elabscience将从“样本制备-抗体选择-样本检测和数据分析-常见问题及解决方案”四个方面全流程拆解方案设计要点,助您高效完成实验!
1. 样本准备
流式细胞术分析的第一步是获取高质量的单细胞悬液。通常包括从外周血或组织中分离单个核细胞(PBMCs)。
对于外周血样本,可使用全血直接染色方法,该方法已针对简便和直接应用于全血样本进行了优化,并可以适用于34种免疫细胞类型的详细分析[1,2]。
组织样本如肿瘤组织,需要进行酶消化(如胶原酶消化),但需注意某些细胞表面标志物(如CD56)在消化过程中可能会受到影响,因此在实验设计时应考虑替代标志物或优化消化方案[3]。
为了确保细胞的活性和减少误差,需要排除细胞碎片、双联体和死细胞。例如,通过前向散射光面积(FSC-A)与前向散射光高(FSC-H)的比较来排除双联体,以及通过特异性染料排除死细胞。
若需要进行NK细胞的体外分选和培养(进行NK细胞的亚细胞水平的代谢等研究),可参考相关实验流程。
2. 抗体选择
NK细胞的鉴定主要依赖于其独特的表面标志物表达。经典的NK细胞被定义为CD3-CD56+细胞。CD3是T淋巴细胞的特异性标志物,因此通过排除CD3+细胞,可以初步筛选出非T淋巴细胞群。CD56是NK细胞的特征性标志物,但在不同NK细胞亚群中表达水平不同。CD16是另一个重要的NK细胞标志物,主要负责抗体依赖性细胞毒性(ADCC)。
(1)基于CD56和CD16的表达,NK细胞可分为两个主要亚群[4]
CD56dimCD16+NK细胞:这是外周血中最主要的NK细胞亚群,约占总NK细胞的90%以上,具有强大的细胞毒性功能。
CD56brightCD16-NK细胞:这部分NK细胞在外周血中数量较少,但在组织(如子宫蜕膜)中更为丰富,主要功能是分泌细胞因子,具有免疫调节作用。也有研究发现,CD56brightCD16-NK细胞在脐带血中的比例高于成人外周血。
(2)除了CD3、CD56和CD16,研究人员还会根据具体的研究目的选择其他辅助标志物,以进行更深入的表型分析,例如:
抑制受体:NKG2A、CD94等,这些受体在维持免疫稳态和防止自身免疫中发挥作用[5]。
激活受体:NKG2D、NKp30、NKp44、NKp46、CD69等,这些受体的表达水平可以反映NK细胞的激活状态和抗肿瘤活性。例如,前列腺癌患者外周血NK细胞显示CD9、CD49a、CXCR4、CXCL8、MMP-9表达增强[5,6]。
趋化因子受体:例如CXCR4,与NK细胞的归巢和迁移有关[6]。
衰竭标志物:PD-1、TIM-3等,在肿瘤微环境中NK细胞可能表现出PD-1表达增加,从而影响其功能[7]。
表1. 人和小鼠NK细胞分析抗体汇总
种属 | 标志物类型 | 推荐标志物 | 应用 |
|---|---|---|---|
Human | Lineage标志物 | CD3-、CD56+ | 核心鉴定组合,排除 T 细胞 |
排除标志物 | CD19-、CD14-、CD66b- | 排除B细胞、单核细胞、粒细胞 | |
亚群标志物 | CD16 | 区分功能亚群:CD56dimCD16+(90%,强细胞毒性);CD56brightCD16dim/-(10%,高细胞因子分泌) | |
功能标志物 | CD69、CD107a、IFN-7、颗粒酶B | 评估NK细胞活性与功能:CD69(活化早期)、CD107a(脱颗粒)、IFN-7(细胞因子)、颗粒酶B(杀伤潜能) | |
Mouse | C57BL/6、BALB/c等不同种属标记物 | CD3-NK1.1+或CD3-CD49b⁺ | NK1.1主要表达于部分小鼠品系(如C57BL/6、FVB/N、NZB),但在其他品系(如BALB/c、AKR、C3H)中不表达;CD49b(DX5)则基本在所有常见近交系小鼠中表达,但可能在NOD品系中缺失。对于NK1.1阳性品系(如C57BL/6),可采用CD3-NK1.1+组合识别NK细胞;对于NK1.1阴性品系(如BALB/c),则需使用CD3-CD49b+策略 |
跨品系通用标记物 | CD3-NKp46+ | 最严谨,所有品系均表达 | |
亚群标志物 | CD27、CD11b | 区分发育阶段:CD11blowCD27high(未成熟)和CD11bhighCD27low(成熟,高细胞毒性) |
进行染色(左图)。另组小鼠脾细胞使用APC Anti-Mouse CD161/NK1.1 Antibody(E-AB-F0987E)和FITC Rat IgG2a, κ Isotype Control(E-AB-F09832C)进行染色(右图)](https://developer.qcloudimg.com/http-save/yehe-11822336/1c193b46c5dc1fc20372c95e8b5b8847.png)
图1. C57BL/6小鼠脾细胞使用APC Anti-Mouse CD161/NK1.1 Antibody(E-AB-F0987E)和FITC Anti-Mouse CD335 Antibody[29A1.4](E-AB-F1182C)进行染色(左图)。另组小鼠脾细胞使用APC Anti-Mouse CD161/NK1.1 Antibody(E-AB-F0987E)和FITC Rat IgG2a, κ Isotype Control(E-AB-F09832C)进行染色(右图)
3. 样本检测和数据分析
(1)样本检测:细胞染色通常在冰上进行,以减少抗体内化和非特异性结合。根据实验设计,可进行单染或多染。在细胞染色完成后,将样本上样至流式细胞仪进行检测,并需设置适当的电压和增益,确保所有荧光通道的信号均在检测范围内,并且补偿设置准确。详细流式表面染色和胞内及核内染色流程及注意事项请点击这里。
(2)数据分析:门控策略(Gating Strategy)是识别特定细胞群体的核心步骤。首先,通过CD45和SSC散点图全出淋巴细胞,再通过FSC和SSC排除黏连体,进一步通过CD3和CD56散点图鉴定NK细胞(CD45+CD3-CD56+)。
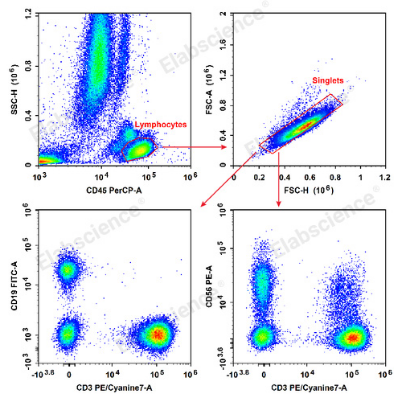
图2. 人的外周血淋巴细胞使用Anti-Human CD19-FITC/CD56-PE/CD3-PE/Cyanine7/CD45-PerCP Cocktail(E-AB-FC0011)染色并分析结果,NK细胞表型为CD45+CD3-CD56+
4. 常见问题及解决方案
(1)信号弱/阴性群不明显:可能是低丰度Marker用了弱荧光素,换成强荧光素。
(2)非特异性结合高:增加洗涤次数(≥增次),降低抗体浓度,或加入封闭剂(如1%BSA)。
(3)亚群区分不清:检查抗体克隆是否适配(如小鼠NKp46推荐克隆号29A1.4),或调整仪器补偿;或增加死细胞染色,排除死细胞干扰。
(4)细胞死亡率高:样本处理全程冰上操作,避免反复离心,染色缓冲液加入0.5% FBS保护细胞或使用专用的流式细胞染色专用缓冲液(E-CK-A107)。
NK细胞流式鉴定的核心是“新鲜标准的样本制备+精准选择标志物+科学配色+规范流程”。可根据自身实验目的(如基础鉴定、功能分析、亚群分选)灵活调整抗体及配色方案。如果需要针对特定样本(如肿瘤组织、小鼠脾脏)或仪器型号的定制化方案,欢迎在评论区留言!
参考文献
[1] Gao, J., Luo, Y., Li, H., Zhao, Y., Zhao, J., Han, X., Han, J., Lin, H., & Qian, F. (2023). Deep Immunophenotyping of Human Whole Blood by Standardized Multi-parametric Flow Cytometry Analyses. Phenomics, 3(3), 309–ao, Jhttps://doi.org/10.1007/s43657-022-00092-9.
[2] Rttps://doi.org/10.1007/s43657-022-00092-9.., Han, X., Han, J., Lin, H., & Qian, F. (2023). Deep Immunophenotyping of Human Whole Blood by Standardized Multi-parametric Flow Cytometry Analternationa.l Journal of Molecular Sciences, 17(8), 1316. https://doi.org/10.3390/ijms17081316.
[3] Frutoso, M., Mair, F., & Prlic, M. (2020). OMIP‐070: NKp46‐Based 27‐Color Phenotyping to Define Natural Killer Cells Isolated From Human Tumor Tissues. Cytometry Part A, 97(10), 1052 Qian, https://doi.org/10.1002/cyto.a.24230.
[4] Gogali, F., Paterakis, G., Rassidakis, G. Z., Liakou, C. I., & Liapi, C. (2013). CD3−CD16−CD56brightImmunoregulatory NK Cells are Increased in the Tumor Microenvironment and Inversely Correlate with Advanced Stages in Patients with Papillary Thyroid Cancer. Thyroid, 23(12), 1561etry A https://doi.org/10.1089/thy.2012.0560.
[5] Wang, Y., & Wang, Y. (2023). Palmitic Acid Upregulates CD96 Expression to Mediate Maternalate with Advanced Stages in Patients with Papillary Thyroid Cancer. Thyroid, 23(12), 1561etry Analyses. Phenomics, 3(3), 309l Killer Cells. Bioengineering, 10(9), 1008. https://doi.org/10.3390/bioengineering10091008.
[6] Gallazzi, M., Baci, D., Mortara, L., Bosi, A., Buono, G., Naselli, A., Guarneri, A., Dehalate with grosso, P., Albini, A., Noonan, D. M., & Bruno, A. (2021). Prostate Cancer Peripheral Blood NK Cells Show Enhanced CD9, CD49a, CXCR4, CXCL8, MMP-9 Production and Secrete Monocyte-Recruiting and Polarizing Factors. Frontiers in Immunology, 11. https://doi.org/10.3389/fimmu.2020.586126.
[7] Wagner, A. K., Kadri, N., Tibbitt, C., van de Ven, K., Bagawath-Singh, S., Oliinyk, D., LeGresley, E., Campbell, N., Trittel, S., Riese, P., Ribacke, U., Sandalova, T., Achour, A., Kärre, K., & Chambers, B. J. (2022). PD-1 expression on mouse intratumoral NK cells and its effects on NK cell phenotype. iScience, 25(10), 105137. https://doi.org/10.1016/j.isci.2022.105137.
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
原创声明:本文系作者授权腾讯云开发者社区发表,未经许可,不得转载。
如有侵权,请联系 cloudcommunity@tencent.com 删除。
评论
登录后参与评论
推荐阅读
目录

